Science:全文解读!开发出CRISPR LiveFISH技术,成功对活细胞中的DNA和RNA进行实时成像
来源:本站原创 2019-09-30 21:58
2019年9月30日讯/生物谷BIOON/---基因组编辑可以诱导包括易位在内的染色体重排。尽管测序方法已用于鉴定和描述与遗传疾病和基因编辑有关的染色体异常,但是染色体重排的时间动态变化鲜为人知。之前的研究依赖于使用基因组整合的LacO/TetO阵列,这既枯燥又有挑战性。与荧光蛋白融合在一起的没有核酸酶活性的dCas9,或者招募单向导RNA(sgRNA)的与荧光蛋白融合在一起的RNA结合蛋白能够对
2019年9月30日讯/生物谷BIOON/---基因组编辑可以诱导包括易位在内的染色体重排。尽管测序方法已用于鉴定和描述与遗传疾病和基因编辑有关的染色体异常,但是染色体重排的时间动态变化鲜为人知。
之前的研究依赖于使用基因组整合的LacO/TetO阵列,这既枯燥又有挑战性。与荧光蛋白融合在一起的没有核酸酶活性的dCas9,或者招募单向导RNA(sgRNA)的与荧光蛋白融合在一起的RNA结合蛋白能够对基因组位点进行CRISPR介导的实时成像。但是,对编码CRISPR组件的DNA的需要限制了它的使用。传统的荧光原位杂交(FISH)需要DNA变性,同时在体外与sgRNA组装在一起的荧光标记dCas9(CASFISH)仅检测固定样本中的基因组位点,这就限制了实时追踪。

在一项新的研究中,来自美国斯坦福大学、卡斯迪加学校和中国浙江大学的研究人员报道了一种称为CRISPR活细胞荧光原位杂交(CRISPR live-cell fluorescent in situ hybridization, CRISPR LiveFISH)的实时成像方法,从而允许研究活细胞中的各种染色体功能。相关研究结果发表在2019年9月20日的Science期刊上,论文标题为“CRISPR-mediated live imaging of genome editing and transcription”。
这些研究人员首次将等摩尔含量的蛋白dCas9-EGFP(即与增强型绿色荧光蛋白融合在一起的dCas9)和经过Cy3标记的向导RNA(gRNA)组装成荧光核糖核蛋白(fRNP),所组装而成的fRNP靶向3号染色体(Chr3)中的一个重复序列区域(Chr3q29,大约500次重复)。他们通过电穿孔将fRNP递送到人骨肉瘤U2OS细胞中。流式细胞仪分析表明95%以上的gRNA信号在转染之后的4小时内受到降解,这与之前报道的gRNA在细胞环境中高度不稳定相一致。然而,他们观察到Cy3-gRNA对这个Chr3位点(即Chr3q29)的快速且持久的标记,这表明稳定的与靶标结合在一起的dCas9-gRNA复合物形成了。Cy3-gRNA的信噪比(signal-to-background ratio, S/B)比dCas9-EGFP的S/B高4倍以上。与经常在核仁中聚集的dCas9-EGFP不同的是,Cy3-gRNA并不在核仁中聚集。通过进行体外测定,他们发现过量的靶DNA而不是非靶DNA,保护Cas9:gRNA:DNA三元复合物中的Cy3-gRNA免受核糖核酸酶A降解。此外,相比于存在不小于6个碱基对(bp)错配的靶DNA,结合着dCas9的Cy3-gRNA更好地受到完全匹配的靶DNA或者在PAM(protospacer adjacent motif, 前间隔序列邻近基序)远端存在不大于4bp错配的靶DNA的保护。
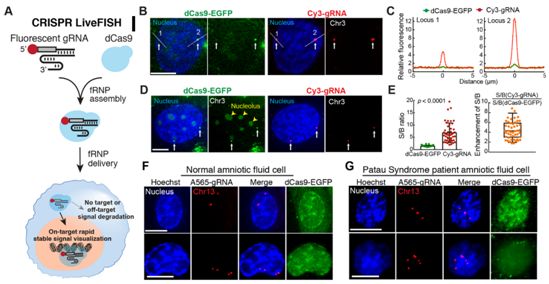
基于这种靶DNA依赖性的gRNA保护,这些研究人员开发出CRISPR LiveFISH,即一种部署与dCas9组装在一起的荧光gRNA探针来靶向和标记活细胞中基因组序列的方法。他们在来自巴陶综合征(Patau Syndrome)患者的细胞中测试了这种方法,其中巴陶综合征是一种13号染色体(Chr13)三体遗传病,它导致器官缺陷、智能障碍和身体缺陷,并且最终是致命性的。他们将含有dCas9和Atto565标记的gRNA(Atto565-gRNA)且靶向Chr13上的一个重复序列区域(Chr13q34,大约350次重复)的fRNP转染到正常的或者源自患者的产前羊水细胞中,并检测到Atto565-gRNA快速且稳健地标记Chr13,这优于dCas9-EGFP RNP标记或基于质粒的成像。CRISPR LiveFISH的高效率可通过核型分析进行定量,它的准确性可通过核型分析进行证实。简单地共递送经过不同的荧光团标记的fRNP能够同时地可视化观察U2OS细胞和人原代T细胞中的Chr3重复序列区域和Chr13重复序列区域。之前利用正交dCas9或将sgRNA与RNA适配体(RNA aptamer)和RNA结合蛋白偶联在一起的方法需要多个构造体。
这些研究人员随后利用CRISPR LiveFISH来研究CRISPR-Cas9在活细胞中诱导的DNA双链断裂(DSB)的实时动态变化。他们构建出稳定地表达与荧光Apple蛋白融合在一起的截断53BP1蛋白(aa1220-1711)的U2OS细胞系(以下称为U2OS-53BP1-Apple细胞),其中53BP1蛋白是一种得到很好描述的DNA DSB传感蛋白。人类基因组含有通常与大多数蛋白编码基因(>60%)相邻的重复序列(<100kb)。他们通过核转染方法将切割Chr3中PPP1R2基因的基因编辑RNP(Cas9/gPPP1R2)和对Chr3q29重复序列区域进行标记的CRISPR LiveFISH fRNP(Cas9/A488-gChr3)共递送到U2OS-53BP1-Apple细胞中,其中Chr3q29重复序列区域与PPP1R2切割位点相距36kb。为了避免fRNP介导的DNA切割,他们针对成像gRNA使用了一个短的间隔序列,这不足以进行DNA切割。在转染后不久,他们很快就观察到在含有基因编辑gRNA的细胞中,较高比例的Chr3q29位点与53BP1位点共定位在一起,这表明在PPP1R2位点上快速形成了Cas9诱导的DSB。按序递送成像fRNP和基因编辑RNP能够让他们随着时间的推移追踪单个位点上的DSA形成和53BP1招募过程。在递送基因编辑RNP之后,他们连续数小时地捕捉到53BP1位点快速地和正在招募到53BP1位点。
这些研究人员能够追踪基因编辑事件的动态变化。比如,他们观察到53BP1位点招募Chr3q29位点,随后与Chr3q29位点脱离开来,这可能表明成功修复了DNA DSB。他们还在很多细胞的单个DNA位点上观察到53BP1位点的重复招募和脱离,这表明对靶DNA重复进行切割和修复。最终,在将基因编辑RNP递送到一些细胞之后,多个Chr3q29位点簇集在相同的53BP1位点内,这表明正如之前报道的那样,在DNA DSB位点之间发生同源配对。最初在单独的Chr3q29位点上形成的两个53BP1小体快速地融合在一起,相应地这些同源的Chr3q29位点在融合的53BP1小体内相互作用,这表明53BP1小体融合可能促进同源DSB位点配对。
利用CRISPR对多个基因进行编辑对基因疗法比较重要,但是这能够引入有害的非同源染色体重排。为了可视化观察染色体易位,这些研究人员共递送靶向Chr3中PPP1R2和Chr13中SPACA7的基因编辑RNP和CRISPR LiveFISH fRNP来追踪Chr3q29和Chr13q34(与SPACA7切割位点相距82kb)。在通常是非整倍体的U2OS细胞中,53BP1免疫染色证实了DSB在靶位点上形成。他们能够观察到Chr3q29位点和Chr13q34位点之间的配对。这两个位点显示了几乎相同的运动轨迹,而且它们之间的距离几乎保持恒定,这表明这两个位点之间可能物理连接。他们追踪了这些染色体易位的动态变化。Chr3q29和Chr13q34最初是分开的,随后彼此靠近,并且在很长一段时间内保持在一起,这可能代表着内源性非同源染色体易位。他们还捕捉瞬时事件,在这些瞬时事件中,Chr3q29位点和Chr13q34位点短暂地一起移动并分离开来。为了独立地证实染色体易位,他们进行发生易位的染色体片段进行克隆、测序和验证。
这些研究人员进一步扩展了CRISPR LiveFISH,以便实时地对DNA和RNA进行成像观察。他们利用催化失活的Cas13d(CasRx)--- dCas13d---和人工合成的荧光标记gRNA进行靶RNA成像观察。U2OS 2-6-3细胞系携带一个位于强力霉素(Dox)诱导性基因盒上游的LacO重复序列阵列,其中这种基因盒含有MS2重复序列阵列。为了同时可视化观察DNA和RNA,他们设计了Atto488标记的靶向LacO DNA的Cas9 gRNA(下称gLacO),设计了Atto647标记的靶向MS2 RNA的Cas13d gRNA(下称gMS2)。通过共递送gMS2和dCas9/gLacO到表达dCas13d的U2OS 2-6-3细胞中,他们成功地在Dox的存在下对DNA位点和RNA转录本进行标记。CRISPR LiveFISH也能够让他们追踪活细胞中RNA转录的实时动态变化。在利用高浓度Dox诱导转录后,他们在一段时间内观察到MS2转录本在LacO位点附近主逐渐地聚集。
终上所述,这些研究人员报道了用于活细胞DNA和RNA成像的CRISPR LiveFISH技术。化学合成的荧光gRNA与dCas蛋白形成的复合物能够促进快速稳健地、可扩展地对细胞(包括原代细胞)中的基因组DNA进行追踪和对细胞中的RNA进行成像。在富含核糖核酸酶的环境中,对Cas9:gRNA:DNA三元复合物中gRNA的靶DNA依赖性保护会富集靶信号,同时让背景噪音最小化。CRISPR LiveFISH也允许对活细胞中内源性基因组位点上发生的CRISPR诱导的基因编辑和易位事件进行动态追踪。使用dCas9和dCas13系统的双DNA/RNA CRISPR LiveFISH能够对相同细胞中的基因组DNA和RNA转录本进行实时成像。人们有可能将CRISPR LiveFISH与其他的基因操纵技术(比如,CRISPRi/a、表观遗传修饰和CRISPR-GO)结合使用来加深对基因组组装和细胞核事件的时空动态变化的理解。(生物谷 Bioon.com)
参考资料:
Haifeng Wang et al. CRISPR-mediated live imaging of genome editing and transcription. Science, 2019, doi:10.1126/science.aax7852.
之前的研究依赖于使用基因组整合的LacO/TetO阵列,这既枯燥又有挑战性。与荧光蛋白融合在一起的没有核酸酶活性的dCas9,或者招募单向导RNA(sgRNA)的与荧光蛋白融合在一起的RNA结合蛋白能够对基因组位点进行CRISPR介导的实时成像。但是,对编码CRISPR组件的DNA的需要限制了它的使用。传统的荧光原位杂交(FISH)需要DNA变性,同时在体外与sgRNA组装在一起的荧光标记dCas9(CASFISH)仅检测固定样本中的基因组位点,这就限制了实时追踪。

在一项新的研究中,来自美国斯坦福大学、卡斯迪加学校和中国浙江大学的研究人员报道了一种称为CRISPR活细胞荧光原位杂交(CRISPR live-cell fluorescent in situ hybridization, CRISPR LiveFISH)的实时成像方法,从而允许研究活细胞中的各种染色体功能。相关研究结果发表在2019年9月20日的Science期刊上,论文标题为“CRISPR-mediated live imaging of genome editing and transcription”。
这些研究人员首次将等摩尔含量的蛋白dCas9-EGFP(即与增强型绿色荧光蛋白融合在一起的dCas9)和经过Cy3标记的向导RNA(gRNA)组装成荧光核糖核蛋白(fRNP),所组装而成的fRNP靶向3号染色体(Chr3)中的一个重复序列区域(Chr3q29,大约500次重复)。他们通过电穿孔将fRNP递送到人骨肉瘤U2OS细胞中。流式细胞仪分析表明95%以上的gRNA信号在转染之后的4小时内受到降解,这与之前报道的gRNA在细胞环境中高度不稳定相一致。然而,他们观察到Cy3-gRNA对这个Chr3位点(即Chr3q29)的快速且持久的标记,这表明稳定的与靶标结合在一起的dCas9-gRNA复合物形成了。Cy3-gRNA的信噪比(signal-to-background ratio, S/B)比dCas9-EGFP的S/B高4倍以上。与经常在核仁中聚集的dCas9-EGFP不同的是,Cy3-gRNA并不在核仁中聚集。通过进行体外测定,他们发现过量的靶DNA而不是非靶DNA,保护Cas9:gRNA:DNA三元复合物中的Cy3-gRNA免受核糖核酸酶A降解。此外,相比于存在不小于6个碱基对(bp)错配的靶DNA,结合着dCas9的Cy3-gRNA更好地受到完全匹配的靶DNA或者在PAM(protospacer adjacent motif, 前间隔序列邻近基序)远端存在不大于4bp错配的靶DNA的保护。

图片来自Science, 2019, doi:10.1126/science.aax7852。
基于这种靶DNA依赖性的gRNA保护,这些研究人员开发出CRISPR LiveFISH,即一种部署与dCas9组装在一起的荧光gRNA探针来靶向和标记活细胞中基因组序列的方法。他们在来自巴陶综合征(Patau Syndrome)患者的细胞中测试了这种方法,其中巴陶综合征是一种13号染色体(Chr13)三体遗传病,它导致器官缺陷、智能障碍和身体缺陷,并且最终是致命性的。他们将含有dCas9和Atto565标记的gRNA(Atto565-gRNA)且靶向Chr13上的一个重复序列区域(Chr13q34,大约350次重复)的fRNP转染到正常的或者源自患者的产前羊水细胞中,并检测到Atto565-gRNA快速且稳健地标记Chr13,这优于dCas9-EGFP RNP标记或基于质粒的成像。CRISPR LiveFISH的高效率可通过核型分析进行定量,它的准确性可通过核型分析进行证实。简单地共递送经过不同的荧光团标记的fRNP能够同时地可视化观察U2OS细胞和人原代T细胞中的Chr3重复序列区域和Chr13重复序列区域。之前利用正交dCas9或将sgRNA与RNA适配体(RNA aptamer)和RNA结合蛋白偶联在一起的方法需要多个构造体。
这些研究人员随后利用CRISPR LiveFISH来研究CRISPR-Cas9在活细胞中诱导的DNA双链断裂(DSB)的实时动态变化。他们构建出稳定地表达与荧光Apple蛋白融合在一起的截断53BP1蛋白(aa1220-1711)的U2OS细胞系(以下称为U2OS-53BP1-Apple细胞),其中53BP1蛋白是一种得到很好描述的DNA DSB传感蛋白。人类基因组含有通常与大多数蛋白编码基因(>60%)相邻的重复序列(<100kb)。他们通过核转染方法将切割Chr3中PPP1R2基因的基因编辑RNP(Cas9/gPPP1R2)和对Chr3q29重复序列区域进行标记的CRISPR LiveFISH fRNP(Cas9/A488-gChr3)共递送到U2OS-53BP1-Apple细胞中,其中Chr3q29重复序列区域与PPP1R2切割位点相距36kb。为了避免fRNP介导的DNA切割,他们针对成像gRNA使用了一个短的间隔序列,这不足以进行DNA切割。在转染后不久,他们很快就观察到在含有基因编辑gRNA的细胞中,较高比例的Chr3q29位点与53BP1位点共定位在一起,这表明在PPP1R2位点上快速形成了Cas9诱导的DSB。按序递送成像fRNP和基因编辑RNP能够让他们随着时间的推移追踪单个位点上的DSA形成和53BP1招募过程。在递送基因编辑RNP之后,他们连续数小时地捕捉到53BP1位点快速地和正在招募到53BP1位点。
这些研究人员能够追踪基因编辑事件的动态变化。比如,他们观察到53BP1位点招募Chr3q29位点,随后与Chr3q29位点脱离开来,这可能表明成功修复了DNA DSB。他们还在很多细胞的单个DNA位点上观察到53BP1位点的重复招募和脱离,这表明对靶DNA重复进行切割和修复。最终,在将基因编辑RNP递送到一些细胞之后,多个Chr3q29位点簇集在相同的53BP1位点内,这表明正如之前报道的那样,在DNA DSB位点之间发生同源配对。最初在单独的Chr3q29位点上形成的两个53BP1小体快速地融合在一起,相应地这些同源的Chr3q29位点在融合的53BP1小体内相互作用,这表明53BP1小体融合可能促进同源DSB位点配对。
利用CRISPR对多个基因进行编辑对基因疗法比较重要,但是这能够引入有害的非同源染色体重排。为了可视化观察染色体易位,这些研究人员共递送靶向Chr3中PPP1R2和Chr13中SPACA7的基因编辑RNP和CRISPR LiveFISH fRNP来追踪Chr3q29和Chr13q34(与SPACA7切割位点相距82kb)。在通常是非整倍体的U2OS细胞中,53BP1免疫染色证实了DSB在靶位点上形成。他们能够观察到Chr3q29位点和Chr13q34位点之间的配对。这两个位点显示了几乎相同的运动轨迹,而且它们之间的距离几乎保持恒定,这表明这两个位点之间可能物理连接。他们追踪了这些染色体易位的动态变化。Chr3q29和Chr13q34最初是分开的,随后彼此靠近,并且在很长一段时间内保持在一起,这可能代表着内源性非同源染色体易位。他们还捕捉瞬时事件,在这些瞬时事件中,Chr3q29位点和Chr13q34位点短暂地一起移动并分离开来。为了独立地证实染色体易位,他们进行发生易位的染色体片段进行克隆、测序和验证。
这些研究人员进一步扩展了CRISPR LiveFISH,以便实时地对DNA和RNA进行成像观察。他们利用催化失活的Cas13d(CasRx)--- dCas13d---和人工合成的荧光标记gRNA进行靶RNA成像观察。U2OS 2-6-3细胞系携带一个位于强力霉素(Dox)诱导性基因盒上游的LacO重复序列阵列,其中这种基因盒含有MS2重复序列阵列。为了同时可视化观察DNA和RNA,他们设计了Atto488标记的靶向LacO DNA的Cas9 gRNA(下称gLacO),设计了Atto647标记的靶向MS2 RNA的Cas13d gRNA(下称gMS2)。通过共递送gMS2和dCas9/gLacO到表达dCas13d的U2OS 2-6-3细胞中,他们成功地在Dox的存在下对DNA位点和RNA转录本进行标记。CRISPR LiveFISH也能够让他们追踪活细胞中RNA转录的实时动态变化。在利用高浓度Dox诱导转录后,他们在一段时间内观察到MS2转录本在LacO位点附近主逐渐地聚集。
终上所述,这些研究人员报道了用于活细胞DNA和RNA成像的CRISPR LiveFISH技术。化学合成的荧光gRNA与dCas蛋白形成的复合物能够促进快速稳健地、可扩展地对细胞(包括原代细胞)中的基因组DNA进行追踪和对细胞中的RNA进行成像。在富含核糖核酸酶的环境中,对Cas9:gRNA:DNA三元复合物中gRNA的靶DNA依赖性保护会富集靶信号,同时让背景噪音最小化。CRISPR LiveFISH也允许对活细胞中内源性基因组位点上发生的CRISPR诱导的基因编辑和易位事件进行动态追踪。使用dCas9和dCas13系统的双DNA/RNA CRISPR LiveFISH能够对相同细胞中的基因组DNA和RNA转录本进行实时成像。人们有可能将CRISPR LiveFISH与其他的基因操纵技术(比如,CRISPRi/a、表观遗传修饰和CRISPR-GO)结合使用来加深对基因组组装和细胞核事件的时空动态变化的理解。(生物谷 Bioon.com)
参考资料:
Haifeng Wang et al. CRISPR-mediated live imaging of genome editing and transcription. Science, 2019, doi:10.1126/science.aax7852.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


