基于机制的脓毒性休克疗法!“十二肽”TREM-1抑制剂nangibotide获美FDA快速通道资格!
来源:本站原创 2019-09-04 10:09
2019年09月04日讯 /生物谷BIOON/ --Inotrem S.A.是一家专门从事急性和慢性炎症综合征免疫治疗的生物技术公司。近日,该公司宣布,美国食品和药物管理局(FDA)已授予nangibotide(LR12)治疗脓毒性休克的快速通道资格(Fast Track designation,FTD)。脓毒性休克(septic shock)是脓毒症的最终并发症。在发达国家,脓毒性休克的发生率持

2019年09月04日讯 /生物谷BIOON/ --Inotrem S.A.是一家专门从事急性和慢性炎症综合征免疫治疗的生物技术公司。近日,该公司宣布,美国食品和药物管理局(FDA)已授予nangibotide(LR12)治疗脓毒性休克的快速通道资格(Fast Track designation,FTD)。
脓毒性休克(septic shock)是脓毒症的最终并发症。在发达国家,脓毒性休克的发生率持续上升、死亡率仍然很高(35%)。除了抗生素和对症治疗外,目前还没有专门的药物获批针对这一适应症。
nangibotide有潜力成为第一种基于机制的脓毒性休克治疗药物,该药是一种TREM-1抑制剂,有潜力恢复适当的炎症反应、血管功能并提高脓毒性休克后的存活率。
快速通道资格(FTD)旨在加速针对严重疾病的药物开发和快速审查,以解决关键领域严重未获满足的医疗需求。实验性药物获得快速通道资格,意味着药企在研发阶段可以与FDA进行更频繁的会晤,在提交上市申请后如果符合相关标准则有资格进行加速审批和优先审查,以及滚动审查的机会。滚动审查允许药企将其生物制品许可申请(BLA)或新药申请(NDA)中已完成的部分提交给FDA,而不必等到每个部分都完成后再审查整个BLA或NDA。
Inotrem公司首席执行官兼联合创始人Jean Jacques Garaud表示:“FDA授予nangibotide快速通道资格认定,是对公司用于急性炎症管理创新疗法的认可,同时也突显了严重疾病(诸如脓毒性休克)对病因治疗的关键需求。我们期待着与FDA密切合作,推进我们计划开展的ASTONISH临床试验,并加快努力为脓毒性休克患者提供首个有效疗法。”
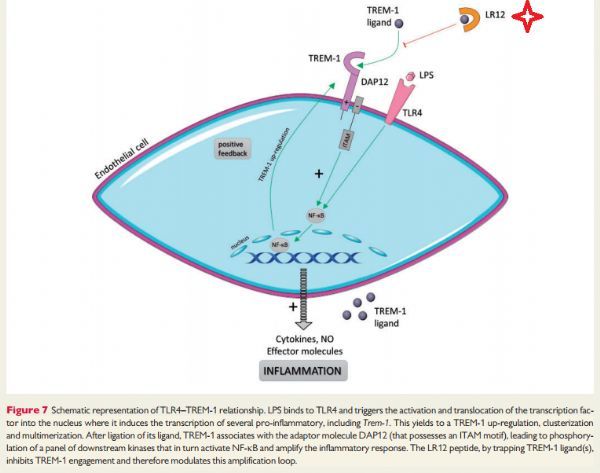
LR12肽捕获TREM-1配体、抑制TREM-1参与,从而调节炎症放大回路(来源文献2)
先天免疫系统构成了抵御入侵微生物病原体的第一道防线。TREM-1(髓样细胞-1上表达的触发受体)是一种在先天免疫细胞上表达的免疫受体。TREM-1调节炎症、导致一种旺盛的免疫反应的产生。与大多数抑制剂不同,基于TREM-1的抑制剂具有独特的治疗能力:利用免疫调节能力可以控制导致患者观察到的有害影响的原因,但不完全消除炎症反应,炎症反应仍然是必要的,例如对于细菌清除。
Inotrem公司发现TREM-1通路是导致炎症反应不平衡的关键因素,并以此为核心目标,开发基于TREM-1抑制的创新个体化医疗方法,用于以急性或慢性炎症综合征为特征的适应症。
nangibotide是活性成分LR12的制剂,LR12是一种化学合成的长度12个氨基酸的肽。LR12是一种特殊的TREM-1抑制剂,作为诱饵受体,干扰TREM-1与其配体的结合。在临床前脓毒性休克模型中,nangibotide能够恢复适当的炎症反应、血管功能,并提高动物脓毒性休克后的存活率。
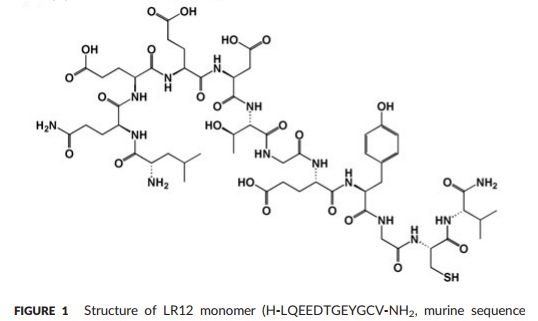
LR12单体结构(图片来源文献3)
最近,Inotrem公司IIb期研究ASTONISH的临床试验申请(IND)获得了FDA的批准。该公司将于今年晚些时候开始对脓毒性休克患者进行计划中的这项全球多中心IIb期研究,该研究的目的是证明nangibotide的疗效,并为脓毒性休克患者中的临床活性提供临床相关证据。此外,该研究还将验证一种个体化的医疗方法,使用可溶性TREM-1作为潜在的伴随诊断测试,识别更可能受益于nangibotide治疗的患者。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->