Cell:震惊!肿瘤微生物组竟能决定癌症患者的生死
来源:本站原创 2019-08-17 12:50
2019年8月17日讯/生物谷BIOON/---在一项新的研究中,来自美国德克萨斯大学MD安德森癌症研究中心的研究人员发现少数长期存活的胰腺癌患者与许多对所有治疗方案都无效的胰腺癌患者之间的一个关键区别在于他们的肿瘤中的细菌群落刺激或抑制免疫反应。相关研究结果发表在2019年8月8日的Cell期刊上,论文标题为“Tumor Microbiome Diversity and Composition
2019年8月17日讯/生物谷BIOON/---在一项新的研究中,来自美国德克萨斯大学MD安德森癌症研究中心的研究人员发现少数长期存活的胰腺癌患者与许多对所有治疗方案都无效的胰腺癌患者之间的一个关键区别在于他们的肿瘤中的细菌群落刺激或抑制免疫反应。相关研究结果发表在2019年8月8日的Cell期刊上,论文标题为“Tumor Microbiome Diversity and Composition Influence Pancreatic Cancer Outcomes”。
这些研究人员还发现来自长期存活者的粪便菌群移植(fecal microbiota transplant, FMT)通过改变肿瘤中的细菌---肿瘤微生物组,促进小鼠模型中的免疫反应和抑制肿瘤。
论文通讯作者、德克萨斯大学MD安德森癌症研究中心临床癌症预防助理教授Florencia McAllister博士说道,“FMT实验的结果代表着通过改变肿瘤免疫微环境来改善胰腺癌治疗的重要治疗机会。这是有前景的,但我们还有很多研究工作要做。”
德克萨斯大学MD安德森癌症研究中心的胰腺癌登月计划(Pancreatic Cancer Moon Shot)为McAllister提供了资金,用于开展针对胰腺癌的FMT临床试验。胰腺癌登月计划是一个合作项目,旨在加速科学发现向临床进展的转化,从而挽救患者的生命。
大多数胰腺导管腺癌(pancreatic ductal adenocarcinoma, PDAC)---最常见的胰腺癌形式 ---患者在确诊时通常处于这种疾病的晚期阶段,仅有9%的患者可存活五年。那些接受过手术切除的早期癌症患者具有较高的复发率,中位生存期为24~30个月。
McAllister说道,目前还没有发现能够解释这部分患者长期存活原因的基因组生物标志物。
长期存活者具有多样化的肿瘤微生物组
McAllister说道,虽然近期的研究已表明生活在消化道中的微生物的组成和多样性---肠道微生物组---能够影响癌症免疫治疗的作用方式,但是很少有研究关注肿瘤中的细菌以及它如何影响预后和存活。“我们已知道胰腺瘤中有细菌,因此我们想知道,'这些细菌是否在癌症中发挥作用?'”
为了开展胰腺癌领域的首次此类研究,McAllister及其同事们分析了长期存活者和短期存活者肿瘤中的细菌DNA并进行匹配,这些患者来自德克萨斯大学MD安德森癌症研究中心和约翰霍普金斯医院的两个独立队列(下称MD Anderson队列和霍普金斯医院队列)。在MD Anderson队列中,长期存活者(22名患者)的中位生存期为10年,短期存活者(21名患者)的中位生存期为1.6年。在霍普金斯医院队列中,15名患者的总生存期超过10年,10名患者的存活期不到5年。
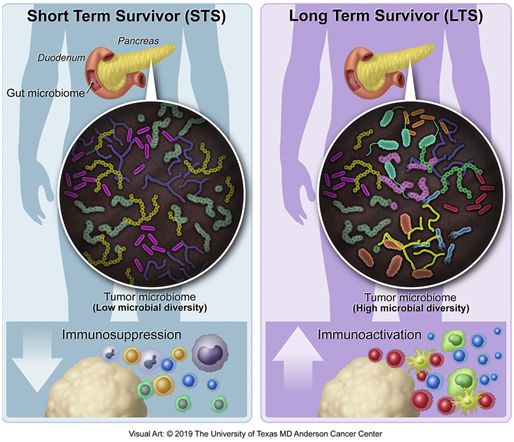
这些研究人员通过使用16S rRNA基因测序,发现长期存活者的细菌种类多样性远远超过短期存活者。仅通过这种多样性测量对来自MD Anderson队列的患者进行分类表明具有高度多样性的患者的中位生存期为9.66岁,而多样性较低的患者的中位生存期为1.66年。
这种多样性结果与诸如之前采用的疗法、身体质量指数(BMI)和抗生素使用之类的其他因素无关,这就使得它成为患者存活的预测因子,并指出肿瘤微生物组在癌症进展中的潜在重要性。
这些研究人员还发现在长期存活者和短期存活者群体中发现的细菌群落存在显著差异。长期存活者表现出相对丰富的假黄色单胞菌(Pseudoxanthomonas)、Saccharropolyspora和链霉菌(Streptomyces)。所有这三个细菌分类群以及克劳氏芽孢杆菌(Bacillus Clausii)的存在预示着这两个队列中患者具有更好治疗结果。
特定的微生物组增强了对肿瘤的免疫攻击
免疫组织化学显示这两个队列中长期存活者的肿瘤具有更大的T细胞密度,包括CD8阳性杀伤性T细胞,这就与之前的研究结果---长期存活者具有更强的免疫反应---相一致。
McAllister及其同事们发现免疫细胞浸润与肿瘤中的微生物组多样性之间存在很强的相关性。进一步的分析表明,T细胞的免疫浸润和活化与长期存活者肿瘤中发现的三种富集的细菌类型有关。
由于肿瘤微生物组与免疫反应之间存在明显的关联性,McAllister及其团队着手寻找改变肿瘤微生物组的方法。
利用肠道微生物组改变肿瘤微生物组
McAllister说道,“不能够直接调节肿瘤微生物组,但是你能够调节肠道微生物组,而且如果肠道微生物组和肿瘤微生物组存在交谈的话,那么你能够间接地改变肿瘤微生物组。”
McAllister团队比较了三名手术患者的肠道、肿瘤和邻近组织中的细菌。他们发现肠道微生物组大约占肿瘤微生物组的25%,但在正常的邻近组织中不存在,这表明肠道中的细菌能够能在胰腺瘤中定植。
这些研究人员将晚期癌症患者的粪便菌群移植到小鼠体内,发现供者微生物组大约占由此产生的肿瘤微生物组的5%,但是整个肿瘤微生物组的70%已被移植的粪便菌群改变。
McAllister说道,“如今我们知道你能够通过FMT完全改变肿瘤微生物组中的细菌组成。”
利用FMT逆转免疫抑制
接下来,他们将来自晚期胰腺癌患者、存活超过5年且无疾病迹象的患者和健康对照者的粪便菌群移植到小鼠体内。
在肿瘤产生五周后,接受来自晚期胰腺癌患者的粪便菌群移植的小鼠具有更大的肿瘤,而接受来自长期存活者的粪便菌群移植的小鼠体内的肿瘤的平均大小减少了70%,接受来自健康对照者的粪便菌群移植的小鼠体内的肿瘤的平均大小减少了50%。
免疫分析显示与其他两组相比,接受来自长期存活者的粪便菌群移植的小鼠具有显著更高的CD8阳性T细胞数量和更大的CD8阳性T细胞活化。接受来自晚期胰腺癌患者的粪便菌群移植的小鼠具有增加的调节性T细胞和髓源性抑制细胞,这两种细胞都抑制免疫反应。
为了评估FMT的作用是否依赖于免疫系统,这些研究人员剔除了一组接受来自长期存活者的粪便菌群移植的小鼠中的T细胞,这完全阻断了FMT的抗肿瘤作用。(生物谷 Bioon.com)
参考资料:
1.Erick Riquelme et al. Tumor Microbiome Diversity and Composition Influence Pancreatic Cancer Outcomes. Cell, 2019, doi:10.1016/j.cell.2019.07.008.
3.Study finds specific microbiome tied to long-term survival of patients with pancreatic cancer
https://medicalxpress.com/news/2019-08-specific-microbiome-tied-long-term-survival.html

这些研究人员还发现来自长期存活者的粪便菌群移植(fecal microbiota transplant, FMT)通过改变肿瘤中的细菌---肿瘤微生物组,促进小鼠模型中的免疫反应和抑制肿瘤。
论文通讯作者、德克萨斯大学MD安德森癌症研究中心临床癌症预防助理教授Florencia McAllister博士说道,“FMT实验的结果代表着通过改变肿瘤免疫微环境来改善胰腺癌治疗的重要治疗机会。这是有前景的,但我们还有很多研究工作要做。”
德克萨斯大学MD安德森癌症研究中心的胰腺癌登月计划(Pancreatic Cancer Moon Shot)为McAllister提供了资金,用于开展针对胰腺癌的FMT临床试验。胰腺癌登月计划是一个合作项目,旨在加速科学发现向临床进展的转化,从而挽救患者的生命。
大多数胰腺导管腺癌(pancreatic ductal adenocarcinoma, PDAC)---最常见的胰腺癌形式 ---患者在确诊时通常处于这种疾病的晚期阶段,仅有9%的患者可存活五年。那些接受过手术切除的早期癌症患者具有较高的复发率,中位生存期为24~30个月。
McAllister说道,目前还没有发现能够解释这部分患者长期存活原因的基因组生物标志物。
长期存活者具有多样化的肿瘤微生物组
McAllister说道,虽然近期的研究已表明生活在消化道中的微生物的组成和多样性---肠道微生物组---能够影响癌症免疫治疗的作用方式,但是很少有研究关注肿瘤中的细菌以及它如何影响预后和存活。“我们已知道胰腺瘤中有细菌,因此我们想知道,'这些细菌是否在癌症中发挥作用?'”
为了开展胰腺癌领域的首次此类研究,McAllister及其同事们分析了长期存活者和短期存活者肿瘤中的细菌DNA并进行匹配,这些患者来自德克萨斯大学MD安德森癌症研究中心和约翰霍普金斯医院的两个独立队列(下称MD Anderson队列和霍普金斯医院队列)。在MD Anderson队列中,长期存活者(22名患者)的中位生存期为10年,短期存活者(21名患者)的中位生存期为1.6年。在霍普金斯医院队列中,15名患者的总生存期超过10年,10名患者的存活期不到5年。
这些研究人员通过使用16S rRNA基因测序,发现长期存活者的细菌种类多样性远远超过短期存活者。仅通过这种多样性测量对来自MD Anderson队列的患者进行分类表明具有高度多样性的患者的中位生存期为9.66岁,而多样性较低的患者的中位生存期为1.66年。
这种多样性结果与诸如之前采用的疗法、身体质量指数(BMI)和抗生素使用之类的其他因素无关,这就使得它成为患者存活的预测因子,并指出肿瘤微生物组在癌症进展中的潜在重要性。
这些研究人员还发现在长期存活者和短期存活者群体中发现的细菌群落存在显著差异。长期存活者表现出相对丰富的假黄色单胞菌(Pseudoxanthomonas)、Saccharropolyspora和链霉菌(Streptomyces)。所有这三个细菌分类群以及克劳氏芽孢杆菌(Bacillus Clausii)的存在预示着这两个队列中患者具有更好治疗结果。
特定的微生物组增强了对肿瘤的免疫攻击
免疫组织化学显示这两个队列中长期存活者的肿瘤具有更大的T细胞密度,包括CD8阳性杀伤性T细胞,这就与之前的研究结果---长期存活者具有更强的免疫反应---相一致。
McAllister及其同事们发现免疫细胞浸润与肿瘤中的微生物组多样性之间存在很强的相关性。进一步的分析表明,T细胞的免疫浸润和活化与长期存活者肿瘤中发现的三种富集的细菌类型有关。
由于肿瘤微生物组与免疫反应之间存在明显的关联性,McAllister及其团队着手寻找改变肿瘤微生物组的方法。
利用肠道微生物组改变肿瘤微生物组
McAllister说道,“不能够直接调节肿瘤微生物组,但是你能够调节肠道微生物组,而且如果肠道微生物组和肿瘤微生物组存在交谈的话,那么你能够间接地改变肿瘤微生物组。”
McAllister团队比较了三名手术患者的肠道、肿瘤和邻近组织中的细菌。他们发现肠道微生物组大约占肿瘤微生物组的25%,但在正常的邻近组织中不存在,这表明肠道中的细菌能够能在胰腺瘤中定植。
这些研究人员将晚期癌症患者的粪便菌群移植到小鼠体内,发现供者微生物组大约占由此产生的肿瘤微生物组的5%,但是整个肿瘤微生物组的70%已被移植的粪便菌群改变。
McAllister说道,“如今我们知道你能够通过FMT完全改变肿瘤微生物组中的细菌组成。”
利用FMT逆转免疫抑制
接下来,他们将来自晚期胰腺癌患者、存活超过5年且无疾病迹象的患者和健康对照者的粪便菌群移植到小鼠体内。
在肿瘤产生五周后,接受来自晚期胰腺癌患者的粪便菌群移植的小鼠具有更大的肿瘤,而接受来自长期存活者的粪便菌群移植的小鼠体内的肿瘤的平均大小减少了70%,接受来自健康对照者的粪便菌群移植的小鼠体内的肿瘤的平均大小减少了50%。
免疫分析显示与其他两组相比,接受来自长期存活者的粪便菌群移植的小鼠具有显著更高的CD8阳性T细胞数量和更大的CD8阳性T细胞活化。接受来自晚期胰腺癌患者的粪便菌群移植的小鼠具有增加的调节性T细胞和髓源性抑制细胞,这两种细胞都抑制免疫反应。
为了评估FMT的作用是否依赖于免疫系统,这些研究人员剔除了一组接受来自长期存活者的粪便菌群移植的小鼠中的T细胞,这完全阻断了FMT的抗肿瘤作用。(生物谷 Bioon.com)
参考资料:
1.Erick Riquelme et al. Tumor Microbiome Diversity and Composition Influence Pancreatic Cancer Outcomes. Cell, 2019, doi:10.1016/j.cell.2019.07.008.
3.Study finds specific microbiome tied to long-term survival of patients with pancreatic cancer
https://medicalxpress.com/news/2019-08-specific-microbiome-tied-long-term-survival.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


