对抗高度耐药型结核病!TB联盟口服新药pretomanid获美国FDA专家委员会推荐批准
来源:本站原创 2019-06-10 14:55
2019年06月10日讯 /生物谷BIOON/ --非盈利药物开发商TB Alliance(结核病联盟)近日宣布,美国食品和药物管理局(FDA)抗菌药物咨询委员会已投票表决(14票赞成,4票反对,0票弃权),认为有大量证据表明,pretomanid作为与贝达喹啉(bedaquiline)和利奈唑胺(linezolid)联合治疗方案的一部分,用于治疗广泛耐药(XDR)或药物不耐受或无反应性多药耐药(

2019年06月10日讯 /生物谷BIOON/ --非盈利药物开发商TB Alliance(结核病联盟)近日宣布,美国食品和药物管理局(FDA)抗菌药物咨询委员会已投票表决(14票赞成,4票反对,0票弃权),认为有大量证据表明,pretomanid作为与贝达喹啉(bedaquiline)和利奈唑胺(linezolid)联合治疗方案的一部分,用于治疗广泛耐药(XDR)或药物不耐受或无反应性多药耐药(MDR)肺结核病成人患者具有充分的有效性和安全性证据。
pretomanid是一种试验性抗结核药物,目前该药的上市申请文件正在接受FDA的优先审查以及欧洲药品管理局(EMA)的审查。pretomanid由TB Alliance开发,作为全口服组合疗法BPaL(由贝达喹啉、pretomanid、利奈唑胺组成)的一部分。
需要指出的是,FDA咨询委员会的投票结果对FDA没有约束力,但FDA会考虑其意见,并将在2019年8月做出最终审查决定。
TB Alliance总裁兼首席执行官Mel Spigelman表示:“FDA咨询委员会投票赞成将pretomanid与贝达喹啉及利奈唑胺联合用于治疗高耐药结核病,我们对此感到鼓舞,我们期待着FDA的最终审查决定。”
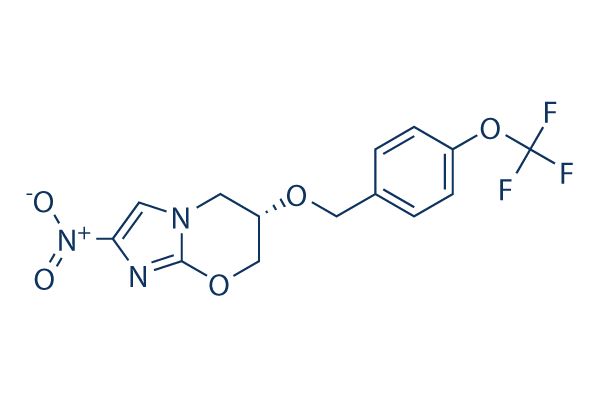
pretomanid分子结构式(图片来源:Wikipedia)
pretomanid是一种新化学实体,属于名为硝基咪唑嗪类化合物。该药已在20项临床试验中单独或与其他抗结核药物联合进行了研究。自从2002年TB Alliance开始开发pretomanid以来,该药已在14个国家对1200多人进行了临床试验。
在III期Nix-TB试验中,首次对BPaL方案进行了临床评估。该研究是一项开放标签、单臂研究,入组的患者为广泛耐药结核(XDR-TB)、药物不耐受或非反应性耐多药结核(MDR-TB)。研究中,患者接受BPaL方案治疗6个月,可以延长至9个月,以期治愈。
根据2018年联合国世界肺部健康会议上提交的前75例受试者的中期结果进行的改良意向治疗分析,89%的受试者结局良好,接受治疗6个月后以及治疗后随访6个月时显示临床感染得到解决、TB痰培养呈阴性。
结核病(tuberculosis)是一种全球性疾病,在每个国家都有发现,是导致死亡的首要传染病。2017年,有1000万人患有活动性结核病,160万人死亡。这是一种可以通过咳嗽或打喷嚏传播的空气传播疾病。耐药结核病例继续增加,2017年报告的耐药结核病例超过50万例,估计有127个国家报告了广泛耐药结核病例。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


