多篇文章聚焦科学家们在胚胎发育研究领域取得的新成果!
来源:本站原创 2020-04-26 21:33
本文中,小编对近期科学家们在胚胎发育研究领域取得的新成果进行整理,分享给大家!图片来源:University of Cambridge【1】Nature:分节时钟的时间延迟同步振荡调节着胚胎发育doi:10.1038/s41586-019-1882-z在一项新的研究中,来自日本京都大学和日本理化研究所的研究人员在小鼠细胞中利用一种新的活体成像(live-im
本文中,小编对近期科学家们在胚胎发育研究领域取得的新成果进行整理,分享给大家!
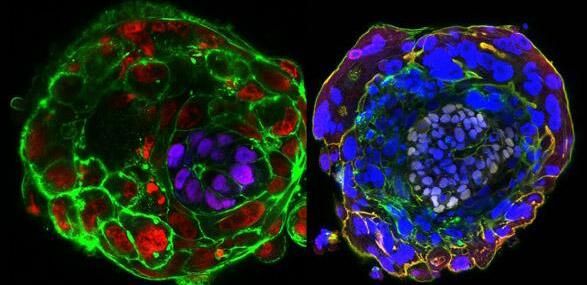
图片来源:University of Cambridge
【1】Nature:分节时钟的时间延迟同步振荡调节着胚胎发育
doi:10.1038/s41586-019-1882-z
在一项新的研究中,来自日本京都大学和日本理化研究所的研究人员在小鼠细胞中利用一种新的活体成像(live-imaging)技术发现一个特定的时钟基因,即Hes7,会在一定的时间延迟内振荡,从而产生脊椎动物中的脊椎骨(vertebrae)、脊柱和枕骨。这一发现揭示了细胞内的通讯在正常发育中如何受到控制和定时,以及涉及哪些化合物,相关研究结果发表在Nature期刊上。
在胚胎发育过程中,将形成神经组织和结缔组织的细胞排列在一起并开始表达相关基因。这个过程有规律地发生,发育生物学家称之为分节时钟(segmentation clock)。由此形成的重复结构沿着身体轴线分布,并产生脊椎骨和肋骨。论文通讯作者、京都大学综合细胞材料科学研究所发育生物学家Ryoichiro Kageyama及其同事们想要了解细胞内的协调动力学。在此之前,人们仅在快照中研究了这一过程,但未使用活体成像。
doi:10.1126/science.aax7890等
原肠胚形成(gastrulation)是发育中的里程碑事件,它涉及早期胚胎发生中出现的一系列复杂的分子、物理和能量重塑转变。不同物种间的这种转变过程各不相同,导致地球上动物形态的多样性。由于技术和伦理上的限制,灵长类动物原肠胚形成的分子和细胞机制尚不清楚。缺乏处于原肠胚形成阶段的灵长类动物胚胎样品限制了科学家们对灵长类动物中这一关键事件的理解。近期,人类胚胎在体外培养了12到13天。许多政府和国际组织建议不要让人类胚胎在体外培养超过14天。因此,有理由期待对非人灵长类动物胚胎模型系统的分析将阐明原肠胚形成机制,并有望阐明人类发育以及早期发育过程中出现的过程异常如何导致发育缺陷和疾病。
猴子长期以来被认为是一种可靠的研究人类生理和病理事件的动物模型,这是因为它们在基因组和形态学特征上与人类高度相似。在两项新的研究中,我国研究人员开发出一种体外培养(in vitro culture, IVC)系统来研究食蟹猴胚胎植入后发育到原肠胚形成阶段和超过原肠胚形成阶段(受精后第9~20天);相关研究结果发表在Science期刊上。文章中,研究人员开发出一种可在受精后长达20天的时间内支持食蟹猴胚胎在体外培养的系统。通过将组织学染色和免疫荧光染色与单细胞RNA测序(RNA-seq)分析相结合,他们发现这些体外培养的猴子胚胎的发育超过了早期的原肠胚形成阶段,并概述了灵长类动物体内胚胎植入后早期发育的关键事件。
【3】Science:中美科学家联合研究揭开灵长类动物胚胎发育的“魔盒”
doi:10.1126/science.aaw5754
目前我们并不清楚灵长类动物早期胚胎发育过程中所发生的分子和细胞事件,如今,来自中国和美国的科学家们通过联合研究开发了一种新方法,能在实验室中研究灵长类动物胚胎的生长过程,同时也能帮助研究人员首次观察到胚胎关键发育过程中的分子细节,相关研究刊登于国际杂志Science上。
这项研究是在非人类的灵长类动物细胞中进行的,其对于人类早期发育的研究也具有重要的意义;能提供早期胚胎发育的信息,并提供关键信息来改善人类再生医学的研究进度。研究者Juan Carlos Izpisua Belmonte说道,我们的研究为揭开胚胎早期发育的黑匣子提供了第一个视角,如今我们就能观察到每一个胚胎发育过程细胞的进展情况以及胚胎发育需要哪些因素。
【4】Nature:华人科学家开发微流体类胚胎模型,助力揭开胚胎发育的秘密
doi:10.1038/s41586-019-1535-2
早期人类胚胎发育包括广泛的谱系多样化、细胞命运分化和组织模式。尽管早期人类胚胎发育具有基础性和临床重要性,但由于种间差异和对人类胚胎样本的可获得性有限,科学家们目前为止仍然不清楚对早期人类胚胎发育的原因。为了揭示其中的秘密,来自密西根大学的华人科学家Jianping Fu和加州大学的研究人员合作,报告了一种人类多能干细胞(hPSCs)体外微流控培养系统,相关研究成果发表在Nature杂志上。
这种系统以一种高度可控和可伸缩的方式,模拟了上胚层和羊膜外胚层部分的发育,包括外胚层的腔内形成和由此产生的前羊膜腔,双极胚胎囊的形成,以及原始生殖细胞和原始条纹细胞的分化。研究人员进一步证明羊膜外胚层样细胞作为一个信号中心,在人乳头状细胞中触发类似于胃泌素的事件。
【5】Cell:长期存在的细胞发育难题终破解!揭示神经嵴细胞在胚胎发育早期清除死亡细胞
doi:10.1016/j.cell.2019.08.001
无论是人类、鱼类还是任何其他类型的脊椎动物,在其一生当中,细胞都会死亡,从而为新细胞腾出空间来进行重要的过程。但是死细胞必须被清除,在胚胎阶段之后,细胞碎片是通过称为巨噬细胞的免疫系统细胞清除的。 然而,处于胚胎阶段的有机体还没有发育出巨噬细胞和免疫系统。它们是随后在有机体的进一步发育过程中产生的。那么在巨噬细胞出现之前,死细胞是如何被清除的呢?这是发育生物学家长期以来提出的一个老问题。 如今,在一项新的研究中,来自美国弗吉尼亚大学的研究人员描述了他们发现的一个过程:神经系统的胚胎细胞-神经嵴细胞-在斑马鱼发育的较早阶段执行死细胞清除任务,相关研究结果发表在Cell期刊上。
通过对活斑马鱼胚胎进行成像,这些研究人员能够观察到迁移性的神经嵴细胞以一种非常类似巨噬细胞的方式发挥功能。这些最终产生周围神经系统并产生多种组织(骨骼、色素细胞、软骨和纤维结缔组织)的神经嵴细胞似乎在物理上接触死细胞,包围它们,随后吸收它们所含的诸如氨基酸之类的化合物,这些化合物接着就可用于构建新的细胞。
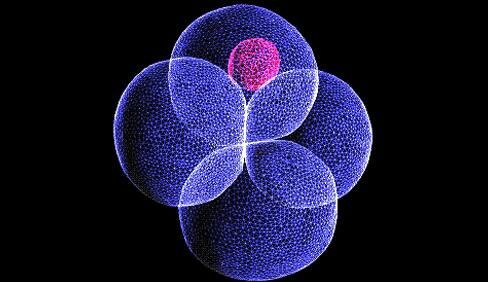
图片来源:University of Cambridge
doi:10.1038/s41586-019-1492-9
来自艾克斯马赛大学和CNRS、Turing生命系统中心、芝加哥大学和法兰西学院的一组研究人员揭示了果蝇胚胎发育过程中细胞内化的一个此前未知的过程。在他们发表在《Nature》杂志上的论文中,该小组描述了他们对果蝇胚胎发育的研究,以及他们从中学到的东西。果蝇是一种常见的果蝇。华威大学(University of Warwick)的Kristen Panfilio在同一期期刊上发表了一篇新闻和观点文章,概述了该团队的工作。
正如Panfilio所指出的,胚胎发育期间会发生一个叫做形态发生的过程,在这个过程中,身体形成了。正如她进一步指出的,在大多数情况下,会发生许多组织重塑。举个例子,在在形态发生的最后时间段,形成肌肉组织的细胞实际上会从早期胚胎的外部移动到更内部的位置。在这项新的研究中,研究人员报告说,他们在果蝇身上发现了这个过程中以前从未见过的一个方面。
【7】Mol Cell:揭秘胚胎发育奥秘!为何发育中胚胎的细胞彼此并不相同?
doi:10.1016/j.molcel.2019.06.038
近日,一项刊登在国际杂志Molecular Cell上的研究报告中,来自纽约大学的科学家们通过研究阐明了在胚胎发育(embryogenesis)过程中细胞变得彼此不同的分子机制,相关研究结果或能帮助阐明胚胎发育的遗传规律,同时也能帮助理解疾病发生和出生缺陷的原因。研究者Stephen Small教授解释道,很多年来科学家们一直知道,在特定细胞中改变基因的开启或会引起出生缺陷的癌症发生,然而其中的分子机制研究者却知之甚少,本文研究结果揭示了在胚胎发生过程中该过程被调节的分子机制。此前研究人员鉴别出了基因启动子(promoters)的存在,然而这些研究并未描述这些启动子是如何被激活的,以及在胚胎发育过程中细胞是如何变得彼此不同的。
这项研究中,研究人员重点对一种名为hunchback (hb,驼背基因)的基因进行研究,该基因能使得果蝇胚胎头部的细胞与腹部细胞不同,如今研究者在名为bh启动子(或遗传开关)的区域中发现了hb基因的DNA序列代码,如果hb启动子的开关被关闭的话,hb基因就会沉默并停止表达,然而一旦其开启表达,基因就会产生RNA副本,其对于指定头部发育至关重要。
【8】Science:我国科学家揭示人类早期胚胎发育中的组蛋白修饰重编程
doi:10.1126/science.aaw5118
在真核生物中,组蛋白与带负电荷的双螺旋DNA组装成核小体。因氨基酸成分和分子量不同,组蛋白主要分成5类:H1,H2A,H2B,H3和H4。除H1外,其他4种组蛋白均分别以二聚体形式相结合,形成核小体核心。DNA便缠绕在核小体的核心上。而H1则与核小体间的DNA结合。组蛋白修饰(histone modification)是指组蛋白在相关酶作用下发生甲基化、乙酰化、磷酸化、腺苷酸化、泛素化、ADP核糖基化等修饰的过程。
组蛋白上发生甲基化的位点是赖氨酸和精氨酸。赖氨酸能够分别发生一、二、三甲基化,精氨酸只能发生一、二甲基化。在组蛋白H3上,共有5个赖氨酸位点可以发生甲基化修饰。一般来说,组蛋白H3K4的甲基化主要聚集在活跃转录的启动子区域。组蛋白H3K9的甲基化与基因的转录抑制及异染色质有关。H3K27甲基化可导致相关基因的沉默,并且与X染色体失活相关。H3K36的甲基化与基因转录激活相关。组蛋白修饰调节基因表达和发育。在一项新的研究中,为了解决在人类早期发育中组蛋白修饰如何发生重编程,清华大学等机构的研究人员研究了人卵母细胞和早期胚胎中的关键组蛋白标记,相关研究结果发表在Science期刊上。
在小鼠卵母细胞中,H3K4me3与H3K27me3都表现出与体细胞不同的非经典分布规律。与小鼠中不同的是,允许性标记H3K4me3在人卵母细胞的启动子中主要表现出经典的分布模式。在受精后,合子基因组激活(zygotic genome activation, ZGA)前的胚胎在富含CpG的调节区域中获得可访问性的染色质和广泛的H3K4me3。相比之下,抑制性标记H3K27me3经历全局性消除。随后,一旦合子基因组激活,富含CpG的调节区域转变为活性或抑制状态,随后在发育基因上恢复H3K27me3。
doi:10.1038/s41586-019-1233-0
最新一项研究表明,卵母细胞受精后立即会出现DNA活性和非活性区域的分化,该现象甚至在基因被激活之前就已经出现。该研究将有助于更好地了解单个受精卵母细胞发育成由许多不同细胞类型组成的完整生物体的机制,相关结果发表在Nature杂志上。
受精卵最终会发育成一个完整的,由数万亿个具有多种功能的细胞组成的有机体。尽管这些细胞具有不同的功能,但所有这些细胞中的DNA都是相同的。细胞的特性由基因组的特定表达谱决定。但其中的决定机制并不清楚。DNA在细胞核中并不是随机分布的,他们在空间上具有活性和非活性区域的区分。不同的区域则由被称为Lamina Associated Domains,或LAD的结构分隔。这导致了染色体的空间异质性的形成,与靠近LAD的部分相比,存在于LAD间的部分更容易被激活。
【10】Science:新研究打破人们对基因如何影响早期胚胎发育的常规理解
doi:10.1126/science.aau0583
我们的身体大约有14万亿个细胞,每个细胞含有一个细胞核,每个细胞核含有长2米宽20个原子的DNA。为了适应每个细胞核,DNA缠绕在特定的蛋白周围。这些缠绕的DNA抑制基因调控蛋白结合到基因组中的蛋白编码片段上,这有助于将细胞不需要的基因保持在“关闭”位置。
到目前为止,人们尚不清楚这种DNA包装如何影响早期胚胎的发育。在一项新的研究中,来自美国宾夕法尼亚大学佩雷尔曼医学院的研究人员发现在小鼠胚胎---受精后仅8天大---中,基因组中的紧凑包装区域在蛋白编码基因上增加了。在这种细胞分化阶段几天后,这些紧密包装的基因组区域松散开来,从而允许某些基因被读取和产生相应的蛋白,相关研究结果发表在Science期刊上。
研究者表示,这意味着我们在对早期胚胎中基因如何受到控制的理解上发生了根本性变化,即便我们迄今为止还不能观察到所有潜在的临床影响。这项研究证实基因活性处于‘关闭状态’在早期的动物发育中起着重要作用。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


