Nature Communications:研究揭示动物中DNA转座子通过两种机制介导基因重复
来源:动物研究所 2021-07-14 20:54
转座子被认为是宿主基因组演化的重要推动力。其类型众多,包含non-LTR(Long Terminal Repeat)型逆转座子、LTR型逆转座子、Helitron型DNA转座子、TIR(Terminal Inverted Repeat)型DNA转座子等,可引起包含基因重复(gene duplication)在内的各种遗传突变。已有研究表明,non-LTR型逆
转座子被认为是宿主基因组演化的重要推动力。其类型众多,包含non-LTR(Long Terminal Repeat)型逆转座子、LTR型逆转座子、Helitron型DNA转座子、TIR(Terminal Inverted Repeat)型DNA转座子等,可引起包含基因重复(gene duplication)在内的各种遗传突变。已有研究表明,non-LTR型逆转座子在人类基因组中介导基因重复,产生大量新基因。2016年,中国科学院院动物研究所研究员张勇研究组研究发现,动物中LTR可借由模板跳转介导基因重复;Helitron在蝙蝠中通过通读(transduction)的形式介导基因重复。迄今,TIR型转座子介导基因重复的能力只在植物中被揭示,其中水稻中的MULE元件捕获大量宿主基因,形成Pack-MULE的嵌合结构。但TIR型转座子介导基因重复形成的机制仍不清楚,动物中此类基因重复也鲜有报道。
7月13日,张勇研究组等在Nature Communications上,在线发表了题为DNA transposons mediate duplications via transposition-independent and -dependent mechanisms in metazoans的研究论文。该研究首次大规模搜索了100个动物基因组,鉴定了TIR转座子介导的基因重复,并将其命名为Pack-TIR。研究发现,大部分基因重复的产生不依赖转座活性,符合缺口填补(gap-filling)模型;在黑腹果蝇群体基因组数据中找到的最年轻的多拷贝基因Ssk-FB4则符合新提出的模板跳转及转座(FoSTeST)模型。蛋白质组、自然选择压力分析及表型关联分析显示Ssk-FB4s编码功能蛋白。上述结果证明TIR转座子可以重塑基因结构,产生新基因。
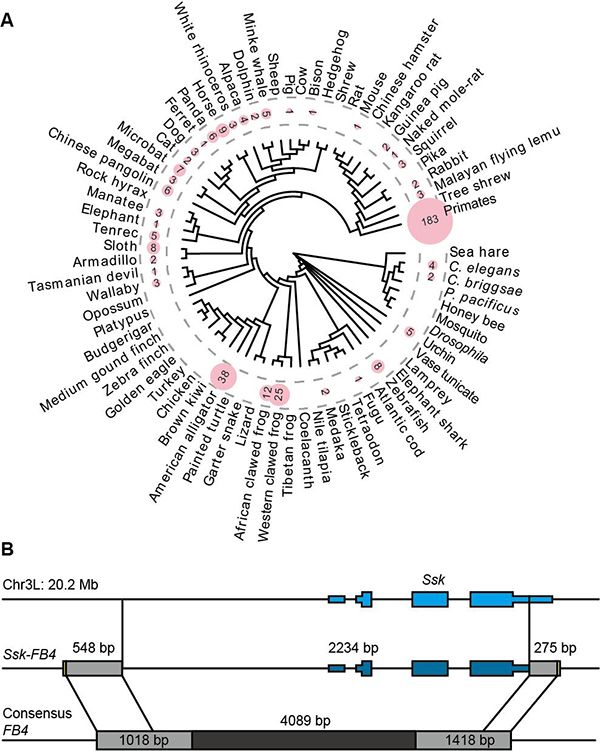
研究中,科研人员收集了公共数据库UCSC中100个后生动物的基因组,计算分析鉴定出370个Pack-TIR元件(图1A)。进而,同时在黑腹果蝇群体中鉴定出一个多拷贝Pack-TIR家族:Ssk-FB4(由FB4 转座子捕获基因Ssk所形成的新基因)。其基因结构和植物中Pack-MULE相似,中间为捕获的外源序列,两侧为TIR转座子序列(图1B)。
研究发现,Pack-TIR与TIR转座子数目成线性正相关(图2A)。对灵长类谱系中Pack-TIR的起源时间分析发现,其零散分布在各演化枝上(图2B)。这些Pack-TIR在各个时间段皆有起源,即使宿主编码的转座子已丧失转座活性。由此推断,大部分Pack-TIR的产生不依赖于转座活性(transposition-independent)。多方面证据表明,Pack-TIR的形成符合缺口填补(gap-filling)模型(图2C):Pack-TIR的丰度与其到母源序列的距离呈负相关,即TIR转座子倾向于捕获临近序列;67.6%事件含有微同源序列(Pack-TIR与母源序列共享较短的相似序列);灵长类物种间的比较分析显示,转座子和外源序列是先后插入的两次独立事件。随后,研究人员发现果蝇中Ssk-FB4其形成过程与缺口填补模型不符,因此提出复制叉停滞-模板跳转-转座(FoSTeST)这一新模型来解释多拷贝Pack-TIR的产生(图2D)。该模型与缺口填补模型不同,模板跳转后转座酶会立即将嵌合的Pack-TIR转座到基因组其它位置,科研人员的策略及发现对植物中Pack-MULE的起源机制研究将具有启发意义。
除机制方面的分析,科研人员还结合转录组数据和进化基因组数据探索Pack-TIRs的功能。研究发现,Pack-TIR倾向于捕获外显子序列,且大部分与所在基因发生融合,具有转录信号(图3A)。Ssk-FB4是罕见的编码功能蛋白的例子,所有拷贝不仅显示出较高的转录和翻译水平(图3B-C),且各拷贝的非同义突变在细胞膜外结构域显着富集,暗示其受到正选择(图3D)。此外,突变机制所赋予的Ssk-FB4嵌合结构使其更容易发挥新功能,可能增加果蝇抵御环境中致病微生物的能力(图3E-F);转座带来的拷贝数增加使自然选择有更多的作用对象,推动了适应性进化更快发生。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


