常凌乾/王杨/钱海生团队开发电微流控生物芯片,实现隐球菌快速裂解和灵敏检测
来源:生物世界 2024-02-10 10:48
该研究开发了一种电微流控生物芯片。该芯片集样本制备和结果定量于一体,实现了“样本进,结果出”的目的。芯片可以在20分钟内检测出隐球菌,并在1小时内达到最大检测限,且能够有效的区分隐球菌的两种亚型。
针对这一需求,北京航空航天大学/安徽医科大学常凌乾联合团队在 Biosensors & Bioelectronics 期刊发表了题为:Rapid Cryptococcus electroporated-lysis and sensitive detection on a miniaturized platform 的研究文章。
该研究开发了一种电微流控生物芯片。该芯片集样本制备和结果定量于一体,实现了“样本进,结果出”的目的。芯片可以在20分钟内检测出隐球菌,并在1小时内达到最大检测限,且能够有效的区分隐球菌的两种亚型。

与其他真菌相比,隐球菌的特征是细胞体周围有一个荚膜(图1a)。隐球菌主要具有两种亚型:新生隐球菌(NEO)和格特隐球菌(GAT),研究人员可以通过它们各自独有的DNA序列进行特异性检测(图1b)。
为了实现快速、准确检测和区分隐球菌亚型的目标,研究团队设计了一种集成的微流控生物芯片。该芯片包含两个区域:用于细胞破裂的电穿孔裂解(EL)区域和用于核酸检测的电化学检测(ED)区域(图1c),它们通过蛇形通道连接。EL区由两个电极组成,每个电极设计有六个矩形区域,彼此之间的距离为100μm(图1d-1f)。在EL区,通过微通道的收缩设计,可以将电场强度集中在收缩区域,实现了电场强度的显著放大,通过注射泵的驱动,液体样本中的隐球菌的荚膜在流经EL区时被快速的电穿孔裂解并释放核酸(图1c)。
随后,溶液会填充满整个ED区(图1c)。研究团队在三电极系统的基础上,在ED区设计了三个独立的电化学检测单元,包括三个工作电极、一个公共参比电极和一个公共对电极(图1c)。AuNPs可以与rGO上的氨基(-NH2)非共价结合,从而可以在工作电极上进行修饰。特异探针通过金-巯基(Au-S)相互作用共价连接到AuNPs层,并在其5'端修饰了亚甲基蓝(MB)分子(图1g)。液体样本中的目标序列与工作电极上修饰的特异探针杂交后,MB分子从电极表面移开,导致电流减小,可以实现对目标序列的定量检测(图1h)。
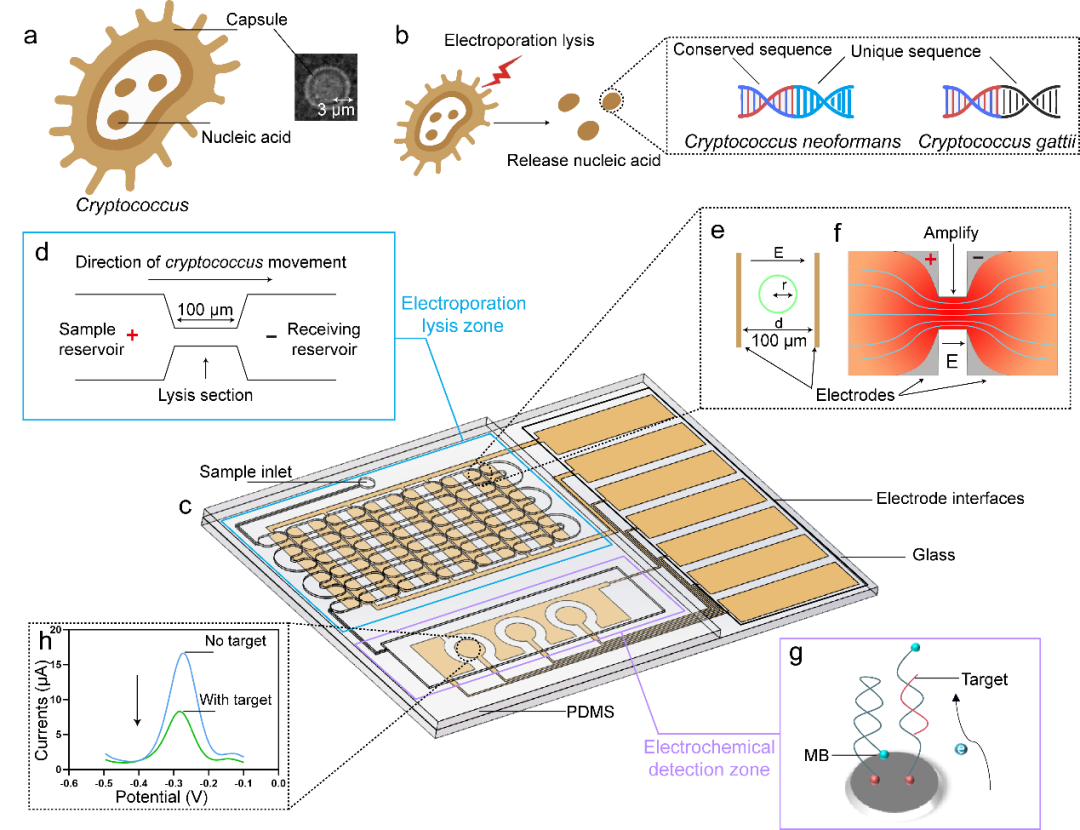
图1. 隐球菌核酸序列的差异及电微流控芯片的工作原理
研究团队通过微分脉冲伏安法(DPV)研究了修饰电极的性能。通过DPV测试,NEO和GAT的检出限分别为60 pg/mL和100 pg/mL。
在临床应用中,对北京世纪坛医院提供的20个随机样本进行隐球菌的检测。将20个样本分为两组,其中一组样本通过芯片进行裂解检测,另一组样本用传统的实验室方法进行裂解以及扩增检测(图2a)。结果表明,该检测平台在较短的时间内获得了与传统方法相同的检测结果,且操作简单,灵敏度达到了100%(图2b),这进一步证明了该平台在隐球菌检测中有着极好的灵敏度和实用性,具有良好的发展前景。此外,整个过程在封闭的环境中进行,避免了对周围环境和操作人员的污染,减轻了人员、时间和地点的负担。该芯片结合了高灵敏、快速的电化学检测、快速的隐球菌电穿孔裂解、核酸提取等技术,集样本制备和结果定量于一体,实现了“样本进,结果出”的目的,这对于资源有限地区的隐球菌病快速、安全的医学诊断来说具有广阔的应用前景。
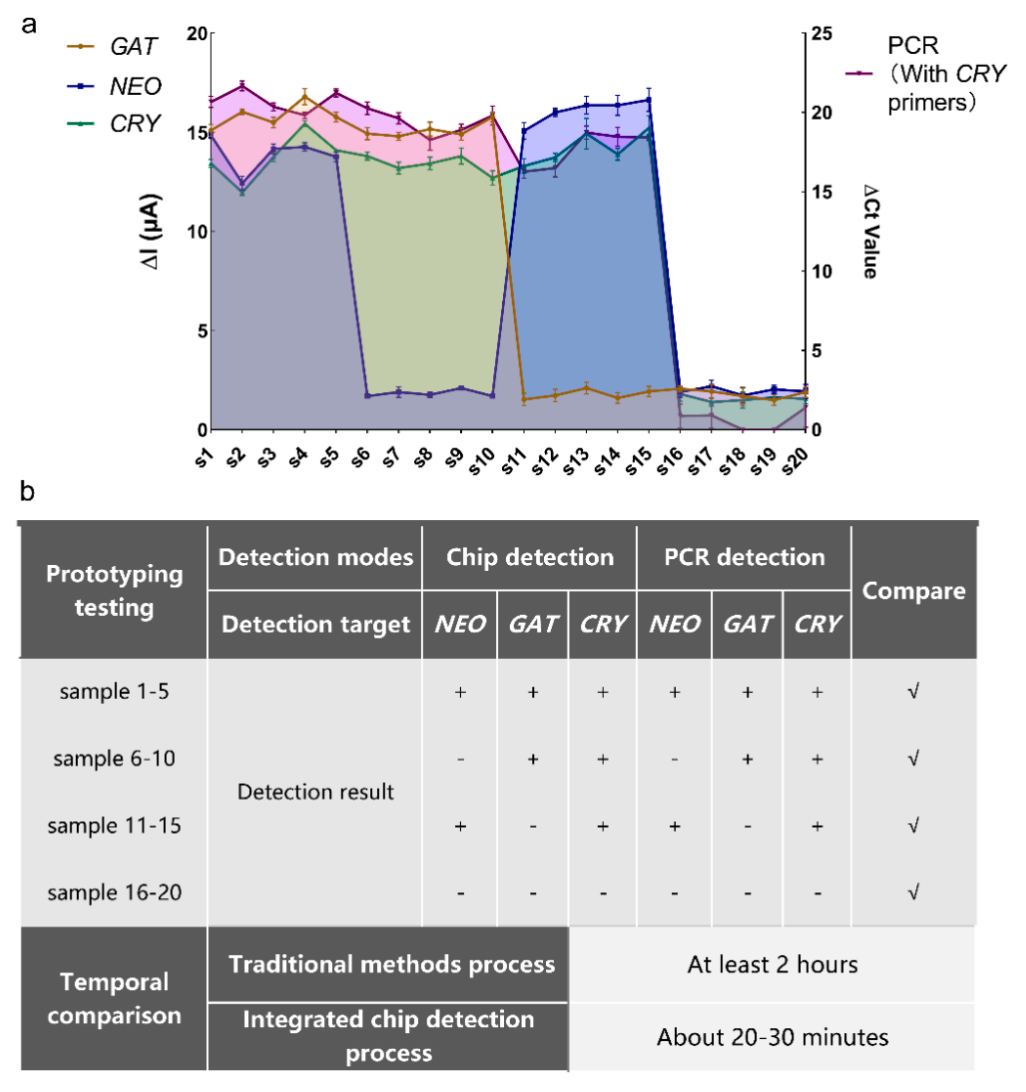
图2. 用实际的样本测试微芯片的性能
该研究的通讯作者为北航生物与医学工程学院常凌乾教授,医学科学与工程学院王杨副教授、董再再助理教授,和安徽医科大学生物医学工程学院钱海生教授。第一作者为安徽医科大学生物医学工程学院的硕士研究生孔祥珠、程龙。安徽医科大学生物医学工程学院为第一作者单位。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


