多篇重要研究成果解读科学家们如何利用人工智能技术来改善多种人类疾病的研究!
来源:生物谷原创 2024-05-29 10:45
新研究利用人工智能破解基因调控密码、一种新型人工智能策略或有望帮助识别新的免疫疗法靶点、科学家成功利用人工智能技术通过“脑肠轴”来改善阿尔兹海默病的疗法
本文中,小编整理了近期多篇重要研究成果,共同解读科学家们如何利用人工智能技术来改善对多种人类疾病的研究,分享给大家!
doi:10.1038/s41586-023-06905-9
有机体由成千上万种不同的蛋白组成,每种蛋白都由特定的基因编码。一种细胞类型要获得其独特的身份、形态和功能,就必须通过“增强子”来激活基因。长期以来,科学家们一直试图破解增强子的运作密码。如今,一篇发表在国际杂志Nature上题为“Targeted design of synthetic enhancers for selected tissues in the Drosophila embryo”的研究报告中,来自奥地利维也纳生物中心分子病理学研究所等机构的科学家们通过研究利用基因组学和人工智能破解了第二种遗传密码,即基因调控的基础密码。
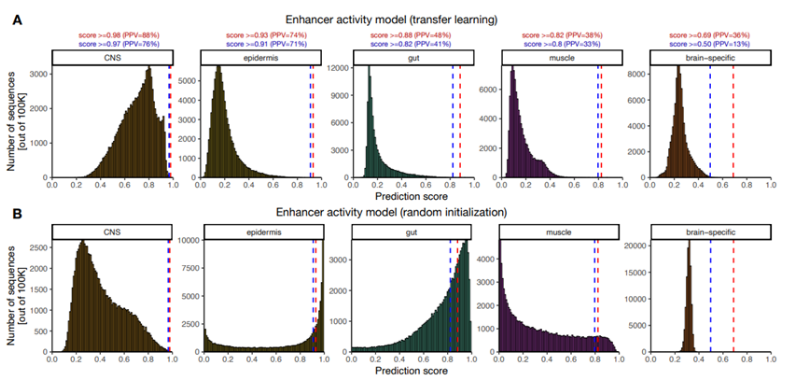
图片来源:Nature, 2023, doi:10.1038/s41586-023-06905-9
复杂有机体的每个健康细胞都含有完全相同的基因组拷贝,其中包括数千个基因,即构建蛋白的蓝图。为了形成不同的细胞类型、组织和器官,需要额外的机制来高精度地开启和关闭特定基因的表达。
作为基因组中的DNA片段,增强子是开启基因的关键因素。Stark实验室把破解将增强子 DNA 序列与它的基因调控功能关联在一起的密码作为自己的使命。虽然第一批增强子是在 20 世纪 80 年代初发现的,但是科学家们只是在过去十年中才开发出通过实验识别增强子的方法。
在此基础上,Stark实验室和合作者如今瞄准了三项任务,它们共同构成了一个似乎不可能实现的长期目标:根据增强子的DNA序列预测它们的活性;预测增强子突变的后果;为特定组织从头设计增强子。换句话说:读取、理解和编写第二种遗传密码。
【2】Brief Bioinform:一种新型人工智能策略或有望帮助识别新的免疫疗法靶点
doi:10.1093/bib/bbad504
能结合I型主要组织相容性复合体(MHC)分子的肽类抗原的免疫识别对于新型免疫疗法的发展和人类健康都是必不可少的,目前预测抗原肽类免疫原性的方法主要依赖于简单的序列的表示,其允许对免疫特征进行一些理解,但对于与肽类识别相关的分子机制的全面考虑仍然不足。
近日,一篇发表在国际杂志Briefings in Bioinformatics上题为“Unsupervised and supervised AI on molecular dynamics simulations reveals complex characteristics of HLA-A2-peptide immunogenicity”的研究报告中,来自克利夫兰诊所等机构的科学家们通过研究开发了一种通过人工智能技术(AI)识别免疫疗法新型靶点的策略。文章中,研究人员开发出了监督和无监督的人工智能技术来揭示肽类抗原的分子特征,肽类抗原是一种免疫细胞用来识别威胁的小块蛋白分子。
研究者Chan说道,在过去,我们关于癌症抗原靶点的所有数据都来自于试验和错误,通过与IBM的研究人员联合研究就能帮助我们突破人工智能和健康科学研究的界限,从而帮助改变我们开发并评估癌症疗法靶点的方式。几十年来,科学家们一直在研究如何更好地识别抗原并利用其来攻击癌细胞和被病毒感染的细胞,然而事实证明,这项任务具有一定的挑战性,因为抗原肽类能根据细胞表面的特定特征与免疫细胞相互作用,而这一过程目前仍未得到很好地理解。研究人员一直受到了影响免疫系统如何识别这些靶点的变量数量的限制,而通过常规计算来识别这些变量是非常困难且耗时的,因为当前的模型是非常有限的,有时或许并不准确。
【3】Cell Rep:科学家成功利用人工智能技术通过“脑肠轴”来改善阿尔兹海默病的疗法
doi:10.1016/j.celrep.2024.114128
肠道微生物代谢产物的改变往往与人类阿尔兹海默病发生直接相关,但感知并对这些代谢产物产生反应的宿主受体,科学家们在很大程度上并不清楚。近日,一篇发表在国际杂志Cell Reports上题为“Systematic characterization of multi-omics landscape between gut microbial metabolites and GPCRome in Alzheimer's disease”的研究报告中,来自克利夫兰诊所等机构的科学家们通过研究利用人工智能技术揭示了肠道微生物组和阿尔兹海默病之间的关联。
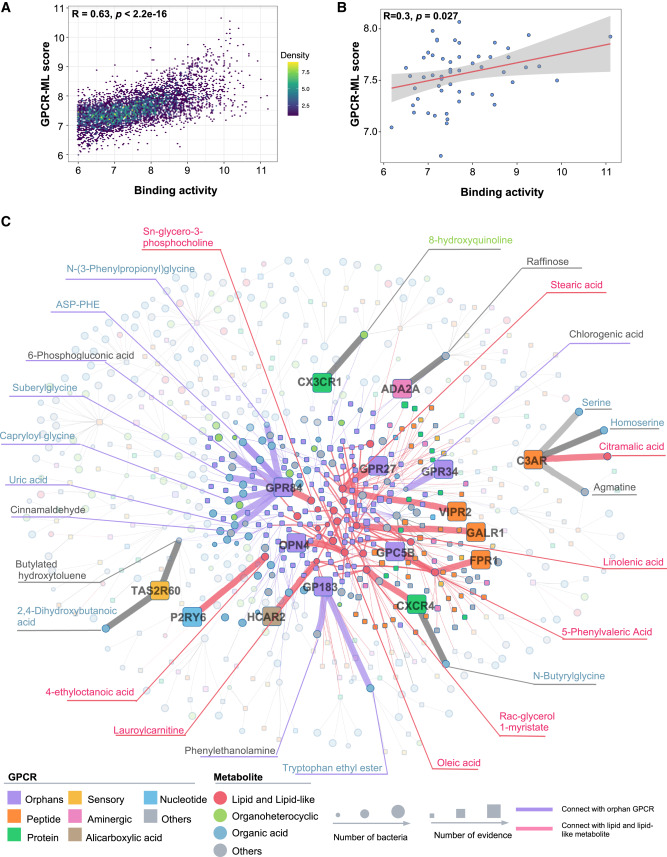
科学家成功利用人工智能技术通过“脑肠轴”来改善阿尔兹海默病的疗法
图片来源:Cell Reports (2024). DOI:10.1016/j.celrep.2024.114128
此前研究结果表明,阿尔兹海默病患者往往会随着疾病进展发生肠道菌群的改变,这项研究中,研究人员提出了一种计算方法来确定细菌的代谢产物如何与细胞上的受体相互作用并促进阿尔兹海默病发生。研究者Feixiong Cheng博士说道,文章中,我们根据代谢产物和受体彼此之间相互作用的可能性,以及其对阿尔兹海默病产生影响的可能性,对其进行了排序,相关数据或许能为研究代谢产物相关疾病提供迄今为止最全面的路线图。
当细菌分解我们所摄入的食物从而获取能量时,它们就会向机体系统释放特定代谢产物,随后,这些代谢产物就会与细胞发生相互作用并对其产生影响,促进对健康有益或有害的细胞过程。除了阿尔兹海默病外,研究人员还将代谢产物与心脏病、不孕症、癌症、自身免疫性疾病和过敏症联系了起来。预防代谢产物和细胞之间的有害相互作用或许有望帮助抵御疾病发生,目前研究人员正在努力研究开发药物来激活或阻断代谢产物与细胞表面的受体进行连接,这种方法的进展较为缓慢,因为研究人员需要大量的信息来识别目标受体。
【4】The Lancet子刊:科学家概述人工智能蓝图如何帮助解决全球范围内的抗生素耐药性问题
doi:10.1016/S2589-7500(23)00221-2
多种人工智能的不断增加为改善人类的医疗保健带来了许多机会,人工智能模型能利用复杂不断变化的数据,从而为人类的行为提供信息,并增强人类的行为,且能从诸如发病率和死亡率等人类健康结果中学习。近日,一篇发表在国际杂志The Lancet Digital Health上题为“Antimicrobial learning systems: an implementation blueprint for artificial intelligence to tackle antimicrobial resistance”的研究报告中,来自利物浦大学等机构的科学家们通过研究概述了一种人工智能框架,其或能改善人类抗生素的使用和感染的护理,并能帮助应对抗生素耐药性的全球挑战。
研究者Alex Howard博士表示,如今不同形式的人工智能常常为改善人类健康护理带来了很多机会,其能利用并学习复杂的数据改善人类健康,抗生素耐药性这一全球公众健康挑战需要大规模地优化抗生素的使用以及进行更为广泛的感染护理,这或许能通过精心构建的人工智能来得以实现。尽管人工智能变得越来越有用和强大,但卫生保健系统在部署人工智能方面仍然存在一定的挑战性,而且在人工智能的承诺与其在患者和人群护理的应用之间往往存在着实施的差距。
考虑到这一点,研究人员在文章中概述了人工智能的适应性实施和维护框架,从而改善抗菌药物的使用和感染护理,并能将其作为一种学习系统;这就考虑到了与抗生素靶向性人工智能开发、评估、维护和可伸缩性相关的抗生素耐药性问题的识别、法律/法规、组织支持和数据处理等。
【5】EJMC:中国科学家利用人工智能技术开发出用于癌症免疫疗法的新型抑制剂
doi:10.1016/j.ejmech.2024.116390
近些年来,以PD-1及其配体PD-L1阻滞为代表的癌症免疫疗法取得了显著的进展,但尽管免疫疗法药物提供了新的治疗可能性,但只有20%至40%的患者对这些疗法能产生反应,大多数患者要么不产生反应,要么会对疗法产生一定的耐受性,如今,科研界正积极探索拓宽肿瘤免疫治疗覆盖面的新路径,以惠及更多患者。
近日,一篇发表在国际杂志European Journal of Medicinal Chemistry上题为“Synthesis and structure-activity optimization of azepane-containing derivatives as PTPN2/PTPN1 inhibitors”的研究报告中,来自中国上海英矽智能科技有限公司等机构的科学家们通过研究利用人工智能(AI)技术开发出了用于癌症免疫治疗的新型PTPN2/N1抑制剂。
研究者表示,其中一种途径就是通过蛋白酪氨酸磷酸酶非受体2型(PTPN2,protein tyrosine phosphatase non-receptor type 2)及其亲密超家族成员PTPN1,其在此前研究中被认为是重要的调节子,主要参与到了免疫细胞信号通路的调节中,进而会通过减弱肿瘤定向性免疫力来促进肿瘤发生,尽管PTPN2/PTPN1抑制剂具有极大的前景,但对其进行开发的过程中,研究人员却面临着巨大挑战,由于其具有较高的阳离子活性位点和蛋白质表面相对较浅的性质,其药代动力学表现一直不太好。
这项研究中,研究人员通过基于结构的药物设计和药物样特性的优化后,发现了双重PTPN2/N1抑制剂ABBV-CLS-484,目前研究人员启动了一项快速跟进的策略计划,旨在设计一种具有药物样特性且能口服吸收的新型PTPN2/N1抑制剂。文章中,研究人员以已知的PTPN2/N1抑制剂结构作为参考化合物整合到Chemistry42(一种利用全新分子设计的产品)中并作为研究起点,同时基于配体药物设计生成了一系列新型PTPN2/N1抑制剂;随后研究人员进一步优化并合成了最有希望的分子,并获得了具有理想ADME特性的候选分子。
【6】Nat Biotechnol:科学家利用人工智能技术开发出了能以较高准确率预测肿瘤杀伤性细胞活性的特殊模型
doi:10.1038/s41587-024-02232-0
开发个体化癌细胞免疫疗法的核心挑战就是识别出肿瘤反应性T细胞受体(TCRs)。近日,一篇发表在国际杂志Nature Biotechnology上题为“Identification of clinically relevant T cell receptors for personalized T cell therapy using combinatorial algorithms”的研究报告中,来自洛桑大学等机构的科学家们通过研究利用人工智能技术开发出了一种强大的预测模型,其或能识别出用于癌症免疫疗法的最具潜能的杀灭癌症的免疫细胞。当与其它算法相结合后,这种预测模型就能应用于个体化的癌症治疗,并根据每位患者机体的肿瘤特殊细胞组成来制定个体化疗法。

科学家利用人工智能技术开发出了能以较高准确率预测肿瘤杀伤性细胞活性的特殊模型
图片来源:Nature Biotechnology (2024). DOI:10.1038/s41587-024-02232-0
研究者Alexandre Harari表示,人工智能在细胞疗法中的应用是一项全新的领域,其或能改变游戏规则,且为患者提供新的临床选择。细胞疗法主要涉及从患者肿瘤中提取免疫细胞,并选择性地对其改造增强器抵御癌症的天然能力,随后在体外大量培养扩增后再将其输注回患者体内发挥作用。T细胞是白细胞或淋巴细胞两种主要类型的细胞之一,其能在血液中循环并巡逻找出病毒感染的细胞或癌变细胞。能穿透实体瘤的T细胞被称为肿瘤浸润性淋巴细胞(TILs,tumor-infiltrating lymphocytes),然而并非所有的TILs都能有效识别并攻击肿瘤细胞。
仅有一小部分的TILs实际上是肿瘤反应性的,大多数都是“旁观者”,研究人员为自己设定的挑战就是识别少数配备能识别肿瘤抗原的T细胞受体的TILs。为了做到这一点,研究人员开发了一种新型AI驱动的预测模型—TRTpred,其能根据肿瘤反应性对T细胞受体进行排名;为了开发TRTpred,研究人员利用从转移性黑色素瘤患者机体中受体的235个T细胞受体进行研究,这些患者已经被分类为肿瘤反应性或非反应型。研究人员将携带每种T细胞受体的T细胞的全局基因表达(转录组)装载到机器学习模型中来识别能区分肿瘤反应性T细胞和非反应型T细胞的模式。
【7】Sci Rep:科学家成功利用人工智能技术发现诱发人类阿尔兹海默病的两种新型遗传突变
doi:10.1038/s41598-023-44378-y
阿尔兹海默病是一种复杂的遗传性疾病,通过全基因组关联性研究所发现的突变只能解释其部分遗传性。近日,一篇发表在国际杂志Scientific Reports上题为“Novel Alzheimer's disease genes and epistasis identified using machine learning GWAS platform”的研究报告中,来自昆士兰大学等机构的科学家们通过研究成功利用人工智能技术进一步揭开了阿尔兹海默病的遗传秘密。
文章中,研究人员利用CSIRO工具VariantSpark和BitEpi来识别出与阿尔兹海默病相关的两个新型遗传突变,同时还发现了或能调节阿尔兹海默病中遗传突变影响的95个新型基因相互作用。识别出这些突变体或能帮助预测人类神经变性疾病的发生、严重性和潜在治疗手段,然而,仅凭识别出的突变体并不能解释阿尔兹海默病和其它神经变性疾病发生的所有遗传性,突变体之间的相互作用(上位效应,Epistasis)常常被认为会促进疾病的发生和进展。
文章中,研究人员表示,一些基因之间的相互作用或能帮助机体抵御阿尔兹海默病,通过利用BitEpi,我们就能识别出这些相互作用并解释阿尔兹海默病遗传性缺失的一些环节;阿尔兹海默病是痴呆症最主要的形式,仅2022年澳大利亚就有超过40万人患有痴呆症,而且随着人口的增长和老龄化的发生,预计到2058年,痴呆症患者的数量将会翻一倍。通过纳入重要的上位效应相互作用,研究人员就要比过去能多捕获10.41%的表型变异。
【8】Lancet 子刊:科学家利用人工智能工具识别出人类5种心力衰竭亚型
doi:10.1016/S2589-7500(23)00065-1
如今机器学习已经被用来分析心力衰竭的亚型,但并没有跨越大型、不同的基于人群的数据集,也没有快约整个病因和表现,或者通过不同的机器学习方法来进行临床和非临床验证。近日,一篇发表在国际杂志The Lancet Digital Health上题为“Identifying subtypes of heart failure from three electronic health record sources with machine learning: an external, prognostic, and genetic validation study”的研究报告中,来自英国伦敦大学学院等机构的科学家们通过研究识别出了五种心力衰竭亚型,其或能被潜在用来预测个体患者未来患病的风险。
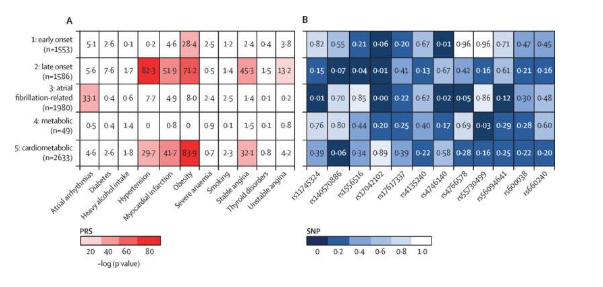
科学家利用人工智能工具识别出人类5种心力衰竭亚型
图片来源:The Lancet Digital Health (2023). DOI:10.1016/S2589-7500(23)00065-1
心力衰竭是一个总称,指的是心脏无法正常向机体周围泵送血液,目前对心力衰竭分类的方法并不能准确预测疾病是如何进展的;这项研究中,研究人员分析了在英国被诊断为心力衰竭的30多万名30岁及以上人群的匿名患者数据,时间跨度达20年之久。利用多种机器学习方法,研究人员识别出了五种心力衰竭亚型,包括早发、晚发、心房颤动相关(心房颤动是一种会导致机体心律不齐的疾病)、代谢型(与肥胖相关但表现为较低的心血管疾病发生率)进而心脏代谢型(与肥胖和心血管疾病有关)。
研究人员发现,不同亚型的患者在确诊后一年内死亡的风险上存在着差异,一年后的全因死亡风险为:早发(20%)、晚发(46%)、心房颤动相关(61%)、代谢型(11%)和心脏代谢型(37%)。随后他们还开发了一种app,临床医生能用来确定心力衰竭患者的亚型,这或许就有望改善对个体未来疾病风险的预测并与患者讨论相关信息。Amitava Banerjee教授说道,我们试图改善对心力衰竭的分类,目的在于更好地理解疾病的可能性过程以及将信息传达给患者。目前,疾病如何发展对于患者而言是很难预测的,有些人的病情很多年都会稳定,而有些人则会很快就恶化。
【9】Nature:新研究表明人工智能在评估超声心动图方面优于人类
doi:10.1038/s41586-023-05947-3
心脏超声检查是全面心脏健康的主要测试。近日,一篇发表在国际杂志Nature上题为“Blinded, randomized trial of sonographer versus AI cardiac function assessment”的研究报告中,来自美国西达赛奈医学中心等机构的科学家们在一项迄今为止进行的最严格的临床试验中发现,人工智能在评估心脏超声方面优于人类。
虽然以前的研究已说明了人工智能模型在读取医疗扫描数据方面的潜在力量,但是在这项新的研究中,这些作者表示这是第一项针对心脏健康的盲目、随机的临床试验。论文共同通讯作者、西达赛奈医学中心心脏病专家David Ouyang说,“围绕人工智能有很多兴奋点”,但严格的评估仍然至关重要。Ouyang补充说,这项成功的临床试验“确实加强了这样一个论点,即我们现在已经为黄金时段做好了准备”。
心脏超声检查,也被称为超声心动图(echocardiogram),是由超声技师对患者进行的,他们通常在将扫描结果交给心脏病专家之前对其进行初步评估。心脏超声检查是衡量心脏功能如何的主要方法。它被用来判断患者是否有心脏病发作,或者患者是否能够接受诸如植入除颤器之类的治疗。
这项新的研究让人工智能模型与超声技师对决,看谁能给出最准确的初步评估。双方都对所谓的左心室射血分数(left ventricular ejection fraction)进行了超声评估,而左心室射血分数衡量的是心脏在心跳期间向身体泵血的能力。在这项研究中,近3500张超声心动图在超声技师和人工智能模型之间被随机分配。随后,双方的评估结果由心脏病专家评估,这些专家不知道哪些评估结果来自超声技师,哪些来自人工智能模型。
【10】Science子刊:利用人工智预测癌症对免疫检查点抑制剂的反应性
doi:10.1126/sciadv.adj0785
近日,一篇发表在国际杂志Science Advances上题为“Cell-cell communication network-based interpretable machine learning predicts cancer patient response to immune checkpoint inhibitors”的研究报告中,来自韩国浦项科技大学和ImmunoBiome公司的研究人员通过研究介绍了一种利用经过细胞间通信网络训练的人工智能(AI)预测癌症对免疫疗法的药物反应性。
当免疫细胞不能正确识别癌细胞和正常细胞时,就会出现自身免疫紊乱。免疫检查点是一种防御机制,可防止人体自身组织受到攻击。然而,癌细胞往往利用这些免疫检查点来躲避免疫细胞的攻击,因此免疫检查点抑制剂(immune checkpoint inhibitor, ICI)在癌症治疗中大受欢迎。鉴于遗传和环境因素的固有差异性以及患者肿瘤特征的多样性,只有不到三分之一的患者对单一 ICI 有反应。预测患者的反应对于制定高效的癌症治疗方案和为无应答患者制定新策略不可或缺。
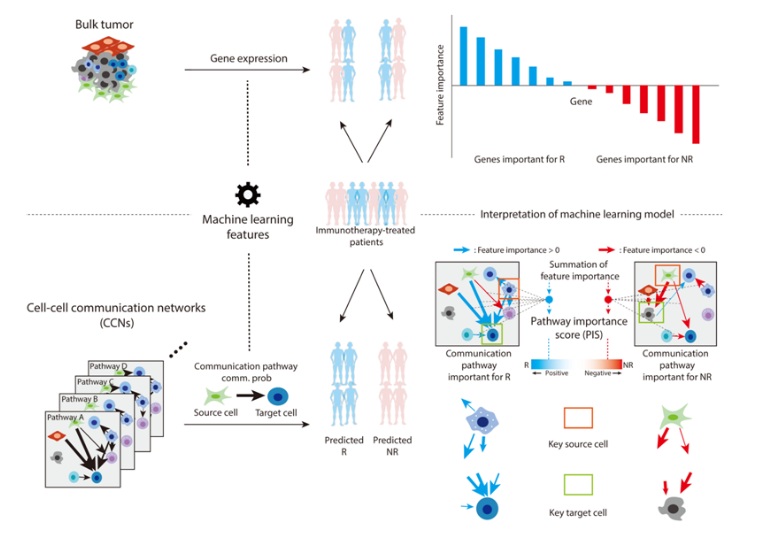
图片来源:Science Advances, 2024, doi:10.1126/sciadv.adj0785
此前,这些作者在2022年建立了一种人工智能模型,通过训练细胞内的蛋白相互作用来预测免疫癌症疗法的疗效。在这项新的研究中,他们更进一步。他们训练人工智能学习细胞外的细胞通信网络。这种先进的人工智能通过分析癌细胞和免疫细胞之间的网络,让人联想到人们通过社交媒体进行交流,从而预测患者对 ICI的反应。这种新的模型在分析来自700名患有黑色素瘤、胃癌、肺癌和膀胱癌之一的患者样本时表现出很高的准确性。此外,它还成功地识别了与对 ICI的反应性和抵抗性有关的关键通信途径,并精确定位了负责这些相互作用的细胞。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


