针对新冠病毒SARS-CoV-2/COVID-19,Science期刊研究进展一览(第6期)
来源:本站原创 2020-11-30 23:34
2020年11月30日讯/生物谷BIOON/---自2019年12月8日以来,中国湖北省武汉市报告了几例病因不明的肺炎。大多数患者在当地的华南海鲜批发市场工作或附近居住。在这种肺炎的早期阶段,严重的急性呼吸道感染症状出现了,一些患者迅速发展为急性呼吸窘迫综合征 (acute respiratory distress syndrome, ARDS)、急性呼吸衰竭
2020年11月30日讯/生物谷BIOON/---自2019年12月8日以来,中国湖北省武汉市报告了几例病因不明的肺炎。大多数患者在当地的华南海鲜批发市场工作或附近居住。在这种肺炎的早期阶段,严重的急性呼吸道感染症状出现了,一些患者迅速发展为急性呼吸窘迫综合征 (acute respiratory distress syndrome, ARDS)、急性呼吸衰竭和其他的严重并发症。2020年1月7日,中国疾病预防控制中心(China CDC)从患者的咽拭子样本中鉴定出一种新型冠状病毒,最初被世界卫生组织(WHO)命名为2019-nCoV。大多数2019-nCoV肺炎患者的 症状较轻,预后良好。到目前为止,一些患者已经出现严重的肺炎,肺水肿,ARDS或多器官功能衰竭和死亡。
2020年2月11日,世卫组织将这种疾病病重命名为2019年冠状病毒病(COVID-19)。同一天,负责分类和命名病毒的的国际病毒分类学委员会的冠状病毒研究小组在bioRxiv上发表了一篇文章,指出该研究小组已经决定,新型冠状病毒2019-nCoV是导致2002-2003年爆发严 重急性呼吸综合征(SARS)冠状病毒(SARS-CoV)的变种。因此,将这种新病原体重新命名为严重急性呼吸综合征冠状病毒2号(severe acute respiratory syndrome coronavirus 2),或SARS-CoV-2。值得注意的一点是,尽管国际病毒分类委员会冠状病毒研究小组将 病毒命名为SARS-CoV-2,但该研究小组主席John Ziebuhr认为这个名字(SARS-CoV-2)和SARS(严重急性呼吸综合征,也称非典型肺炎)没有关联。不过,这种病毒的重新命名引起了不少争议。据《科学》网站报道,世界卫生组织不满意SARS-CoV-2这个名字,而且不打 算采用此名称。
冠状病毒可引起多种动物的多系统感染。在此之前已有6种冠状病毒可以感染人类,它们主要引起人类的呼吸道感染:两种高度致命性的冠状病毒,即严重急性呼吸道综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV);4种可导致温 和的上呼吸道疾病的冠状病毒,即HCoV-OC43、HCoV-229E、HCoV-NL63和HCoV-HKU1。
基于此次疫情给中国和全世界带来严重的危害,小编针对Nature期刊上发表的2019-nCoV/COVID-19研究进行一番梳理,以飨读者。
1.Science论文解读!湖南省年初的新冠病毒传播存在大量的异质性,隔离措施成功阻断该地区的病毒传播
doi:10.1126/science.abe2424
在一项新的研究中,来自中国复旦大学、湖南省疾病预防控制中心、美国国家卫生研究院和印第安纳大学公共卫生学院等研究机构的研究人员基于通过广泛的监测和接触者追踪工作收集的细化流行病学信息,重建了截至2020年4月3日湖南省所有已确认的SARS-CoV-2感染者之间的传播链。相关研究结果于2020年11月24日在线发表在Science期刊上,论文标题为“Transmission heterogeneities, kinetics, and controllability of SARS-CoV-2”。论文通讯作者为复旦大学公共卫生学院的余宏杰(Hongjie Yu)教授和美国国家卫生研究院的Kaiyuan Sun博士。
这些作者确定了驱动传播异质性的人口、临床和行为因素,并评估了干预措施如何调节传播网络的拓扑结构。此外,他们重建了SARS-CoV-2在典型感染过程中的感染谱(infectiousness profile),并估计了通过基于个体和人群的干预措施控制疫情的可行性。
根据中国湖南患者和接触者的详细追踪数据,这些作者发现80%的继发感染可追溯到15%的SARS-CoV-2原发感染,这表明存在大量的传播异质性。传播风险与接触时间和社会互动的密切程度呈正相关,并受到人口统计学和临床因素的调节。封锁增加了家庭和家庭中的传播风险,而隔离减少了所有类型接触者的风险。针对典型SARS-CoV-2患者重建的感染谱在症状出现前达到峰值。建模结果表明,由于这种病毒的特定传播动力学,控制SARS-CoV-2疫情需要病例隔离、接触者隔离和人群水平干预措施的协同作用。
总的来说,这些作者发现病例隔离成功地阻断了湖南地区密切接触者的传播,估计有4.3%的传播发生在SARS-CoV-2患者被隔离后。在这种情况下,所有SARS-CoV-2感染者无论临床严重程度如何都在专门的医院进行医学隔离管理,而接触者则在指定的医学观察中心进行隔离。然而,在家中进行自我隔离可能并不那么有效,预计继续传播的比例应该更高。
2.Science详解:失之桑榆,收之东隅!常见的刺突蛋白突变D614G让新冠病毒高效复制,更快传播,但同时也可能让它对疫苗更加敏感
doi:10.1126/science.abe8499
在一项新的研究中,来自美国北卡罗来纳大学教堂山分校、威斯康星大学麦迪逊分校、日本国立传染病研究所和东京大学的研究人员证实冠状病毒SARS-CoV-2发生的一种称为D614G的突变使得这种病毒能够在世界范围内迅速传播,但是这种发生在刺突蛋白(S蛋白)上的突变也可能使得这种病毒对疫苗更加敏感。相关研究结果于2020年11月12日在线发表在Science期刊上,论文标题为“SARS-CoV-2 D614G variant exhibits efficient replication ex vivo and transmission in vivo”。
这种发生D614G突变的SARS-CoV-2毒株(下称D614G毒株)出现在欧洲,并已成为世界上最常见的毒株。这项研究显示,D614G毒株的复制速度更快,比最初在中国扩散的SARS-CoV-2毒株更具传播性。这些研究结果中也有亮点:虽然D614G毒株传播速度更快,但在动物研究中,它与更严重的疾病无关,而且该毒株对抗体药物的中和作用略微更加敏感。因此,这项研究提供了一些关于SARS-CoV-2如何进化的首批具体发现。
3.Science:新研究估计肯尼亚的新冠病毒抗体总体血清阳性率为4.3%
doi:10.1126/science.abe1916
在一项新的研究中,来自肯尼亚和英国的研究人员通过分析肯尼亚各地献血者的血液样本,估计到2020年6月,肯尼亚4.3%的人携带针对SARS-CoV-2冠状病毒的抗体,当时曾预计肯尼亚会有很多人死于COVID-19,但实际并没有出现如此大规模的死亡。相关研究结果于2020年11月11日在线发表在Science期刊上,论文标题为“Seroprevalence of anti–SARS-CoV-2 IgG antibodies in Kenyan blood donors”。
这些作者说,这表明SARS-CoV-2暴露情况比肯尼亚基于病例的监测所显示的更为广泛。他们的结果将有助于指导该地区的大流行病应对,在该地区,封锁的经济影响---包括它破坏了妇女和儿童的常规医疗护理的方式---已被证明是特别严重的。
4.Science:新研究表明新冠病毒可在水貂和人类之间双向传播
doi:10.1126/science.abe5901
在一项新的研究中,来自荷兰鹿特丹大学医学院等多家研究机构的研究人员对荷兰16个水貂养殖场爆发疫情的SARS-CoV-2冠状病毒的全基因组测序显示,这种病毒在人与水貂之间以及水貂与人之间传播。相关研究结果于2020年11月10日在线发表在Science期刊上,论文标题为“Transmission of SARS-CoV-2 on mink farms between humans and mink and back to humans”。
这些作者说,这种病毒最初是从人类传入的,此后又不断进化。他们写道,“在水貂和其他鼬科动物物种中进行更多的研究对于了解这些物种是否有可能成为SARS-CoV-2的储存库非常重要。”
5.Science:此前已经存在的抗体有助于保护儿童免受新冠病毒感染
doi:10.1126/science.abe1107
弗朗西斯·克里克研究所和伦敦大学学院的研究人员发现,在普通感冒冠状病毒感染期间由免疫系统产生的某些抗体也可以靶向SARS-CoV-2,并可能针对新病毒株赋予一定程度的保护。相关研究结果发表在《Science》杂志上。
对病毒感染作出反应后,免疫系统会产生抗体来对抗病毒。这些抗体在感染后会在血液中保留一段时间,如果再次感染,它们可以再次抵抗病毒。 在这项研究中,科学家们发现,尽管从未感染过这种病毒,但某些人,尤其是儿童,其血液中的抗体对SARS-CoV-2有反应。这些抗体可能是暴露于其他冠状病毒的结果,这些冠状病毒会引起普通感冒,并且与SARS-CoV-2具有结构相似性。
研究人员在开发针对COVID-19的高度敏感的抗体测试时发现了这一发现。为了了解他们的化验测试效果如何,他们将COVID-19患者的血液与未患该疾病的患者进行了比较。令人惊讶的是,他们发现一些未暴露于SARS-CoV-2的人血液中含有可识别该病毒的抗体。为了证实他们的发现,他们分析了2011年至2018年大流行之前收集的300多个血液样本。结果表明,几乎所有样品都具有与普通感冒冠状病毒反应的抗体。但是,一小部分成年供体(约十分之一)也具有与SARS-CoV-2交叉反应的抗体。值得注意的是,这种交叉反应性抗体在6至16岁儿童的血液样本中发现的频率更高。
6.Science:美洲驼纳米抗体有望成为对抗新冠病毒的强大武器
doi:10.1126/science.abe4747
在一项新的研究中,来自美国匹兹堡大学的研究人员描述了一种从美洲驼(llama)身上提取小型的但极其强大的SARS-CoV-2抗体片段的新方法,这种抗体片段可以被制成可吸入的治疗剂,具有预防和治疗COVID-19的潜力。相关研究结果于2020年11月5日在线发表在Science期刊上,论文标题为“Versatile and multivalent nanobodies efficiently neutralize SARS-CoV-2”。
这些特殊的称为“纳米抗体(nanobody)”的美洲驼抗体比人类抗体小得多,在中和SARS-CoV-2病毒方面的效果要好很多倍。它们也更稳定。论文共同通讯作者、匹兹堡大学细胞生物学助理教授Yi Shi博士说,“大自然是我们最好的发明家。我们开发的技术以前所未有的规模调查中和SARS-CoV-2的纳米抗体,这使得我们能够迅速发现数千种具有无与伦比的亲和力和特异性的纳米抗体。”
7.Science:从头设计的蛋白诱饵在体外阻断新冠病毒感染,在体内保护仓鼠免受感染
doi:10.1126/science.abe0075
Neoleukin医疗公司(Neoleukin Therapeutics, Inc.,下称Neoleukin公司)是一家利用复杂的计算方法从头设计蛋白药物的生物制药公司。如今,在一项新的研究中,Neoleukin公司描述了旨在治疗或预防SARS-CoV-2感染的新分子。相关研究结果于2020年11月5日在线发表在Science期刊上,论文标题为“De novo design of potent and resilient hACE2 decoys to neutralize SARS-CoV-2”。
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。这项研究详细介绍了从头设计的蛋白诱饵(protein decoy)的过程,这些蛋白诱饵高亲和力地结合SARS-CoV-2刺突蛋白(S蛋白),从而阻止S蛋白与病毒受体hACE2结合,而这种受体是SARS-CoV-2感染人体细胞所必需的。
据报道,这些经过优化的高稳定性蛋白诱饵与这种病毒结合,从而阻止它进入宿主细胞。先导分子NL-CVX1(CTC-445.2d)被证明可以防止多种人类细胞系遭受SARS-CoV-2感染,并保护仓鼠免受这种病毒感染后出现的严重后果。预防性鼻内给送这些蛋白诱饵可让所有接受致命剂量SARS-CoV-2挑战的仓鼠存活下来。
8.Science:揭示超强效的合成纳米抗体中和新冠病毒机制
doi:10.1126/science.abe3255
在一项新的研究中,来自美国加州大学旧金山分校等研究机构的研究人员通过筛选酵母表面展示文库(含有大于2×109种合成纳米抗体序列)中与S蛋白胞外结构域(ectodomain)结合的纳米抗体序列,分离出中和SARS-CoV-2的单域抗体(纳米抗体)。
这些作者利用SARS-CoV-2 S蛋白的一种突变形式(SpikeS2P)作为抗原。SpikeS2P缺乏S1和S2结构域之间的两个蛋白切割位点之一,并引入两个突变和一个三聚化结构域(trimerization domain)来稳定S蛋白的融合前构象。他们用生物素或用荧光染料标记SpikeS2P,并通过多轮筛选---先是通过磁珠结合随后通过荧光活化细胞分选---来选择展示纳米体的酵母。相关研究结果近期发表在Science期刊上,论文标题为“An ultrapotent synthetic nanobody neutralizes SARS-CoV-2 by stabilizing inactive Spike ”。
三轮筛选产生了21个独特的结合SpikeS2P的纳米抗体,而且ACE2胞外结构域(ACE2-Fc)的二聚体构造体可降低这种结合。这些纳米抗体分为两类。第I类纳米抗体结合RBD并直接与ACE2-Fc竞争(图1B)。这一类的典型例子是纳米抗体Nb6,它可与SpikeS2P和RBD单独结合,结合常数KD分别为210nM和41nM。第II类纳米抗体,以纳米抗体Nb3为例,它结合SpikeS2P (KD=61nM),但不显示与RBD单独结合。在存在过量ACE2-Fc的情况下,Nb6和其他I类纳米抗体的结合完全被阻断,而Nb3和其他II类纳米抗体的结合则适度下降。这些结果表明,I类纳米抗体以RBD为靶点阻断ACE2结合,而II类纳米抗体以其他表位为靶点。事实上,表面等离子共振(SPR)实验表明I类和II类纳米抗体可以同时结合SpikeS2P。
9.Science:大多数人对SARS-CoV-2产生强劲的抗体反应,而且这种抗体反应至少在5个月内保持相对稳定
doi:10.1126/science.abd7728
在一项新的研究中,来自美国西奈山伊坎医学院的研究人员发现绝大多数感染轻度到中度COVID-19的人都会产生强大的抗体反应,这种抗体反应至少在5个月内保持相对稳定。此外,他们还发现这种抗体反应与人体中和(或者说杀灭)SARS-CoV-2(导致COVID-19疾病的冠状病毒)的能力相关。相关研究结果于2020年10月28日在线发表在Science期刊上,论文标题为“Robust neutralizing antibodies to SARS-CoV-2 infection persist for months”。
论文共同通讯作者、西奈山伊坎医学院疫苗学教授Florian Krammer博士说,“虽然有些报告说针对这种病毒的抗体很快就会消失,但是我们发现恰恰相反:90%以上轻度或中度患病的人都会产生足以中和这种病毒的抗体反应,而且这种抗体反应会维持多个月。发现针对SARS-CoV-2的抗体反应的稳健性,包括它的持久性和中和作用,对于让我们能够有效地监测社区的血清阳性率并确定保护我们免受再感染的抗体的持续时间和水平至关重要。这对有效的疫苗开发至关重要。”
10.Science:重大突破!蛋白Neuropilin-1是SARS-CoV-2感染的宿主因子
doi:10.1126/science.abd3072
在一项新的研究中,来自英国布里斯托大学和澳大利亚昆士兰大学等研究机构的研究人员取得一项重大突破:他们可能发现了SARS-CoV-2冠状病毒具有高度传染性并能在人体细胞中迅速传播的原因。这些发现描述了SARS-CoV-2感染人体细胞的能力是如何通过抑制剂阻断一种新发现的病毒与宿主相互作用来降低的,这有助人们开发出一种潜在的抗病毒治疗方法。相关研究结果于2020年10月20日在线发表在Science期刊上,论文标题为“Neuropilin-1 is a host factor for SARS-CoV-2 infection”。与可引起普通感冒和轻度呼吸道症状的其他冠状病毒的不同的是,作为导致COVID-19疾病的病原体,SARS-CoV-2具有很强的传染性和传播性。在此之前,关于SARS-CoV-2为什么容易感染呼吸系统以外的大脑和心脏等器官的主要问题仍未得到解答。
在这项突破性的研究中,布里斯托大学生命科学学院的Peter Cullen教授、Yohei Yamauchi博士、Boris Simonetti博士和James Daly博士及其合作者们利用多种方法发现SARS-CoV-2能识别人体细胞表面上的一种名为神经纤毛蛋白1(neuropilin-1, NRP1)的蛋白,以促进病毒感染。
Yamauchi、Simonetti和Cullen解释道,“在研究SARS-CoV-2刺突蛋白的序列时,我们被一个小的氨基酸序列所震惊,这个序列似乎模仿了在人类蛋白中发现的与NRP1相互作用的蛋白序列。这使得使我们提出了一个简单的假设:SARS-CoV-2的刺突蛋白是否能与NRP1结合以帮助这种病毒感染人类细胞?令人兴奋的是,在应用一系列结构和生化方法时,我们能够确定SARS-CoV-2的刺突蛋白确实与NRP1结合。一旦我们确定这种刺突蛋白与NRP1结合,我们就能够证实这种相互作用可增强SARS-CoV-2对体外培养的人体细胞的入侵。重要的是,通过使用单克隆抗体(简称单抗)--实验室构建的类似于天然抗体的蛋白---或一种阻断这种相互作用的选择性药物,我们能够降低SARS-CoV-2感染人体细胞的能力。这凸显我们的发现在对抗COVID-19方面的潜在治疗价值。”
11.Science:重大突破!蛋白Neuropilin-1促进新冠病毒进入和感染人体细胞
doi:10.1126/science.abd2985
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。众所周知,SARS-CoV-2是通过受体ACE2感染宿主细胞的。在一项新的研究中,来自德国神经退行性疾病研究中心、慕尼黑工业大学、哥廷根大学医学中心和芬兰赫尔辛基大学等研究机构的研究人员发现神经纤毛蛋白1(neuropilin-1, NRP1)是一种可以促进SARS-CoV-2进入细胞内部的因子。NRP1定位于呼吸道和嗅觉上皮,这可能是一个重要的战略定位,但却有助于SARS-CoV-2的感染和传播。相关研究结果于2020年10月20日在线发表在Science期刊上,论文标题为“Neuropilin-1 facilitates SARS-CoV-2 cell entry and infectivity”。论文通讯作者为慕尼黑工业大学的Mikael Simons和赫尔辛基大学的Giuseppe Balistreri。
利用实验室培养的细胞、模拟SARS-CoV-2的人工病毒以及天然存在的病毒进行的实验表明,在ACE2存在的情况下,NRP1能够促进病毒感染。通过用抗体特异性阻断NRP1,这种病毒感染可被抑制。Simons解释说,“如果你把ACE2看作是进入细胞的一扇门,那么NRP1可能是引导这种病毒进入这扇门的一个因素。ACE2在大多数细胞中的表达水平很低。因此,这种病毒不容易找到进入细胞的门。诸如NRP1之类的其他因素可能是帮助这种病毒进入细胞的必要因素。”
12.Science:从结构上分析候选新冠疫苗NVAX-CoV2373中的全长刺突蛋白
doi:10.1126/science.abe1502
在一项新的研究中,来自美国斯克利普斯研究所的研究人员描述了一种先进的候选SARS-CoV-2 S疫苗(NVAX-CoV2373)的结构,这种候选疫苗是基于包括跨膜结构域(TM)和胞质尾区(cytoplasmic tail, CT)的全长S蛋白(氨基酸残基1~1273)开发的。相关研究结果近期发表在Science期刊上,论文标题为“Structural analysis of full-length SARS-CoV-2 spike protein from an advanced vaccine candidate”。
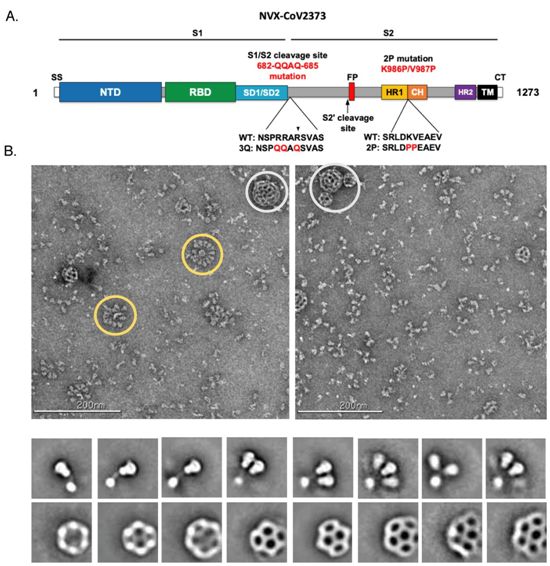
作为这种候选疫苗中的最终构建体,SARS-CoV-2-3Q-2P也在S1/S2多碱性切割位点(polybasic cleavage site,即含有多个精氨酸残基的切割位点,其中精氨酸是碱性氨基酸)上进行修饰,使之从原先的RRAR突变为QQAQ,从而使得它具有蛋白酶抗性,与此同时在S2融合核心的K986和V987残基处进行2个脯氨酸替换以增强它的稳定性,从而产生SARS-CoV-2 3Q-2P-FL蛋白。
从昆虫细胞中表达和纯化的3Q-2P-FL蛋白,在0.01%(v/v)聚山梨酯80(PS 80)洗涤剂中配制。为了表征3Q-2P-FL免疫原的结构完整性,这些研究人员在Matrix-M佐剂存在的情况下,对在PS 80下重建的3Q-2P-FL进行了阴性染色电镜成像,从而再现了正在人类中测试的疫苗配方。这种成像显示这种三聚体3Q-2P-FL蛋白以游离三聚体或多三聚体玫瑰花结(multi-trimer rosette)的形式存在,后者含有多达14个三聚体而且它们的跨膜结构域封闭在PS 80洗涤剂的胶束核(micellar core)中。NVAX-CoV2373纳米颗粒疫苗配方中的3Q-2P-FL蛋白紧密簇聚可能导致比单独的可溶性三聚体更强的免疫反应,这一点类似于其他的病毒糖蛋白免疫原(流感病毒的HA蛋白和RSV病毒的 F蛋白)。
13.Science:全球200名科学家们通力合作揭示SARS-CoV-2、SARS-CoV-1和MERS-CoV冠状病毒的共同弱点
doi:10.1126/science.abe9403
近日,一项刊登在国际杂志Science上的研究报告中,来自乔治亚州立大学等机构的科学家们通过研究发现,三种致命的冠状病毒:SARS-CoV-2、SARS-CoV-1和MERS-CoV都有共同的弱点,比如会频繁劫持细胞中的信号通路,这或许有望帮助研究人员寻找有效广泛抑制冠状病毒感染的潜在靶点和疗法。
在过去20年里,全球面临着三种致命性的冠状病毒,即SARS-CoV-2、SARS-CoV-1和MERS-CoV,而SARS-CoV-2所诱发的COVID-19在全球引起了疾病的大流行,目前在全球已经感染了3700多万人,而且造成了100多万人死亡。这项研究中,研究人员通过研究确认了冠状病毒之间的共性,并解释了多个共同的细胞过程和蛋白靶点,其或能作为新型靶点帮助开发当前和未来冠状病毒感染大流行的治疗性和干预性措施。
这项研究是由来自6个国家14个领先的研究机构中将近200名科学家们合作完成的;此前研究中,研究人员识别了超过300个能与SARS-CoV-2蛋白相互作用的宿主蛋白,这项研究中,研究人员想进一步研究筛选出拥有能改变病毒生长能力的特殊宿主蛋白。研究者Christopher Basler说道,我们至少发现了20个宿主基因所编码的蛋白产物能明显改变感染的宿主细胞产生病毒的水平,这些蛋白质或许就能作为开发治疗性干预措施的潜在靶点,比如,如果某一种细胞蛋白是病毒有效生长所需要的,那么抑制细胞中特殊蛋白的药物或能减缓病毒的感染过程。
14.Science:揭示抗体混合物REGN-COV2有望预防和治疗新冠肺炎
doi:10.1126/science.abe2402
如今,在一项新的研究中,通过在这两篇论文的基础上进行扩展,研究人员发现这种抗体鸡尾酒无论是预防性还是治疗性施用,都给模拟SARS-CoV-2感染的不同病理的动物模型带来了益处。相关研究结果于2020年10月9日在线发表在Science期刊上,论文标题为“REGN-COV2 antibodies prevent and treat SARS-CoV-2 infection in rhesus macaques and hamsters”。
在Johanna Hansen等人和Alina Baum等人在今年6月发表在Science期刊上的两篇确定并表征了一种双抗体疗法的论文的基础上,Baum及其同事们在表现出轻度COVID-19症状的恒河猴和表现出更严重COVID-19症状(包括体重快速下降)的金仓鼠中测试了这种称为REGN-COV2的抗体鸡尾酒。
这些研究人员说,当在SARS-CoV-2病毒挑战三天前进行REGN-COV2给药时,这种治疗几乎完全阻止了恒河猴体内的病毒感染。他们指出,这种能力“相当于或超过了与最近使用相同动物模型的疫苗疗效研究中显示的效果”。
15.Science:史上最大规模接触者追踪研究发现儿童和年轻人是传播新冠病毒的关键
doi:10.1126/science.abd7672; doi:10.1126/science.abe9707
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。对印度50多万暴露于SARS-CoV-2的人进行的一项新研究表明这种病毒的持续传播只由一小部分感染者推动。此外,儿童和年轻人(特别是在家庭中)在传播这种病毒方面发挥的作用可能比之前的研究所确定的更大。相关研究结果于2020年9月30日在线发表在Science期刊上,论文标题为“Epidemiology and transmission dynamics of COVID-19 in two Indian states”。
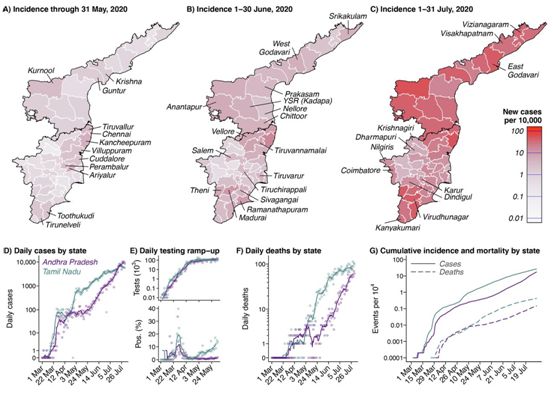
在这项新的研究中,来自美国普林斯顿环境研究所、约翰-霍普金斯大学、加州大学伯克利分校的研究人员与印度东南部的泰米尔纳德邦和安得拉邦的公共卫生官员合作,追踪了575071名接触过84965例SARS-CoV-2确诊病例的人的感染途径和死亡率。这是世界上针对任何一种疾病进行的最大规模的接触者追踪研究。
论文第一作者、普林斯顿环境研究所高级研究学者Ramanan Laxminarayan说,这项新的研究是首项捕捉COVID-19在多大程度上依赖于“超级传播(superspreading)”的大型研究。超级传播指的是一小部分感染人群将病毒传递给更多的人。这些作者发现,71%的感染者没有感染任何接触者,而仅有8%的感染者导致了60%的新感染病例。
Laxminarayan说,“我们的研究展示了我们所知道的任何传染病中最大规模的超级传播经验证明。当人们在研究COVID-19的传播时,超级传播事件是规则而不是例外,无论是在印度还是可能在所有受影响的地方。”
这些作者报告说,这些发现为COVID-19在印度等国家的传播和致命性提供了广泛的洞察力--印度经历了超过96000例COVID-19死亡事件,在这些国家,资源有限的人群发病率高。他们发现,在印度与冠状病毒相关的死亡平均发生在住院后6天,而在美国,这一数字为13天。另外,印度因冠状病毒而死亡的人群一直集中在50~64岁的人中,比美国60岁以上的高危人群略显年轻。(生物谷 Bioon.com)

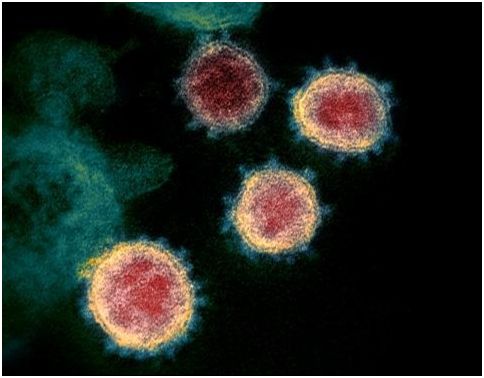
SARS-CoV-2(之前称为2019-nCoV)的透射电镜图,图片来自NIAID RML。
2020年2月11日,世卫组织将这种疾病病重命名为2019年冠状病毒病(COVID-19)。同一天,负责分类和命名病毒的的国际病毒分类学委员会的冠状病毒研究小组在bioRxiv上发表了一篇文章,指出该研究小组已经决定,新型冠状病毒2019-nCoV是导致2002-2003年爆发严 重急性呼吸综合征(SARS)冠状病毒(SARS-CoV)的变种。因此,将这种新病原体重新命名为严重急性呼吸综合征冠状病毒2号(severe acute respiratory syndrome coronavirus 2),或SARS-CoV-2。值得注意的一点是,尽管国际病毒分类委员会冠状病毒研究小组将 病毒命名为SARS-CoV-2,但该研究小组主席John Ziebuhr认为这个名字(SARS-CoV-2)和SARS(严重急性呼吸综合征,也称非典型肺炎)没有关联。不过,这种病毒的重新命名引起了不少争议。据《科学》网站报道,世界卫生组织不满意SARS-CoV-2这个名字,而且不打 算采用此名称。
冠状病毒可引起多种动物的多系统感染。在此之前已有6种冠状病毒可以感染人类,它们主要引起人类的呼吸道感染:两种高度致命性的冠状病毒,即严重急性呼吸道综合征(SARS)冠状病毒(SARS-CoV)和中东呼吸综合征(MERS)冠状病毒(MERS-CoV);4种可导致温 和的上呼吸道疾病的冠状病毒,即HCoV-OC43、HCoV-229E、HCoV-NL63和HCoV-HKU1。
基于此次疫情给中国和全世界带来严重的危害,小编针对Nature期刊上发表的2019-nCoV/COVID-19研究进行一番梳理,以飨读者。
1.Science论文解读!湖南省年初的新冠病毒传播存在大量的异质性,隔离措施成功阻断该地区的病毒传播
doi:10.1126/science.abe2424
在一项新的研究中,来自中国复旦大学、湖南省疾病预防控制中心、美国国家卫生研究院和印第安纳大学公共卫生学院等研究机构的研究人员基于通过广泛的监测和接触者追踪工作收集的细化流行病学信息,重建了截至2020年4月3日湖南省所有已确认的SARS-CoV-2感染者之间的传播链。相关研究结果于2020年11月24日在线发表在Science期刊上,论文标题为“Transmission heterogeneities, kinetics, and controllability of SARS-CoV-2”。论文通讯作者为复旦大学公共卫生学院的余宏杰(Hongjie Yu)教授和美国国家卫生研究院的Kaiyuan Sun博士。

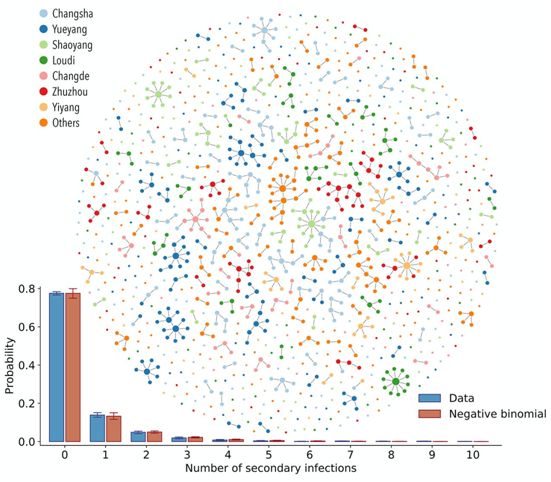
湖南省的SARS-CoV-2传播链,图片来自Science, 2020, doi:10.1126/science.abe2424。
这些作者确定了驱动传播异质性的人口、临床和行为因素,并评估了干预措施如何调节传播网络的拓扑结构。此外,他们重建了SARS-CoV-2在典型感染过程中的感染谱(infectiousness profile),并估计了通过基于个体和人群的干预措施控制疫情的可行性。
根据中国湖南患者和接触者的详细追踪数据,这些作者发现80%的继发感染可追溯到15%的SARS-CoV-2原发感染,这表明存在大量的传播异质性。传播风险与接触时间和社会互动的密切程度呈正相关,并受到人口统计学和临床因素的调节。封锁增加了家庭和家庭中的传播风险,而隔离减少了所有类型接触者的风险。针对典型SARS-CoV-2患者重建的感染谱在症状出现前达到峰值。建模结果表明,由于这种病毒的特定传播动力学,控制SARS-CoV-2疫情需要病例隔离、接触者隔离和人群水平干预措施的协同作用。
总的来说,这些作者发现病例隔离成功地阻断了湖南地区密切接触者的传播,估计有4.3%的传播发生在SARS-CoV-2患者被隔离后。在这种情况下,所有SARS-CoV-2感染者无论临床严重程度如何都在专门的医院进行医学隔离管理,而接触者则在指定的医学观察中心进行隔离。然而,在家中进行自我隔离可能并不那么有效,预计继续传播的比例应该更高。
2.Science详解:失之桑榆,收之东隅!常见的刺突蛋白突变D614G让新冠病毒高效复制,更快传播,但同时也可能让它对疫苗更加敏感
doi:10.1126/science.abe8499
在一项新的研究中,来自美国北卡罗来纳大学教堂山分校、威斯康星大学麦迪逊分校、日本国立传染病研究所和东京大学的研究人员证实冠状病毒SARS-CoV-2发生的一种称为D614G的突变使得这种病毒能够在世界范围内迅速传播,但是这种发生在刺突蛋白(S蛋白)上的突变也可能使得这种病毒对疫苗更加敏感。相关研究结果于2020年11月12日在线发表在Science期刊上,论文标题为“SARS-CoV-2 D614G variant exhibits efficient replication ex vivo and transmission in vivo”。
这种发生D614G突变的SARS-CoV-2毒株(下称D614G毒株)出现在欧洲,并已成为世界上最常见的毒株。这项研究显示,D614G毒株的复制速度更快,比最初在中国扩散的SARS-CoV-2毒株更具传播性。这些研究结果中也有亮点:虽然D614G毒株传播速度更快,但在动物研究中,它与更严重的疾病无关,而且该毒株对抗体药物的中和作用略微更加敏感。因此,这项研究提供了一些关于SARS-CoV-2如何进化的首批具体发现。
3.Science:新研究估计肯尼亚的新冠病毒抗体总体血清阳性率为4.3%
doi:10.1126/science.abe1916
在一项新的研究中,来自肯尼亚和英国的研究人员通过分析肯尼亚各地献血者的血液样本,估计到2020年6月,肯尼亚4.3%的人携带针对SARS-CoV-2冠状病毒的抗体,当时曾预计肯尼亚会有很多人死于COVID-19,但实际并没有出现如此大规模的死亡。相关研究结果于2020年11月11日在线发表在Science期刊上,论文标题为“Seroprevalence of anti–SARS-CoV-2 IgG antibodies in Kenyan blood donors”。
这些作者说,这表明SARS-CoV-2暴露情况比肯尼亚基于病例的监测所显示的更为广泛。他们的结果将有助于指导该地区的大流行病应对,在该地区,封锁的经济影响---包括它破坏了妇女和儿童的常规医疗护理的方式---已被证明是特别严重的。
4.Science:新研究表明新冠病毒可在水貂和人类之间双向传播
doi:10.1126/science.abe5901
在一项新的研究中,来自荷兰鹿特丹大学医学院等多家研究机构的研究人员对荷兰16个水貂养殖场爆发疫情的SARS-CoV-2冠状病毒的全基因组测序显示,这种病毒在人与水貂之间以及水貂与人之间传播。相关研究结果于2020年11月10日在线发表在Science期刊上,论文标题为“Transmission of SARS-CoV-2 on mink farms between humans and mink and back to humans”。

图片来自Pixabay/CC0 Public Domain。
这些作者说,这种病毒最初是从人类传入的,此后又不断进化。他们写道,“在水貂和其他鼬科动物物种中进行更多的研究对于了解这些物种是否有可能成为SARS-CoV-2的储存库非常重要。”
5.Science:此前已经存在的抗体有助于保护儿童免受新冠病毒感染
doi:10.1126/science.abe1107
弗朗西斯·克里克研究所和伦敦大学学院的研究人员发现,在普通感冒冠状病毒感染期间由免疫系统产生的某些抗体也可以靶向SARS-CoV-2,并可能针对新病毒株赋予一定程度的保护。相关研究结果发表在《Science》杂志上。
对病毒感染作出反应后,免疫系统会产生抗体来对抗病毒。这些抗体在感染后会在血液中保留一段时间,如果再次感染,它们可以再次抵抗病毒。 在这项研究中,科学家们发现,尽管从未感染过这种病毒,但某些人,尤其是儿童,其血液中的抗体对SARS-CoV-2有反应。这些抗体可能是暴露于其他冠状病毒的结果,这些冠状病毒会引起普通感冒,并且与SARS-CoV-2具有结构相似性。
研究人员在开发针对COVID-19的高度敏感的抗体测试时发现了这一发现。为了了解他们的化验测试效果如何,他们将COVID-19患者的血液与未患该疾病的患者进行了比较。令人惊讶的是,他们发现一些未暴露于SARS-CoV-2的人血液中含有可识别该病毒的抗体。为了证实他们的发现,他们分析了2011年至2018年大流行之前收集的300多个血液样本。结果表明,几乎所有样品都具有与普通感冒冠状病毒反应的抗体。但是,一小部分成年供体(约十分之一)也具有与SARS-CoV-2交叉反应的抗体。值得注意的是,这种交叉反应性抗体在6至16岁儿童的血液样本中发现的频率更高。
6.Science:美洲驼纳米抗体有望成为对抗新冠病毒的强大武器
doi:10.1126/science.abe4747
在一项新的研究中,来自美国匹兹堡大学的研究人员描述了一种从美洲驼(llama)身上提取小型的但极其强大的SARS-CoV-2抗体片段的新方法,这种抗体片段可以被制成可吸入的治疗剂,具有预防和治疗COVID-19的潜力。相关研究结果于2020年11月5日在线发表在Science期刊上,论文标题为“Versatile and multivalent nanobodies efficiently neutralize SARS-CoV-2”。
这些特殊的称为“纳米抗体(nanobody)”的美洲驼抗体比人类抗体小得多,在中和SARS-CoV-2病毒方面的效果要好很多倍。它们也更稳定。论文共同通讯作者、匹兹堡大学细胞生物学助理教授Yi Shi博士说,“大自然是我们最好的发明家。我们开发的技术以前所未有的规模调查中和SARS-CoV-2的纳米抗体,这使得我们能够迅速发现数千种具有无与伦比的亲和力和特异性的纳米抗体。”
7.Science:从头设计的蛋白诱饵在体外阻断新冠病毒感染,在体内保护仓鼠免受感染
doi:10.1126/science.abe0075
Neoleukin医疗公司(Neoleukin Therapeutics, Inc.,下称Neoleukin公司)是一家利用复杂的计算方法从头设计蛋白药物的生物制药公司。如今,在一项新的研究中,Neoleukin公司描述了旨在治疗或预防SARS-CoV-2感染的新分子。相关研究结果于2020年11月5日在线发表在Science期刊上,论文标题为“De novo design of potent and resilient hACE2 decoys to neutralize SARS-CoV-2”。
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。这项研究详细介绍了从头设计的蛋白诱饵(protein decoy)的过程,这些蛋白诱饵高亲和力地结合SARS-CoV-2刺突蛋白(S蛋白),从而阻止S蛋白与病毒受体hACE2结合,而这种受体是SARS-CoV-2感染人体细胞所必需的。
据报道,这些经过优化的高稳定性蛋白诱饵与这种病毒结合,从而阻止它进入宿主细胞。先导分子NL-CVX1(CTC-445.2d)被证明可以防止多种人类细胞系遭受SARS-CoV-2感染,并保护仓鼠免受这种病毒感染后出现的严重后果。预防性鼻内给送这些蛋白诱饵可让所有接受致命剂量SARS-CoV-2挑战的仓鼠存活下来。
8.Science:揭示超强效的合成纳米抗体中和新冠病毒机制
doi:10.1126/science.abe3255
在一项新的研究中,来自美国加州大学旧金山分校等研究机构的研究人员通过筛选酵母表面展示文库(含有大于2×109种合成纳米抗体序列)中与S蛋白胞外结构域(ectodomain)结合的纳米抗体序列,分离出中和SARS-CoV-2的单域抗体(纳米抗体)。
这些作者利用SARS-CoV-2 S蛋白的一种突变形式(SpikeS2P)作为抗原。SpikeS2P缺乏S1和S2结构域之间的两个蛋白切割位点之一,并引入两个突变和一个三聚化结构域(trimerization domain)来稳定S蛋白的融合前构象。他们用生物素或用荧光染料标记SpikeS2P,并通过多轮筛选---先是通过磁珠结合随后通过荧光活化细胞分选---来选择展示纳米体的酵母。相关研究结果近期发表在Science期刊上,论文标题为“An ultrapotent synthetic nanobody neutralizes SARS-CoV-2 by stabilizing inactive Spike ”。

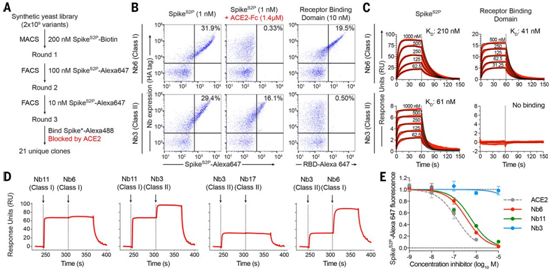
发现两种不同类别的抗S蛋白纳米抗体。图片来自Science, 2020, doi:10.1126/science.abe3255。
三轮筛选产生了21个独特的结合SpikeS2P的纳米抗体,而且ACE2胞外结构域(ACE2-Fc)的二聚体构造体可降低这种结合。这些纳米抗体分为两类。第I类纳米抗体结合RBD并直接与ACE2-Fc竞争(图1B)。这一类的典型例子是纳米抗体Nb6,它可与SpikeS2P和RBD单独结合,结合常数KD分别为210nM和41nM。第II类纳米抗体,以纳米抗体Nb3为例,它结合SpikeS2P (KD=61nM),但不显示与RBD单独结合。在存在过量ACE2-Fc的情况下,Nb6和其他I类纳米抗体的结合完全被阻断,而Nb3和其他II类纳米抗体的结合则适度下降。这些结果表明,I类纳米抗体以RBD为靶点阻断ACE2结合,而II类纳米抗体以其他表位为靶点。事实上,表面等离子共振(SPR)实验表明I类和II类纳米抗体可以同时结合SpikeS2P。
9.Science:大多数人对SARS-CoV-2产生强劲的抗体反应,而且这种抗体反应至少在5个月内保持相对稳定
doi:10.1126/science.abd7728
在一项新的研究中,来自美国西奈山伊坎医学院的研究人员发现绝大多数感染轻度到中度COVID-19的人都会产生强大的抗体反应,这种抗体反应至少在5个月内保持相对稳定。此外,他们还发现这种抗体反应与人体中和(或者说杀灭)SARS-CoV-2(导致COVID-19疾病的冠状病毒)的能力相关。相关研究结果于2020年10月28日在线发表在Science期刊上,论文标题为“Robust neutralizing antibodies to SARS-CoV-2 infection persist for months”。
论文共同通讯作者、西奈山伊坎医学院疫苗学教授Florian Krammer博士说,“虽然有些报告说针对这种病毒的抗体很快就会消失,但是我们发现恰恰相反:90%以上轻度或中度患病的人都会产生足以中和这种病毒的抗体反应,而且这种抗体反应会维持多个月。发现针对SARS-CoV-2的抗体反应的稳健性,包括它的持久性和中和作用,对于让我们能够有效地监测社区的血清阳性率并确定保护我们免受再感染的抗体的持续时间和水平至关重要。这对有效的疫苗开发至关重要。”
10.Science:重大突破!蛋白Neuropilin-1是SARS-CoV-2感染的宿主因子
doi:10.1126/science.abd3072
在一项新的研究中,来自英国布里斯托大学和澳大利亚昆士兰大学等研究机构的研究人员取得一项重大突破:他们可能发现了SARS-CoV-2冠状病毒具有高度传染性并能在人体细胞中迅速传播的原因。这些发现描述了SARS-CoV-2感染人体细胞的能力是如何通过抑制剂阻断一种新发现的病毒与宿主相互作用来降低的,这有助人们开发出一种潜在的抗病毒治疗方法。相关研究结果于2020年10月20日在线发表在Science期刊上,论文标题为“Neuropilin-1 is a host factor for SARS-CoV-2 infection”。与可引起普通感冒和轻度呼吸道症状的其他冠状病毒的不同的是,作为导致COVID-19疾病的病原体,SARS-CoV-2具有很强的传染性和传播性。在此之前,关于SARS-CoV-2为什么容易感染呼吸系统以外的大脑和心脏等器官的主要问题仍未得到解答。
在这项突破性的研究中,布里斯托大学生命科学学院的Peter Cullen教授、Yohei Yamauchi博士、Boris Simonetti博士和James Daly博士及其合作者们利用多种方法发现SARS-CoV-2能识别人体细胞表面上的一种名为神经纤毛蛋白1(neuropilin-1, NRP1)的蛋白,以促进病毒感染。
Yamauchi、Simonetti和Cullen解释道,“在研究SARS-CoV-2刺突蛋白的序列时,我们被一个小的氨基酸序列所震惊,这个序列似乎模仿了在人类蛋白中发现的与NRP1相互作用的蛋白序列。这使得使我们提出了一个简单的假设:SARS-CoV-2的刺突蛋白是否能与NRP1结合以帮助这种病毒感染人类细胞?令人兴奋的是,在应用一系列结构和生化方法时,我们能够确定SARS-CoV-2的刺突蛋白确实与NRP1结合。一旦我们确定这种刺突蛋白与NRP1结合,我们就能够证实这种相互作用可增强SARS-CoV-2对体外培养的人体细胞的入侵。重要的是,通过使用单克隆抗体(简称单抗)--实验室构建的类似于天然抗体的蛋白---或一种阻断这种相互作用的选择性药物,我们能够降低SARS-CoV-2感染人体细胞的能力。这凸显我们的发现在对抗COVID-19方面的潜在治疗价值。”
11.Science:重大突破!蛋白Neuropilin-1促进新冠病毒进入和感染人体细胞
doi:10.1126/science.abd2985
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。众所周知,SARS-CoV-2是通过受体ACE2感染宿主细胞的。在一项新的研究中,来自德国神经退行性疾病研究中心、慕尼黑工业大学、哥廷根大学医学中心和芬兰赫尔辛基大学等研究机构的研究人员发现神经纤毛蛋白1(neuropilin-1, NRP1)是一种可以促进SARS-CoV-2进入细胞内部的因子。NRP1定位于呼吸道和嗅觉上皮,这可能是一个重要的战略定位,但却有助于SARS-CoV-2的感染和传播。相关研究结果于2020年10月20日在线发表在Science期刊上,论文标题为“Neuropilin-1 facilitates SARS-CoV-2 cell entry and infectivity”。论文通讯作者为慕尼黑工业大学的Mikael Simons和赫尔辛基大学的Giuseppe Balistreri。
利用实验室培养的细胞、模拟SARS-CoV-2的人工病毒以及天然存在的病毒进行的实验表明,在ACE2存在的情况下,NRP1能够促进病毒感染。通过用抗体特异性阻断NRP1,这种病毒感染可被抑制。Simons解释说,“如果你把ACE2看作是进入细胞的一扇门,那么NRP1可能是引导这种病毒进入这扇门的一个因素。ACE2在大多数细胞中的表达水平很低。因此,这种病毒不容易找到进入细胞的门。诸如NRP1之类的其他因素可能是帮助这种病毒进入细胞的必要因素。”
12.Science:从结构上分析候选新冠疫苗NVAX-CoV2373中的全长刺突蛋白
doi:10.1126/science.abe1502
在一项新的研究中,来自美国斯克利普斯研究所的研究人员描述了一种先进的候选SARS-CoV-2 S疫苗(NVAX-CoV2373)的结构,这种候选疫苗是基于包括跨膜结构域(TM)和胞质尾区(cytoplasmic tail, CT)的全长S蛋白(氨基酸残基1~1273)开发的。相关研究结果近期发表在Science期刊上,论文标题为“Structural analysis of full-length SARS-CoV-2 spike protein from an advanced vaccine candidate”。

图片来自Science, 2020, doi:10.1126/science.abe1502。
作为这种候选疫苗中的最终构建体,SARS-CoV-2-3Q-2P也在S1/S2多碱性切割位点(polybasic cleavage site,即含有多个精氨酸残基的切割位点,其中精氨酸是碱性氨基酸)上进行修饰,使之从原先的RRAR突变为QQAQ,从而使得它具有蛋白酶抗性,与此同时在S2融合核心的K986和V987残基处进行2个脯氨酸替换以增强它的稳定性,从而产生SARS-CoV-2 3Q-2P-FL蛋白。
从昆虫细胞中表达和纯化的3Q-2P-FL蛋白,在0.01%(v/v)聚山梨酯80(PS 80)洗涤剂中配制。为了表征3Q-2P-FL免疫原的结构完整性,这些研究人员在Matrix-M佐剂存在的情况下,对在PS 80下重建的3Q-2P-FL进行了阴性染色电镜成像,从而再现了正在人类中测试的疫苗配方。这种成像显示这种三聚体3Q-2P-FL蛋白以游离三聚体或多三聚体玫瑰花结(multi-trimer rosette)的形式存在,后者含有多达14个三聚体而且它们的跨膜结构域封闭在PS 80洗涤剂的胶束核(micellar core)中。NVAX-CoV2373纳米颗粒疫苗配方中的3Q-2P-FL蛋白紧密簇聚可能导致比单独的可溶性三聚体更强的免疫反应,这一点类似于其他的病毒糖蛋白免疫原(流感病毒的HA蛋白和RSV病毒的 F蛋白)。
13.Science:全球200名科学家们通力合作揭示SARS-CoV-2、SARS-CoV-1和MERS-CoV冠状病毒的共同弱点
doi:10.1126/science.abe9403
近日,一项刊登在国际杂志Science上的研究报告中,来自乔治亚州立大学等机构的科学家们通过研究发现,三种致命的冠状病毒:SARS-CoV-2、SARS-CoV-1和MERS-CoV都有共同的弱点,比如会频繁劫持细胞中的信号通路,这或许有望帮助研究人员寻找有效广泛抑制冠状病毒感染的潜在靶点和疗法。
在过去20年里,全球面临着三种致命性的冠状病毒,即SARS-CoV-2、SARS-CoV-1和MERS-CoV,而SARS-CoV-2所诱发的COVID-19在全球引起了疾病的大流行,目前在全球已经感染了3700多万人,而且造成了100多万人死亡。这项研究中,研究人员通过研究确认了冠状病毒之间的共性,并解释了多个共同的细胞过程和蛋白靶点,其或能作为新型靶点帮助开发当前和未来冠状病毒感染大流行的治疗性和干预性措施。
这项研究是由来自6个国家14个领先的研究机构中将近200名科学家们合作完成的;此前研究中,研究人员识别了超过300个能与SARS-CoV-2蛋白相互作用的宿主蛋白,这项研究中,研究人员想进一步研究筛选出拥有能改变病毒生长能力的特殊宿主蛋白。研究者Christopher Basler说道,我们至少发现了20个宿主基因所编码的蛋白产物能明显改变感染的宿主细胞产生病毒的水平,这些蛋白质或许就能作为开发治疗性干预措施的潜在靶点,比如,如果某一种细胞蛋白是病毒有效生长所需要的,那么抑制细胞中特殊蛋白的药物或能减缓病毒的感染过程。
14.Science:揭示抗体混合物REGN-COV2有望预防和治疗新冠肺炎
doi:10.1126/science.abe2402
如今,在一项新的研究中,通过在这两篇论文的基础上进行扩展,研究人员发现这种抗体鸡尾酒无论是预防性还是治疗性施用,都给模拟SARS-CoV-2感染的不同病理的动物模型带来了益处。相关研究结果于2020年10月9日在线发表在Science期刊上,论文标题为“REGN-COV2 antibodies prevent and treat SARS-CoV-2 infection in rhesus macaques and hamsters”。
在Johanna Hansen等人和Alina Baum等人在今年6月发表在Science期刊上的两篇确定并表征了一种双抗体疗法的论文的基础上,Baum及其同事们在表现出轻度COVID-19症状的恒河猴和表现出更严重COVID-19症状(包括体重快速下降)的金仓鼠中测试了这种称为REGN-COV2的抗体鸡尾酒。
这些研究人员说,当在SARS-CoV-2病毒挑战三天前进行REGN-COV2给药时,这种治疗几乎完全阻止了恒河猴体内的病毒感染。他们指出,这种能力“相当于或超过了与最近使用相同动物模型的疫苗疗效研究中显示的效果”。
15.Science:史上最大规模接触者追踪研究发现儿童和年轻人是传播新冠病毒的关键
doi:10.1126/science.abd7672; doi:10.1126/science.abe9707
新型冠状病毒SARS-CoV-2导致2019年冠状病毒病(COVID-19),如今正在全球肆虐。对印度50多万暴露于SARS-CoV-2的人进行的一项新研究表明这种病毒的持续传播只由一小部分感染者推动。此外,儿童和年轻人(特别是在家庭中)在传播这种病毒方面发挥的作用可能比之前的研究所确定的更大。相关研究结果于2020年9月30日在线发表在Science期刊上,论文标题为“Epidemiology and transmission dynamics of COVID-19 in two Indian states”。

印度泰米尔纳德邦和安得拉邦各地区的发病率,图片来自Science, 2020, doi:10.1126/science.abd7672。
在这项新的研究中,来自美国普林斯顿环境研究所、约翰-霍普金斯大学、加州大学伯克利分校的研究人员与印度东南部的泰米尔纳德邦和安得拉邦的公共卫生官员合作,追踪了575071名接触过84965例SARS-CoV-2确诊病例的人的感染途径和死亡率。这是世界上针对任何一种疾病进行的最大规模的接触者追踪研究。
论文第一作者、普林斯顿环境研究所高级研究学者Ramanan Laxminarayan说,这项新的研究是首项捕捉COVID-19在多大程度上依赖于“超级传播(superspreading)”的大型研究。超级传播指的是一小部分感染人群将病毒传递给更多的人。这些作者发现,71%的感染者没有感染任何接触者,而仅有8%的感染者导致了60%的新感染病例。
Laxminarayan说,“我们的研究展示了我们所知道的任何传染病中最大规模的超级传播经验证明。当人们在研究COVID-19的传播时,超级传播事件是规则而不是例外,无论是在印度还是可能在所有受影响的地方。”
这些作者报告说,这些发现为COVID-19在印度等国家的传播和致命性提供了广泛的洞察力--印度经历了超过96000例COVID-19死亡事件,在这些国家,资源有限的人群发病率高。他们发现,在印度与冠状病毒相关的死亡平均发生在住院后6天,而在美国,这一数字为13天。另外,印度因冠状病毒而死亡的人群一直集中在50~64岁的人中,比美国60岁以上的高危人群略显年轻。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


