宫颈癌免疫治疗!欧盟批准抗PD-L1疗法Libtayo:无论PD-L1表达水平或肿瘤组织学如何,均显著延长患者生存!
来源:生物谷原创 2022-11-25 12:03
Libtayo是第一个在晚期宫颈癌3期试验中被证实与化疗相比显著延长总生存期(OS)的PD-1抑制剂:Libtayo与化疗相比,将死亡风险降低31%。
图片来源:摄图网
2022年11月22日讯 /生物谷BIOON/ --再生元(Regeneron)近日宣布,欧盟委员会(EC)已批准抗PD-1疗法Libtayo(cemiplimab):作为一种单药疗法,用于治疗接受铂类化疗期间或之后疾病进展的复发或转移性宫颈癌成人患者。此次批准标志着一个重大进步,Libtayo将为这类患者提供一种新的标准护理疗法。
近年来,尽管在预防和治疗宫颈癌方面取得了进展,但复发或转移病例患者的选择仍然有限。Libtayo是第一个在晚期宫颈癌3期试验中证明与化疗相比显著延长总生存期(OS)的PD-1抑制剂。随着欧盟委员会的第四次批准,Libtayo现在可用于治疗欧盟的晚期宫颈癌患者,无论其PD-L1状态或组织学如何。
截至目前,Libtayo在欧盟被批准用于治疗4种癌症:晚期基底细胞癌(BCC)、晚期皮肤鳞状细胞癌(CSCC)、晚期非小细胞肺癌(NSCLC)、晚期宫颈癌。在美国,Libtayo被批准用于治疗3种癌症(BCC、CSCC、NSCLC)。
此次最新批准基于3期临床试验EMPOWER-Cervical 1(NCT03257267)的结果。这是在晚期宫颈癌开展的大规模临床试验,入组了先前接受含铂化疗治疗后疾病进展的复发或转移性宫颈癌患者,不论PD-L1表达状态或组织学如何。研究中,将Libtayo单药疗法与研究调查员选择的化疗进行了对比。
结果显示,该试验达到了总生存期(OS)主要终点:无论PD-L1表达状态或肿瘤组织学如何,与二线化疗相比,Libtayo治疗均显著改善OS,在整个患者群体中将死亡风险降低31%(HR=0.69,单侧p<0.001),在鳞状细胞癌(SCC)患者中将死亡风险降低27%(HR=73;95%CI:0.58-0.91;单侧p=0.003)。该试验的详细数据已于2022年2月发表于国际顶级医学期刊《新英格兰医学杂志》(NEJM)。详见:Survival with Cemiplimab in Recurrent Cervical Cancer。
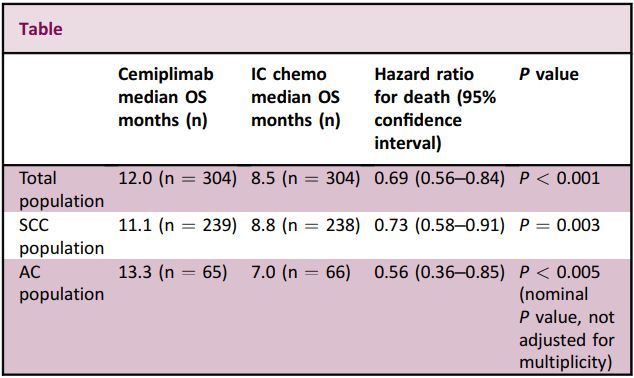
EMPOWER-Cervical 1临床试验数据(图片来源:NEJM)
EMPOWER-Cervical 1是一项开放标签、多中心的3期临床试验,在接受含铂化疗但病情进展的复发或转移性宫颈癌患者中开展,将Libtayo单药疗法与研究者选择的复发或转移性宫颈癌常用化疗方案进行了比较。无论患者肿瘤PD-L1表达情况如何均可入组,78%的患者为鳞状细胞癌(SCC),22%的患者为腺癌(AC)。
这是晚期宫颈癌治疗方面开展的一项大规模3期随机临床试验,共入组了全球14个国家的608例女性患者(中位年龄:51岁)。这些患者被随机分为2组,一组接受Libtayo单药治疗(n=304;每3周一次,350毫克),另一组接受研究者选择的常用化疗方案(n=304;培美曲塞、长春瑞滨、拓扑替康、伊立替康或吉西他滨)。
试验结果表明,与化疗组相比,Libtayo治疗组患者在总生存期(OS)、无进展生存期(PFS)、客观缓解率(ORR)方面均有显著改善:
——在整个研究群体(SCC+AC)中:(1)死亡风险降低了31%,Libtayo治疗组(n=304)中位OS为12.0个月、化疗组(n=304)为8.5个月,数据具有统计学显著差异(HR=0.69;95%CI:0.56-0.84;双侧p<0.001)。(2)疾病进展风险降低25%(HR=0.75;95%CI:0.63-0.89;双侧p<0.001)。(3)ORR显著提高(16.4% vs 6.3%;双侧p<0.001)、中位缓解持续时间(DOR)显著延长(16.4个月 vs 6.9个月)。
——在鳞状细胞癌群体(SCC)中:(1)死亡风险降低27%,Libtayo治疗组(n=239)中位OS为11.1个月、化疗组(n=238)为8.8个月,数据具有统计学显著差异(HR=0.73;95%CI:0.58-0.91;双侧p=0.006)。(2)疾病进展风险降低29%(HR=0.71;95%CI:0.58-0.86;双侧p<0.001)。(3)ORR提高(17.6% vs 6.7%;双侧p<0.001)。
——在腺癌群体(AC)中:(1)死亡风险降低44%,Libtayo治疗组(n=65)中位OS为13.3个月、化疗组(n=66)为7.0个月,数据具有统计学显著差异(HR=0.56;95%CI:0.36-0.85)。(2)疾病进展风险降低9%(HR=0.91;95%CI:0.62-1.34)。(3)ORR提高(12% vs 4%)。
——健康状况/生活质量:Libtayo治疗的患者随着时间的推移,总体上能够改善或维持其基线的整体健康状况/生活质量(GHS/QOL),而那些接受化疗的患者则经历了从第8周期开始具有临床意义的恶化,根据EORTC QLQ-C30(总体估计平均变化95%CI:Libtayo改善1.0[95%CI:-2.0,4.0],化疗恶化-6.8[95%CI:-11.0,-2.6];差值=7.8)。
——该试验中,没有观察到Libtayo新的安全信号。Libtayo治疗组有88.3%的患者、化疗组有91.4%的患者出现不良事件,分别有29.7%、26.9%的患者出现严重不良事件。
宫颈癌是全世界女性癌症死亡的第四大原因,最常见的诊断年龄在35-44岁之间。据估计,全世界每年约有60万女性被诊断患有宫颈癌,每年死亡超过35万例。几乎所有的宫颈癌病例都是由人乳头瘤病毒(HPV)感染引起的,大约80%被归类为鳞状细胞癌(起源于宫颈底部的细胞),其余大部分是腺癌(起源于宫颈上部的腺细胞)。子宫颈癌在早期发现和有效治疗时通常是可以治愈的,但晚期的治疗选择较为有限。
Libtayo属于PD-(L)1抑制剂,这是当前备受瞩目的一类肿瘤免疫疗法,旨在利用人体自身的免疫系统抵御癌症,通过阻断PD-1/PD-L1信号通路使癌细胞死亡,具有治疗多种类型肿瘤的潜力。Libtayo是一种全人单抗,靶向T细胞上的免疫检查点受体PD-1。通过与PD-1结合,Libtayo已被证明可以阻止癌细胞通过PD-1途径抑制T细胞的活化。
在美国,Libtayo已被批准用于治疗2种最常见的皮肤癌晚期患者:(1)Libtayo是第一个获批治疗晚期皮肤鳞状细胞(CSCC)的药物,适用于治疗转移性CSCC患者以及不适合根治性手术或根治性放疗的局部晚期CSCC患者;(2)Libtayo是第一个获批治疗晚期基底细胞癌(BCC)的免疫疗法,该药适用于治疗先前已接受过一种hedgehog通路抑制剂(HHI)治疗或不适合该类药物治疗的晚期BCC患者。
2021年2月,Libtayo获得美国FDA批准第3个适应症:用于一线治疗肿瘤高表达PD-L1(肿瘤比例得分[TPS]≥50%)的晚期非小细胞肺癌(NSCLC)患者,具体为:肿瘤高表达PD-L1(TPS≥50%)、有转移性或局部晚期肿瘤、不适合手术切除或根治性放化疗、肿瘤无EGFR、ALK或ROS1畸变的NSCLC患者。
Libtayo采用再生元专利化的Velocimmune技术平台创造并优化,目前正被开发用于多种类型癌症的治疗。Libtayo的广泛临床项目集中在难治癌症上,包括皮肤癌、宫颈癌、实体瘤和血液癌症。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


