新证据!ASK 相关中和抗体混合物阻断SARS-CoV-2 感染人肺类器官
来源:本站原创 2022-02-14 14:13
细胞表面受体在决定病毒致病机制中起着关键作用。然而,除了血管紧张素转换酶(ACE2),人们对SARS-CoV-2宿主受体知之甚少。
细胞表面受体在决定病毒致病机制中起着关键作用。然而,除了血管紧张素转换酶(ACE2),人们对SARS-CoV-2宿主受体知之甚少。此外,单独的ACE2不能解释SARS-CoV-2的多器官嗜性,也不能解释SARS-CoV-2与SARS-CoV的临床差异,提示其他受体参与其中。
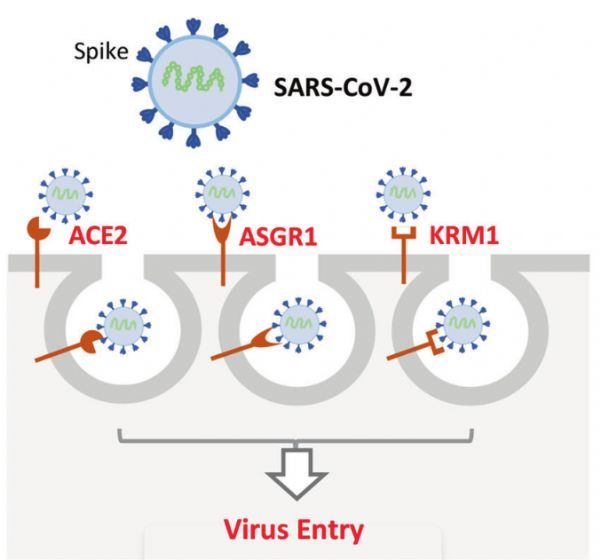
SARS-CoV-2利用不同的血管紧张素转化酶2/去唾液酸糖蛋白受体1/含环状结构跨膜蛋白1(ACE2/ASGR1/KREMEN1, ASK)受体组合进入不同的细胞类型,在细胞和组织水平上,ASK的共同表达与病毒易感性的相关性明显强于任何单个受体。
类器官(Organoids)是指类似于组织器官。其实是一种基于3D体外细胞培养系统建立的,与体内的来源组织或器官高度相似的一种模型,是疾病研究的利器。本研究通过应用类器官技术检测了ASK 相关中和抗体混合物阻断SARS-CoV-2 感染人肺类器官。
图片来源: https://doi.org/10.1038/s41422-021-00595-6
近日,上海复旦大学研究者在Cell Research杂志上发表题为“Receptome profiling identifies KREMEN1 and ASGR1 as alternative
functional receptors of SARS-CoV-2”的文章,在本研究中,作者筛选了5054个单独的人膜蛋白与SARS-CoV-2衣壳刺突(S)蛋白的相互作用,包括ACE2、ASGR1和KREMEN1在内的12种蛋白具有不同的S结合亲和力和模式。ASGR1或KREMEN1足以使SARS-CoV-2进入,但在体内和体外均不能。
该研究揭示了SARS-CoV-2的一个相互作用的宿主受体,并确定了去唾液酸糖蛋白受体1(ASGR1)和含环状结构跨膜蛋白1(KREMEN1)作为替代功能受体,在不依赖ace2的病毒进入过程中发挥重要作用,为深入了解SARS-CoV-2的向性和发病机制提供了线索,以及进一步调查COVID-19的社区资源和潜在治疗策略。
为了在更生理的条件下测试抗体,作者用人类肺类器官进行了实验,检测人肺组织中ASK受体的表达,可以清楚地检测到ACE2、ASGR1和KREMEN1,并且它们的表达几乎没有重叠,这与细胞RNA测序(scRNA-seq)数据一致。
为了更清楚地观察病毒感染,作者用含有GFP报告的SARS-CoV-2S-伪型病毒感染人肺类器官。为了验证这些结果,作者用正宗的SARS-COV-2感染肺类组织,观察到ACE2表达和不表达的细胞都被SARS-COV-2感染,并在SARS-COV-2+ACE2的阴性细胞中检测到kremen1或ASGR1。另外,研究结果还发现,与单独的ASK抗体相比,ASK合成物发挥了显著更高的抑制作用,对假型或真的sars-cov-2的感染提供了最实质性的阻断
。
ASK受体介导的SARS-CoV-2进入示意图
图片来源: https://doi.org/10.1038/s41422-021-00595-6
本研究指出替代的病毒结合受体可能发挥上下文相关的调节作用,导致不同的信号结果,最终影响感染模式、免疫反应和临床进展。本研究确定了一组具有不同S结合模式、信号特性和组织分布的受体样宿主因子,并证明ASGR1和KREMEN1是可替代的功能受体,在ACE2非依赖性病毒进入过程中发挥重要作用,为深入了解SARS-CoV-2的关键病毒-宿主相互作用提供了深入的见解,也为进一步研究新冠肺炎提供了有用的资源和潜在的药物靶点。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。