Nature:靶向PD-L2–RGMb有望增强克服肠道菌群相关的免疫治疗抵抗力,增强癌症免疫疗法的疗效
来源:生物谷原创 2023-05-16 11:29
癌症免疫疗法已经改变了许多类型癌症的治疗。然而,由于仍然不甚明了的原因,并非所有患者都能从这些强大的疗法中获得同样的益处。
癌症免疫疗法已经改变了许多类型癌症的治疗。然而,由于仍然不甚明了的原因,并非所有患者都能从这些强大的疗法中获得同样的益处。
在一项新的研究中,来自美国哈佛医学院和丹娜-法伯癌症研究所的研究人员指出影响癌症免疫疗法治疗结果的一个有力因素似乎是患者的肠道菌群---生活在人类肠道中的数万亿个微生物。相关研究结果于2023年5月3日在线发表在Nature期刊上,论文标题为“Targeting PD-L2–RGMb overcomes microbiome-related immunotherapy resistance”。

这项研究是在小鼠身上完成的,它指出了肠道微生物如何增强身体对一种称为称为PD-1检查点阻断疗法的常见免疫疗法的反应。目前,PD-1检查点阻断疗法用于治疗25种形式的癌症。
该研究发现,特定的肠道细菌可以影响两种免疫分子---PD-L2和RGMb---的活性,以及它们之间的相互作用。该研究还表明,阻断其中任何一种分子的活性或它们之间的相互作用,可以增强对癌症免疫疗法的反应,优化身体检测和摧毁癌细胞的能力。
论文共同通讯作者、哈佛医学院布拉瓦特尼克研究所免疫学系主任Arlene Sharpe说,“我们的研究表明,用阻断PD-L2与RGMb相互作用的抗体进行治疗可以解除对抗癌T细胞的抑制,使得它们能够根除肿瘤。”
这项新的研究还确定了RGMb分子是以前未知的破坏身体发现和摧毁肿瘤能力的帮凶。RGMb主要以其在神经系统发育中的作用而闻名,也在抗癌的T细胞表面上发现。然而,在此之前,没有人知道它在调节T细胞对癌症免疫疗法的反应方面发挥了作用。
这些作者指出,如果在人类身上得到重现,这些发现可以为开发改善免疫疗法治疗结果的疗法提供信息。
论文共同第一作者、Sharpe实验室免疫学博士后研究员Joon Seok Park说,“我们的发现为一个复杂的难题提供了关键的线索,并以此提出了增强癌症免疫疗法效力和改善患者预后的具体方法。我们提出了一种新的方法,通过了解帮助我们的免疫系统对抗癌症的肠道细菌来克服这种疾病对当前癌症免疫疗法的抵抗。”
癌症如何躲避免疫检测和破坏
癌症生存和扩散的关键是它逃避身体免疫防御的能力。从20世纪90年代开始,Sharpe和丹娜-法伯癌症研究所医学教授Gordon Freeman进行了一些关键的早期研究工作,阐明了癌症如何做到这一点。
Sharpe和Freeman的研究工作集中在两种驻留在免疫细胞表面上的分子---PD-L1和PD-L2。他们的研究已表明,当PD-L1或PD-L2与T细胞表面的另一种称为PD-1的分子相互作用时,T细胞的活性就会受到控制。在正常情况下,这种相互作用对T细胞起到了刹车的作用,以确保它们不会错误地攻击身体自身的细胞和组织。
Sharpe、Freeman和其他人已发现癌症正是利用了这种安全机制来逃避T细胞的检测和破坏。癌细胞通过在它们的表面上表达PD-L1和PD-L2,与PD-1结合并控制T细胞来做到这一点。阻断PD-1与PD-L1或PD-L2的相互作用的癌症免疫疗法释放了T细胞对癌症的攻击,,因而被称为免疫检查点阻断。
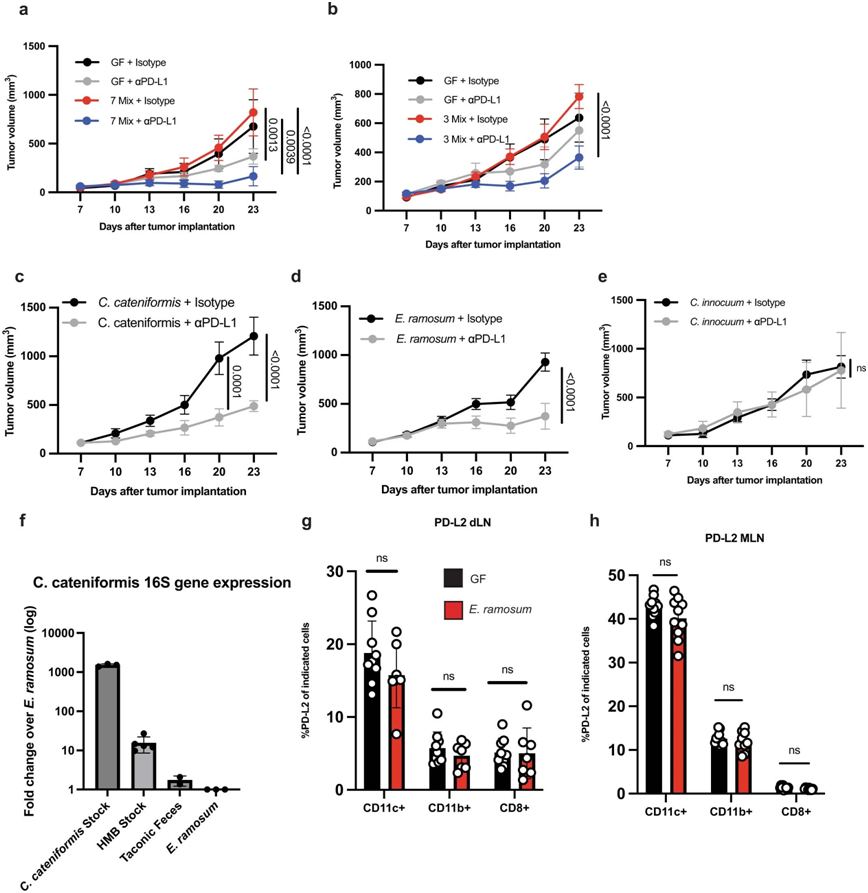
图片来自Nature, 2023, doi:10.1038/s41586-023-06026-3。
这类免疫方法目前用于25种形式的癌症,已经彻底改变了癌症护理,但有一部分患者并没有从中受益。自从这些治疗方法出现以来科学家们一直在试图了解其中的原因。
多年来,免疫系统和肠道菌群之间的相互作用一直是哈佛医学院布拉瓦特尼克研究所免疫学教授Dennis Kasper的研究重点。他的实验室不仅确定了调节机制,而且还确定了负责调节免疫系统的特定微生物分子和微生物酶。
肠道微生物可能影响癌症免疫疗法的概念并不完全是新的。近期的研究已发现了关于肠道微生物在免疫疗法治疗结果中的作用的诱人线索。然而,在此之前,一个关键的问题仍未得到解答:如何做到这一点?
一个新的参与者进入现场
在这项新的研究中,这些作者以小鼠为研究对象,它们的结肠被植入了癌症患者的肠道菌群。其中一些患者对免疫疗法反应良好,而另一些则没有获得什么好处。这些小鼠对免疫疗法的反应模拟了肠道中栖息着肠道微生物的人类的治疗反应。
这些作者比较了这两组小鼠的免疫系统特征,发现参与癌症检测和破坏的多种免疫细胞存在明显的差异。这一发现表明肠道菌群改变了这些免疫细胞的行为,从而改变了对免疫疗法的反应。
小鼠接种了来自对癌症免疫疗法反应良好的患者的肠道微生物后,一类称为抗原呈递细胞的免疫细胞表面上的PD-L2水平较低。这些细胞在召集身体的免疫防御方面发挥着关键作用。它们通过在体内巡逻寻找病原体或肿瘤,并将这些外来或异常的蛋白呈现给T细胞进行破坏。相反,接种了来自对免疫疗法反应不佳的患者的肠道微生物的小鼠具有增加的PD-L2分子水平。
为了弄清特定肠道微生物的影响,这些作者让这些小鼠接受杀死肠道细菌的广谱抗生素处理。经抗生素处理的小鼠对阻断PD-1分子的免疫疗法没有反应。然而,这些小鼠的PD-L2水平很高,这是另一种通常通过PD-1起作用的分子制动器。对这种相同处理有强烈反应的小鼠的PD-L2水平较低。
这些作者对PD-1阻断不起作用感到好奇,他们假设PD-L2不是单独通过PD-1而是通过另一种分子帮凶对T细胞起制动作用。他们将注意力转向了RGMb,Freeman实验室之前已证实RGMb和PD-L2调节肺部的免疫耐受。
当这些作者用阻断RGMb的抗体治疗那些对单独的抗PD-1疗法没有反应的小鼠时,这些小鼠经历了抗癌T细胞的增加和快速的整体改善。
Freeman说,“肠道菌群和免疫细胞在抗癌反应中的相互作用变得更加清晰,而且随着RGMb被确定为PD-L2的分子帮凶,我们有了癌症免疫疗法的另一种靶标。”
进一步的分析表明RGMb和PD-L2之间的这种相互作用取决于肠道微生物的组成。他们发现,某些肠道微生物可以影响这两种分子的水平。
肠道中接种了某些肠道微生物的患癌小鼠在它们的T细胞表面上的RGMb水平比肠道中没有微生物的小鼠低六倍,并且对抗PD-L1或抗PD-1免疫疗法有反应。相比之下,肠道微生物群被剔除的小鼠对这些治疗没有反应,它们的T细胞表面上的RGMb水平较高,尤其是浸润到肿瘤的T细胞表面上。
同样地,在小鼠的肠道中接种了来自治疗反应不佳的患者肠道菌群后,它们的RGMb水平也较高,这一发现表明,对癌症免疫疗法没有良好反应的患者,其T细胞表面上的RGMb水平较高,这反过来干扰了体内免疫细胞的抗肿瘤反应。
让PD-L2或RGMb失活足以保持T细胞的抗肿瘤活性,并确保对PD-L1和PD-1疗法的强劲反应。值得注意的是,阻断PD-L2的活性导致在接受另一种称为树突状细胞疗法的癌症免疫疗法的小鼠中产生强大的抗肿瘤反应。这一观察表明,调节PD-L2的活性有希望提高对多种类型癌症免疫疗法的反应。
肠道微生物调节身体中的免疫反应
通过改变不同组小鼠的肠道菌群的组成,这些作者发现一种肠道微生物,即C. cateniformis,抑制了PD-L2的水平,并使免疫疗法对患癌小鼠更加有效。
这些作者指出,鉴于人类的肠道有成千上万种细菌,这种微生物可能不是唯一能够调节抗肿瘤免疫的肠道微生物。
这一发现表明,特定的微生物分子可以以小分子药物的形式加以利用,增强免疫系统控制癌症的能力。这类治疗可能补充或替代传统的基于抗体的癌症免疫疗法。
Sharpe指出,小分子方法的额外吸引力是开发和储存成本更低,更容易进入人体。小分子药物通常是以药片的形式给药,而癌症免疫疗法是以静脉注射抗体的形式进行的。
这些作者提醒说,虽然他们的研究揭示了这个谜题的关键部分,但这可能只是免疫系统和肠道菌群在癌症中相互作用的几种方式之一。
论文共同第一作者、Kasper实验室前博士后研究员Francesca Gazzaniga说,“这可能只是故事的开始。癌症、免疫系统和肠道微生物组各自的复杂程度令人震惊,但当你把这些系统放在一起时,所产生的相互作用就会成倍地复杂化。”
Kasper,“一般而言,肠道微生物组可能会以许多其他方式影响癌症免疫,特别是癌症免疫疗法。通过这项研究,我们发现了一种全新的方式来研究肠道菌群如何不仅影响癌症治疗的疗效,还如何影响癌症免疫。”(生物谷 Bioon.com)
参考资料:
Joon Seok Park et al. Targeting PD-L2–RGMb overcomes microbiome-related immunotherapy resistance. Nature, 2023, doi:10.1038/s41586-023-06026-3.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


