银屑病创新药!优时比IL-17A/17F双效抑制剂Bimzelx(bimekizumab)在美国监管受挫!
来源:生物谷原创 2022-05-19 11:30
Bimzelx能够强效中和IL-17A和IL-17,3期临床疗效优于修美乐(Humira)、喜达诺(Stelara)、可善挺(Cosentyx)。
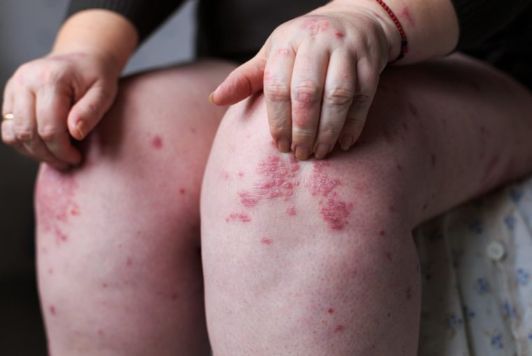
斑块型银屑病(图片来源:dermatologyadvisor.com)
2022年05月16日讯 /生物谷BIOON/ --优时比(UCB)近日宣布,美国食品和药物管理局(FDA)已针对其新型抗炎药Bimzelx(bimekizumab)治疗中度至重度斑块型银屑病的生物制品许可申请(BLA)发布了一封完整回应函(CRL)。CRL表明,FDA不能以当前的形式批准申请。CRL中指出,在批准申请之前,必须解决在批准前检查(Pre-Approval Inspections,PAI)中发现的问题。目前,优时比正在与FDA合作,并正在努力尽快解决这些问题。
Bimzelx是一款IL-17A/IL-17F抑制剂,是第一个旨在选择性和直接抑制2种关键细胞因子(IL-17A和IL-17F)所驱动炎症过程的银屑病治疗药物。
Bimzelx于2021年8月在欧盟和英国获得批准,用于治疗适合系统治疗的中度至重度斑块型银屑病成人患者。今年1月,Bimzelx在日本获批,用于治疗对现有疗法应答不足的斑块型银屑病、泛发性脓疱型银屑病、红皮病型银屑病患者。今年2月和3月,Bimzelx分别在加拿大和澳大利亚获批,用于治疗适合系统治疗或光疗的中度至重度斑块型银屑病患者。
在治疗中重度斑块型银屑病的3期临床研究中,Bimzelx疗效已被证实优于艾伯维Humira(修美乐,阿达木单抗,adalimumab,TNF抑制剂)、强生Stelara(喜达诺,乌司奴单抗,ustekinumab,IL-12/IL-23抑制剂)、诺华Cosentyx(可善挺,司库奇尤单抗,secukinumab,IL-17A抑制剂),显示出更高水平的皮损清除。在这些研究中,Bimzelx治疗的患者中约60%在第16周达到了皮损完全清除且反应持续一年,并且总体耐受性良好。
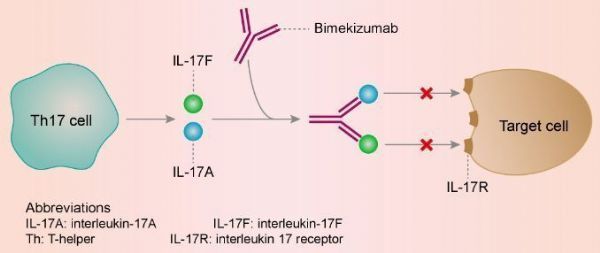
bimekizumab作用机制(图片来源:mosmedpreparaty.ru)
银屑病是一种常见的慢性炎症性疾病,主要累及皮肤。银屑病有几种类型,但斑块型银屑病最常见,占所有病例的58%-97%。斑块型银屑病的特征是干燥的红色斑块,通常覆盖着银色或白色鳞片。泛发性脓疱型银屑病不太常见,影响所有病例的1.1%-12%,其特征是脓疱愈合,充满非传染性脓液。红皮病型银屑病是银屑病中最严重的一种,其特征是大部分体表出现火红和脱落,占所有病例的0.4%-7%。
Bimzelx的活性药物成分bimekizumab是一种具有双重作用机制的独特分子,这是一种新型人源化单克隆IgG1抗体,能强效、选择性地中和IL-17A和IL-17F,这是驱动炎症过程的2种关键细胞因子。IL-17A和IL-17F具有相似的促炎功能,并独立地与其他炎症介质合作,在多个组织中驱动慢性炎症和损害。
bimekizumab独特的IL-17A/IL-17F双重抑制可能为治疗免疫介导的炎症性疾病提供一种新的靶向疗法。在疾病相关细胞中的临床前研究显示,在抑制IL-17A的同时抑制IL-17F能够减少皮肤和关节炎症以及病理性骨形成,其程度大于单独抑制IL-17A的程度。
目前,优时比也正在3期临床试验中,评估bimekizumab治疗银屑病关节炎(PsA)、强直性脊柱炎(AS)、非放射学中轴型脊柱关节炎(nr-axSpA)、化脓性汗腺炎的疗效和安全性。此前,医药市场调研机构Evaluate Vantage发布报告预测,bimekizumab上市后,2026年的全球销售额将达到26亿美元。(生物谷Bioon.com)
原文出处:Update on U.S. FDA Review of Biologics License Application (BLA) for bimekizumab
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


