Science:震惊!人类STING 竟是一种质子通道,可允许质子从高尔基体中泄漏出来
来源:生物谷原创 2023-08-28 15:43
一种名为 STING 的信号蛋白是人体免疫系统中的关键角色,它能检测细胞内的危险信号,然后激活多种防御机制。
一种名为 STING 的信号蛋白是人体免疫系统中的关键角色,它能检测细胞内的危险信号,然后激活多种防御机制。
STING 主要负责侦测 DNA,这可能预示着外来入侵者(如病毒)或宿主组织或细胞受损。当 STING 检测到这一危险信号时,它会开启至少三种不同的途径---第一种产生干扰素,第二种是非经典自噬(参与细胞成分的回收和病原体的清除),第三种是形成炎性体(一种激活炎症反应的蛋白复合物)。
STING刺激干扰素产生的机制已被充分描述,但人们还不清楚它如何激活其他两种途径。如今,在一项新的研究中,来自美国麻省理工学院和哈佛医学院等研究机构的研究人员发现了 STING 如何激活这两种途径。他们发现人类STING 具有一种令人惊讶的、以前未知的功能:它可以充当离子通道,允许质子从一种称为高尔基体的细胞器中泄漏出来。这使它成为第一种能将危险信号转化为离子流的人类免疫传感器。相关研究结果发表在2023年8月4日的Science期刊上,论文标题为“Human STING is a proton channel”。

论文共同通讯作者、哈佛医学院医学教授Nir Hacohen说,“要得出 STING 是质子通道的这一新观点,需要将其他实验室之前的发现联系起来,即 STING 或质子通量(proton flux)都能激活炎性体和非经典自噬,这让我们假设 STING 启动或介导质子通量,从而触发这两个下游过程。”
论文共同通讯作者、麻省理工学院科赫综合癌症研究所的Darrell Irvine教授说,“由于它对宿主免疫的重要性,人们对开发能够激活或抑制STING活性的药物非常感兴趣,而STING离子通道活性的发现将为设计调节STING的药物提供新的思路。”
令人惊讶的作用
STING被认为是引发感染、自身免疫和癌症中免疫反应的主要因素之一。激活 STING 的药物已被开发出来并作为将有助于刺激免疫系统摧毁肿瘤的癌症免疫疗法药物进行临床试验。
STING 是一种可以跨膜的蛋白,它通常被嵌入一种叫做内质网(ER)的细胞器的膜中。一旦检测到DNA,它就会转移到高尔基体,在那里开始激活蛋白,从而开启产生干扰素所需的基因。
论文共同通讯作者、麻省理工学院生物学博士生Bingxu Liu说,“人们很清楚STING是如何诱导干扰素的,但STING是如何诱导自噬和炎性体形成的,这在过去10年里一直是这个领域的一个公开争论点。”
以前的研究已表明,自噬和炎性体(刺激炎症的大型蛋白复合物)的形成都可以由细胞器中的质子泄漏引起,其中质子泄漏会使细胞内部酸性增强。因此,这些作者想知道 STING 是否会以某种方式诱导质子泄漏。
为了探索这种可能性,这些作者在高尔基体上标记了一种在pH值升高时会发出荧光的蛋白。当他们用一种能激活 STING 的分子处理细胞时,高尔基体的酸性降低了,这意味着它正在失去质子。通过基因筛选,他们最大限度地排除了另一种离子通道控制这种离子流动的可能性,因此他们假设 STING 本身就是一种质子通道。
麻省理工学院生物工程副教授Paul Blainey说,“除了生物学意义之外,这项新的研究也是功能基因组学领域日趋成熟的一个显著例证,在这一领域,混合筛选(pooled screening)数据的可靠性足以确定重点研究的方向---即使是阴性结果,正如这项新的研究就是如此。”
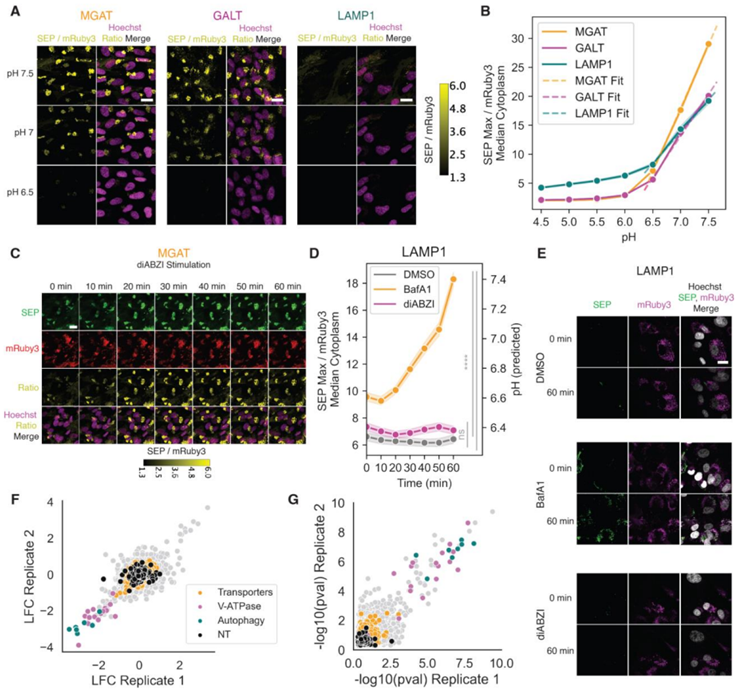
图片来自Science, 2023, doi:10.1126/science.adf8974。
在通过可以预测给定的蛋白结构是否含有孔的计算机模型分析了STING蛋白的结构后,这些作者发现,STING 蛋白经预测后包含一个类似孔的区域。偶然的是,去年一家寻找 STING 激动剂(激活 STING 的分子)的公司发现了一种新分子,后来一个学术小组证明了这种分子可以在这个精确的位置结合。
这些作者推测,这种称为 C53 的STING激动剂阻塞了这个假定的孔。在细胞中加入 C53 后,质子没有从高尔基体中泄漏出来,激活自噬和炎性体形成的下游途径也没有开启,即使 STING 通过其他途径被激活。然而,通过一种不同途径导致的干扰素激活仍然出现了。
麻省理工学院的Rebecca Carlson博士说,“我们第一次能够将这些下游过程解偶联,即我们可以用C53激活干扰素,但抑制导致自噬和炎性体形成的另外两条途径。在 STING 被过度激活的炎症性疾病中,我们如今可以开始探究这些分子机制中哪一个最重要,哪一个对我们看到的表型贡献最大。”
选择性控制
在未来的研究中,这些作者希望利用 C53 来确定这三种途径的相对重要性,并试图找出哪种途径在被刺激或阻断后治疗多种疾病最有用。
美国食品药品管理局(FDA)迄今尚未批准任何 STING 激动剂,尽管目前正在进行多项关于STING 激动剂的临床试验。其他 STING 激动剂未能通过临床试验的一个潜在原因是,这种治疗可能会导致 STING 介导的不必要的细胞死亡。这些作者认为刺激干扰素产生但不刺激细胞死亡或其他炎症途径的药物可能提供一种克服这一障碍的方法。
这些作者希望探索 STING 是否可能对已知由离子通道控制的其他细胞活动的行为产生影响。Carlson说,“既然我们知道 STING 是一种离子通道,我们就可以根据 STING 确实运输质子这一知识,提出我们认为可能产生的其他影响。”(生物谷 Bioon.com)
参考资料:
Bingxu Liu et al. Human STING is a proton channel. Science, 2023, doi:10.1126/science.adf8974.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


