杨森/南京传奇CAR-T疗法获FDA突破性疗法认定 治疗多发性骨髓瘤
来源:药明康德 2019-12-09 12:23
强生集团(J&J)旗下杨森(Janssen)公司宣布,美国FDA授予该公司靶向B细胞抗原(BCMA)的CAR-T疗法JNJ-4528突破性疗法认定,用于治疗经治多发性骨髓瘤患者。突破性疗法认定将加快这一创新疗法的开发和审评过程。JNJ-4528又名LCAR-B38M,是南京传奇公司和杨森公司共同开发的创新CAR-T疗法。多发性骨髓瘤(MM
强生集团(J&J)旗下杨森(Janssen)公司宣布,美国FDA授予该公司靶向B细胞抗原(BCMA)的CAR-T疗法JNJ-4528突破性疗法认定,用于治疗经治多发性骨髓瘤患者。突破性疗法认定将加快这一创新疗法的开发和审评过程。JNJ-4528又名LCAR-B38M,是南京传奇公司和杨森公司共同开发的创新CAR-T疗法。
多发性骨髓瘤(MM)是一种无法治愈的血液癌症,影响骨髓中的浆细胞。癌变的浆细胞迅速增殖扩散,将骨髓中的正常细胞替换为癌细胞。据估计,在2019年,超过32000名患者将被确诊患有MM。MM患者的症状包括骨折或者骨痛,血红细胞计数降低,疲惫、肾脏问题和感染等。
JNJ-4528是一款结构上具有差异性的CAR-T疗法。它的抗体片段中携带两个靶向BCMA的蛋白域。JNJ-4528最初由南京传奇公司设计和开发。在2017年12月,杨森公司与南京传奇达成全球性合作,共同开发和推广JNJ-4528治疗MM患者。在中国,南京传奇与杨森合作开展的2期临床试验CARTIFAN-1,正在招募患者,进一步评估JNJ-4528在治疗晚期复发/难治性MM患者时的疗效。这一疗法已经获得FDA授予的孤儿药资格,以及欧盟EMA授予的PRIME药品认定。
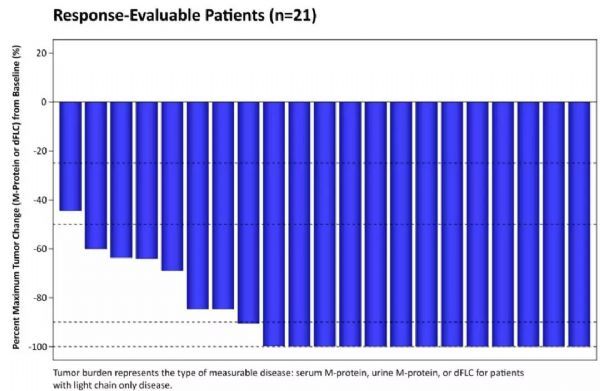
这一突破性疗法认定的授予获得了名为CARTITUDE-1的1b/2期临床试验数据的支持。参加这一开放标签,多中心临床试验的多发性骨髓瘤患者至少接受过3种前期疗法,或者对蛋白酶体抑制剂(PI)和一种免疫调节疗法(IMiD)产生耐药性。它们已经接受过PI,IMiD和抗CD38抗体的治疗,然而疾病继续进展。CARTITUDE-1的初步数据将在本周末开幕的美国血液学会(ASH)年会上公布。ASH会议摘要表明,在能够评估疗效的21名患者中,所有患者的肿瘤负担都有所下降。JNJ-4528达到91%的总缓解率,其中4名患者达到严格完全缓解(stringent complete response),2名患者达到完全缓解,7名达到非常高的部分缓解,6名达到部分缓解。
“突破性疗法认定的授予是我们与南京传奇合作,加速开发这一创新CAR-T疗法进程中的重要里程碑,”杨森研发肿瘤学临床开发副总裁Sen Zhuang博士说:“我们期待与美国FDA紧密合作,推进JNJ-4528的临床开发,最终将这款靶向BCMA的免疫疗法带给需要新治疗选择的多发性骨髓瘤患者。”(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。