Nature:开发出一种计算T细胞的新工具 或能快速预测癌症患者对疗法所产生的反应
来源:本站原创 2021-09-12 23:12
2021年9月13日 讯 /生物谷BIOON/ --免疫微环境会影响肿瘤的进化,其既能预测患者的预后还能预测患者对免疫疗法的反应;然而,对肿瘤浸润性淋巴细胞(TILs)的测定往往会因缺乏合适的数据而受限,DNA的全外显子组测序(WES)经常被用来计算肿瘤的突变负担和识别可操作的突变。近日,一篇发表在国际杂志Nature上题为“Using DNA sequen
2021年9月13日 讯 /生物谷BIOON/ --免疫微环境会影响肿瘤的进化,其既能预测患者的预后还能预测患者对免疫疗法的反应;然而,对肿瘤浸润性淋巴细胞(TILs)的测定往往会因缺乏合适的数据而受限,DNA的全外显子组测序(WES)经常被用来计算肿瘤的突变负担和识别可操作的突变。近日,一篇发表在国际杂志Nature上题为“Using DNA sequencing data to quantify T cell fraction and therapy response”的研究报告中,来自伦敦大学等机构的科学家们通过研究开发了一种新型工具,其或能快速估计癌变肿瘤中免疫T细胞的数量,由于T细胞的丰度能帮助预测患者对免疫疗法所产生的反应,因此研究人员希望这能帮助开发更具靶向性和有效的癌症疗法。
图片来源:https://www.nature.com/articles/s41586-021-03894-5
作为英国癌症研究中心资助的TRACERx研究计划的一部分,本文中,科学家们分析了来自患者癌变肿瘤的DNA测序数据,旨在观察是否能量化样本中的T细胞比例。研究者Nicholas McGranahan教授说道,DNA测序经常在癌症患者机体的肿瘤中进行,以便对患者进行分层并了解其机体的癌症是如何进展的。估算机体中的免疫细胞丰度对于控制癌症非常重要,其会影响患者的生存和指导性疗法的进行,此前研究人员无法仅从DNA测序数据中进行相关推算。
这篇研究报告中,研究人员旨在探索是否能开发一种新方法来直接通过DNA测序阐明免疫细胞,而不需要更多的数据;DNA测序能帮助科学家分析个体机体肿瘤发生的进化史;研究人员利用这种新型工具回顾并计算了T细胞“VDJ重组”的水平,这是T细胞中的一种过程,在该过程中,其能被重组或改变且被赋予工具,从而使其能识别并攻击入侵者。
具体而言,研究人员发现了一种信号,这就揭示了T细胞受体切除环(TRECs)的缺失,而这是T细胞成熟所需要的,其通常在VDJ重组过程中会发生;通过给予这种缺失打分,研究人员就能准确估计出肿瘤中存在的T细胞的数量;这个分数还能被用来预测患者对免疫疗法所产生的反应以及免疫逃逸机制。此外,这种新型评分工具还能应用于从正常血液样本中获得的DNA测序数据,这些血样通常会被收集起来,但截至到现在研究人员还无法对其免疫内容进行系统性地分析。
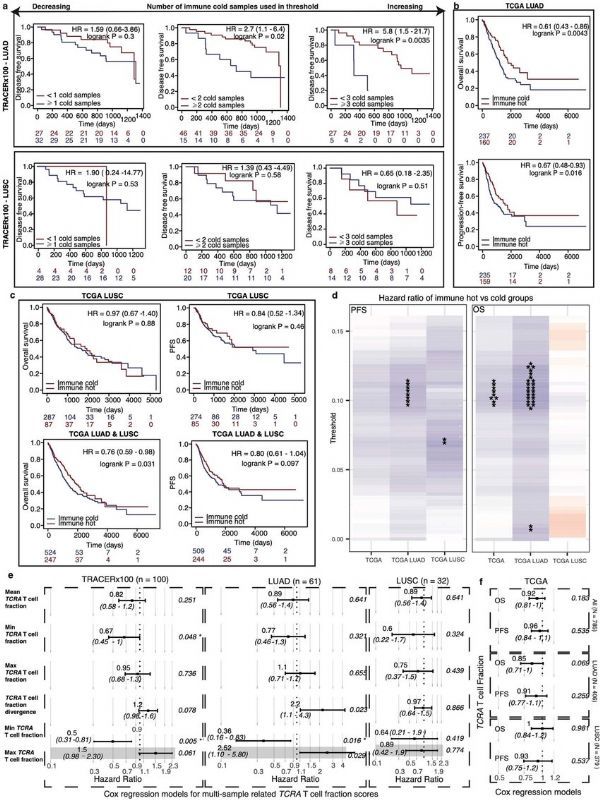
TCRA T细胞分数与预后的关系。
图片来源:Bentham, R., et al. Nature (2021). doi:10.1038/s41586-021-03894-5
近些年来,一种称之为检查点抑制剂(CPIs)的免疫疗法已经成为治疗多种类型癌症的革命性治疗手段,其能通过阻断T细胞所产生的名为检查点蛋白来发挥作用,这些检查点有助于保持机体免疫反应不至于太强,有时能帮助维持T细胞对癌细胞的杀灭能力,当这些检查点被阻断后,T细胞就能更好地杀灭癌细胞。预测免疫疗法可能成功的一种生物标志物就是T细胞的数量,可供CPIs适应的T细胞越多,那么患者机体可摧毁的癌细胞就越多。
研究者Robert Bentham表示,直接从DNA测序中量化T细胞的浸润或能预测患者对疗法的反应,同时还不需要额外的数据;事实上,研究者所开发的方法可以在不增加时间和成本的情况下完成,这或许超出了标准DNA测序的手段;这种新工具还能帮助研究人员更深入地揭示机体免疫系统的奥秘,而并不仅仅是在癌症研究背景下;由于该工具目前只用于研究,下一步研究者还将会进一步对其改造使其也能用于临床中。(生物谷Bioon.com)
原始出处:
Bentham, R., Litchfield, K., Watkins, T.B.K. et al. Using DNA sequencing data to quantify T cell fraction and therapy response. Nature (2021). doi:10.1038/s41586-021-03894-5
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。