HIV二药方案!默沙东islatravir/doravirine 144周数据:疗效媲美三合一复方片Delstrigo(德思卓)!
来源:本站原创 2021-10-28 02:21
islatravir/doravirine在维持病毒学抑制方面,疗效与Delstrigo相似。

2021年10月27日讯 /生物谷BIOON/ --默沙东(Merck & Co)近日在第18届欧洲艾滋病会议(EACS 2021)上公布了一项2b期剂量范围研究(NCT03272347)的144周数据。该研究在先前没有接受过抗逆转录病毒治疗(treatment-naive,初治)的HIV-1成人感染者中开展,正在比较islatravir与doravirine二药方案(伊斯拉曲韦/多拉维林,ISL/DOR)、三合一复方单片Delstrigo(中文商品名:德思卓,通用名:多拉米替片,多拉韦林/拉米夫定/替诺福韦,DOR/3TC/TDF)的抗逆转录病毒活性、耐受性、安全性。
144周数据显示:采用达到HIV-1 RNA水平<50拷贝/毫升(c/mL)的患者比例进行衡量,ISL/DOR维持病毒抑制的疗效与DOR/3TC/TDF相似。数据进一步表征了ISL/DOR二药方案的耐受性和安全性。144周数据是对96周结果和安全性数据的跟进。0.75mg剂量组(选定的3期剂量)中,144周结果与96周结果一致。
islatravir(伊斯拉曲韦,ISL)是默沙东在研的一款新型口服核苷逆转录酶易位抑制剂(NRTTI),用于与其他抗逆转录病毒药物联合治疗HIV-1感染者。doravirine(多拉维林,DOR)已被批准与其他抗逆转录病毒药物联合治疗HIV-1成人感染者:作为单一药物(Pifeltro)和单一片剂方案的组成部分(Delstrigo;DOR/3TC/TDF)。
就在最近,默沙东公布了2项关键3期试验的阳性顶线结果。这2项3期试验在接受不同抗逆转录方案(ART;ILLUMINATE SWITCH A试验)或吉利德三合一药物Biktarvy(BIC/FTC/TAF; ILLUMINATE SWITCH B试验)治疗已实现病毒学抑制的HIV-1成人感染者中开展,评估了一种每日一次口服固定剂量doravirine/islatravir(DOR/ISL)组合片剂的疗效和安全性。结果显示,在治疗第48周,2项试验均达到了主要疗效终点(HIV-1 RNA水平≥50拷贝/mL的患者比例):证实DOR/ISL与ART之间、DOR/ISL与Biktarvy之间的抗病毒疗效相当。迄今为止,试验期间DOR/ISL的安全性和耐受性概况与先前报告的2期研究一致。
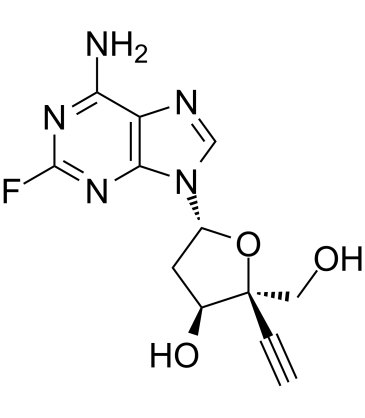
islatravir(MK-8591)化学结构式(图片来源:medchemexpress.cn)
EACS 2021会议上公布的2b期临床试验(NCT03272347)中,先前未接受治疗的HIV-1成人患者被随机分配(1:1:1)到4个每日一次口服治疗组:islatravir 0.25mg(n=29)、0.75mg(n=30)、2.25mg(n=31)联合doravirine(100mg)和3TC(300mg),与DOR/3TC/TDF(n=31)进行对比(第一部分)。在至少治疗24周后,islatravir治疗组HIV-1 RNA<50拷贝/毫升的患者改用由islatravir和doravirine组成的二药方案,不含3TC(第二部分)。islatravir治疗组患者在第60-84周期间过渡到0.75mg islatravir(3期选定剂量)和doravirine治疗,并继续进行联合治疗直至第144周(第3部分)。在第144周,患者将接受选定剂量的islatravir与doravirine固定剂量组合作为开放标签治疗,直到第192周试验结束(第4部分)。
在第144周,根据达到HIV-1 RNA水平<50拷贝/毫升的患者比例进行衡量,在所有剂量水平下,islatravir+doravirine均维持了病毒学抑制:0.25mg、0.75mg、2.25mg剂量组分别有72.4%(n=21/29)、83.3%(n=25/30)、61.3%(n=19/31)维持病毒学抑制。总的来说,合并的islatravir+doravirine组,有72.2%(n=65/90)患者HIV-RNA水平<50拷贝/毫升,与DOR/3TC/TDF组的77.4%(n=24/31)相似。144周内,7例患者符合方案定义的病毒学失败(PDVF)标准(确认的HIV-1 RNA≥50拷贝/毫升)并停止治疗,所有患者的HIV-1 RNA水平均<80拷贝/毫升。没有患者符合临床显著的确认病毒血症标准(HIV-1 RNA≥200拷贝/毫升)或病毒耐药性分析。
安全性方面,在第144周,islatravir+doravirine组、DOR/3TC/TDF组至少发生一次不良事件(AE)的患者比例相似。在第144周,0.25mg、0.75mg、2.25mg剂量islatravir+doravirine组分别有89.7%(n=26/29)、90.0%(n=27/30)、77.4%(n=24/31)的患者出现不良事件。此外,合并的islatravir+doravirine组有85.6%(n=77/90)经历不良事件,DOR/3TC/TDF组为87.1%(n=27/31)。
islatravir+doravirine组与DOR/3TC/TDF组相比最常见的药物相关不良反应为腹泻(1.1%[n=1/90] vs 12.9%[n=4/31])、恶心(3.3%[n=3/90] vs 9.7%[n=3/31])、头痛(2.2%[n=2/90] vs 3.2%[n=1/31]),以及异常梦[2.2%[n=2/90] vs 0%[n=0/31])。在第48周后,islatravir+doravirine组没有额外的患者报告药物相关不良事件。islatravir+doravirine组因药物相关不良事件而停药的比率为2.2%(n=2/90),DOR/3TC/TDF组为3.2%(n=1/31),均发生在第48周之前。islatravir+doravirine组无死亡或严重药物相关不良事件。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


