一项小鼠研究可能发现了预防阿尔茨海默氏症的药物!
来源:本站原创 2021-03-25 23:37
2021年3月25日讯/生物谷BIOON/--虽然65岁以上的人中每14人就有1人患有阿尔茨海默氏症,但阿尔茨海默氏症目前仍无法治愈,也无法干预疾病的发展。但最近的一项研究可能会让我们离预防老年痴呆症更近一步。这项在动物身上进行的试验发现,一种特殊的分子可以防止一种已知会导致大脑中的阿尔茨海默氏症的有毒蛋白质的堆积。
2021年3月25日讯/生物谷BIOON/--虽然65岁以上的人中每14人就有1人患有阿尔茨海默氏症,但阿尔茨海默氏症目前仍无法治愈,也无法干预疾病的发展。但最近的一项研究可能会让我们离预防老年痴呆症更近一步。这项在动物身上进行的试验发现,一种特殊的分子可以防止一种已知会导致大脑中的阿尔茨海默氏症的有毒蛋白质的堆积。
图片来源:Shutterstock
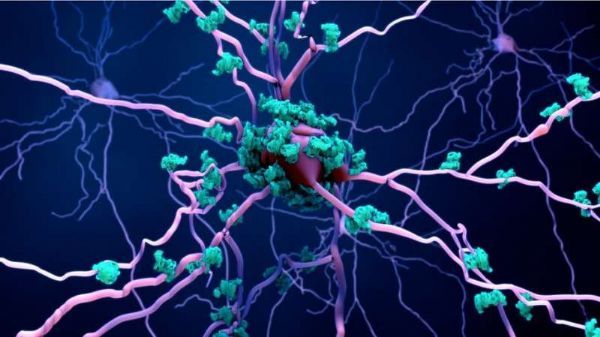
自1906年以来,研究人员已经知道淀粉样蛋白斑块是阿尔茨海默病的病因之一。这些斑块是顽固的粘性沉积物,在我们的大脑中堆积,含有一种叫做β淀粉样蛋白的蛋白质。这种蛋白质一直是许多研究的焦点,我们已经了解了很多关于它的作用和它如何导致神经细胞死亡的知识。
β淀粉样蛋白首先攻击我们神经细胞之间的通讯网络(称为突触),然后使神经细胞窒息。淀粉样蛋白引起的神经细胞损伤是导致阿尔茨海默病症状的原因之一。目前,还没有药物可以改变淀粉样斑块在大脑中积累的数量,或阻止这种积累的发生。
淀粉样蛋白来自一种叫做淀粉样前体蛋白(APP)的蛋白质,这种蛋白质存在于我们的全身,而不仅仅是我们的大脑。APP蛋白家族参与了许多生物功能,包括制造其他蛋白质、控制神经细胞之间的通讯等。
然而,当更大的APP分子被人体分割成更小的碎片时,它们可以采取两条路径。其中一种途径与疾病无关,而另一种途径已被证明会提高β淀粉样蛋白水平。如果我们研究导致阿尔茨海默病的途径,科学家已经发现一种被称为γ分泌酶的酶在将APP转化为β淀粉样蛋白的过程中发挥了关键作用。
科学家们花了很长时间试图瞄准分泌酶,以阻止产生斑块的β淀粉样蛋白的粘性堆积。但是,研究人员在抑制γ分泌酶作用上做的工作在很大程度上失败了,一些试验表明,对其抑制会增加大脑功能衰退的速度。
实验分子
然而,最近的一项研究采用了与过去不同的方法。他们的目标不是关闭γ分泌酶,而是试图降低它的活动。为了做到这一点,研究人员需要产生新的分子来改变伽马分泌酶的活性,并提供保护防止β淀粉样蛋白沉积在大脑中积累。
图片来源:Shutterstock
研究小组生成了三种有趣的化合物,它们在非常低的浓度下就能起效——这对制造新药至关重要。然后,研究人员将这些化合物中的一种带入老年痴呆症的动物模型中进行测试。
为了做到这一点,他们使用了一些被改造成可以产生更多的β淀粉样蛋白的小鼠,从而显示出一些阿尔茨海默氏病的迹象。小鼠在三个月的时间里每天服用这种化合物。结果是大脑中的β淀粉样蛋白减少了一半。尽管其他研究在动物模型中也得出了类似的结果,但这项研究的结果意义重大,因为这种化合物不仅可以用于治疗痴呆,还可以预防它。
他们还注意到,用这种分子处理过的老鼠大脑发生了其他变化。这种分子抑制了大脑免疫细胞——小胶质细胞的反应。尽管这些细胞对大脑健康很重要,但当它们过度活跃时也会有害——阿尔茨海默氏症就是如此。这表明该药物的好处可能是双重的。
下一步是什么?
为了将这种化合物应用于痴呆症患者,下一步即是进行临床试验,以验证实验室的发现。这一步也往往是实验室工作的结论不能起效的地方。
尽管研究人员已经做了大量的研究,让这种化合物有成功的机会,但针对我们大脑的药物的成功率仅约为6%。先前的γ分泌酶调节剂由于参与者报告的不良反应没有进展成为药物。
但这项研究中试验的分子具有更强的效力优势,这最终导致对使用者产生影响所需的分子更少。如果它进入临床试验,研究人员将寻找各种证据来证明一个积极的结果,比如它是否改善了一个人的记忆测试表现。试验还可能涉及大脑扫描,以监测大脑结构变化,跟踪大脑中的β淀粉样蛋白沉积。
虽然从实验室到临床的过渡中许多分子没有达到预期,但这种分子未来发展的迹象是积极的,它确实为试验分子添加了一种新的选择,这是研究人员继续为老年痴呆症患者和等待诊断的人寻求疗法和预防措施的必要条件。(生物谷Bioon.com)
参考文献:
Kevin D. Rynearson, Moorthi Ponnusamy, Olga Prikhodko. et al. Preclinical validation of a potent γ-secretase modulator for Alzheimer’s disease prevention. J Exp Med 5 April 2021; 218 (4): e20202560. doi: https://doi.org/10.1084/jem.20202560
Müller, U., Deller, T. & Korte, M. Not just amyloid: physiological functions of the amyloid precursor protein family. Nat Rev Neurosci 18, 281–298 (2017). https://doi.org/10.1038/nrn.2017.29
Karran E, Mercken M, De Strooper B. The amyloid cascade hypothesis for Alzheimer's disease: an appraisal for the development of therapeutics. Nat Rev Drug Discov. 2011;10(9):698-712. Published 2011 Aug 19. doi:10.1038/nrd3505
Zhang YW, Thompson R, Zhang H, Xu H. APP processing in Alzheimer's disease. Mol Brain. 2011;4:3. Published 2011 Jan 7. doi:10.1186/1756-6606-4-3
Doody RS, Raman R, Farlow M, et al. A phase 3 trial of semagacestat for treatment of Alzheimer's disease. N Engl J Med. 2013;369(4):341-350. doi:10.1056/NEJMoa1210951
Panza F, Frisardi V, Imbimbo BP, et al. REVIEW: γ-Secretase inhibitors for the treatment of Alzheimer's disease: The current state. CNS Neurosci Ther. 2010;16(5):272-284. doi:10.1111/j.1755-5949.2010.00164.x
Study: CNS drugs have lower regulatory success rate, take longer to develop https://www.centerwatch.com/articles/17469
Tartaglia MC, Rosen HJ, Miller BL. Neuroimaging in dementia. Neurotherapeutics. 2011;8(1):82-92. doi:10.1007/s13311-010-0012-2
Kolanko MA, Win Z, Loreto F, et al. Amyloid PET imaging in clinical practice. Practical Neurology 2020;20:451-462.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->