肺癌精准治疗!美国FDA授予DZD9008(sunvozertinib)突破性疗法认定:治疗EGFR外显子20插入突变肺癌!
来源:本站原创 2022-01-31 21:13
DZD9008是一种选择性、不可逆的新型EGFR抑制剂。

2022年01月31日讯 /生物谷BIOON/ --迪哲医药(Dizal Pharmaceutical)近日宣布,美国食品和药物管理局(FDA)已授予DZD9008(Sunvozertinib)突破性疗法认定(BTD):用于治疗先前接受含铂化疗期间或之后病情进展、经检测证实为携带表皮生长因子受体(EGFR)20号外显子插入突变(EGFRex20ins)的局部晚期或转移性非小细胞肺癌(mNSCLC)成人患者。
BTD是FDA的一个新药评审通道,旨在加快开发及审查用于治疗严重或威及生命的疾病、并且有初步临床证据表明与现有治疗药物相比在临床重要终点方面有显著改善的新药。
DZD9008是一种选择性、不可逆的新型EGFR抑制剂。在全球1/2期研究中,DZD9008在先前已接受过治疗的EGFR外显子20插入突变的NSCLC患者中显示了良好的抗肿瘤疗效:确认的客观缓解率(ORR),在200mg剂量水平时为45.5%,在300mg剂量水平时为41.9%(数据截止日期为2021年7月30日)。此外,DZD9008还显示了对脑转移患者或之前接受过EGFR-MET双特异性抗体药物Rybrevant(amivantamab,强生EGFR-MET双特异性抗体疗法)治疗的患者的疗效。DAD9008耐受性良好,不良反应可控制。
迪哲医药由国投创新与阿斯利康于2017年10月合资建立。目前,迪哲医药正在中国、美国、欧盟、日本、澳大利亚、韩国和其他国家和地区进行2期关键临床试验。
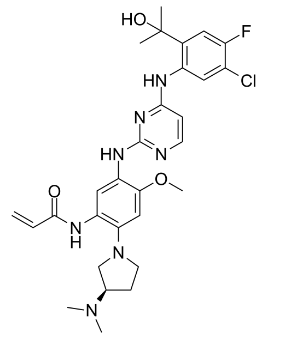
sunvozertinib化学结构式(图片来源:chemsrc.com)
肺癌是全世界癌症死亡的主要原因,非小细胞肺癌(NSCLC)是最常见的肺癌类型,约占肺癌病例的80%-85%。EGFR 20号外显子插入(EGFRex20ins)突变患者仅占所有NSCLC患者的2-3%,预后比其他EGFR突变更差,当前可用的EGFR-TKI和化疗对这类患者的益处有限。
2021年5月和9月,强生EGFR-MET双特异性抗体药物Rybrevant(amivantamab)、武田酪氨酸激酶抑制剂Exkivity(mobocertinib,TAK-788)分别获得美国FDA批准,用于治疗在接受含铂化疗失败后病情进展、携带EGFRex20ins突变的局部晚期或转移性非小细胞肺癌(mNSCLC)成人患者。
值得一提的是,Rybrevant是第一个获监管批准治疗EGFRex20ins突变NSCLC的靶向疗法。Rybrevant的活性药物成分为amivantamab,这是一种全人EGFR-MET双特异性抗体,具有免疫细胞导向活性,靶向携带激活和耐药EGFR及MET突变及扩增的肿瘤。临床数据显示,在接受Rybrevant治疗的患者中,ORR为40%,中位缓解持续时间(DOR)为11.1个月。在病情缓解的患者中,有63%缓解持续时间≥6个月。
Exkivity则是第一个被批准专门选择性靶向EGFRex20ins突变的口服疗法。这是一种新型、强效小分子酪氨酸激酶抑制剂(TKI),旨在高选择性靶向于EGFR和人表皮生长因子受体2(HER2)20号外显子插入突变。在美国和中国,mobocertinib均被授予了治疗携带EGFRex20ins突变NSCLC患者的突破性疗法认定(BTD)。临床数据显示,根据独立审查委员会(IRC)的评估,客观缓解率(ORR)为28%、中位缓解持续时间(DOR)为17.5个月、疾病控制率(DCR)为78%、中位总生存期(OS)为24个月、1年生存率达70%、中位无进展生存期(PFS)为7.3个月,并且在携带各种不同的EGFRex20ins突变NSCLC患者中均观察到了治疗反应。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


