2024年8月Cell期刊精华
来源:生物谷原创 2024-08-30 10:37
甲状腺激素通过重新连接大脑回路来刺激探索的动力、科学家发现油酸竟可恢复健康的阴道微生物组、4年后再发Cell论文,科学家首次提供直接证据表明新型糖偶联物glycoRNA确实存在
2024年8月份即将结束,8月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.甲状腺激素如何变身“探险家”的大脑指挥官?Cell:甲状腺激素通过重新连接大脑回路来刺激探索的动力
doi:10.1016/j.cell.2024.07.041
甲状腺激素在调节人体的代谢、体温、心率以及生长等方面扮演着至关重要的角色。它通过与身体各个器官系统的互动来实现这些功能。尽管甲状腺激素对许多器官的影响已被广泛研究,但其对大脑的具体作用却一直未被完全理解。
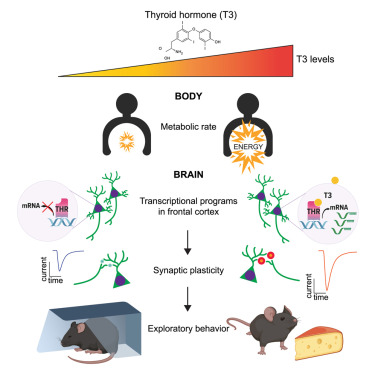
图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.041
如今,在一项新的研究中,来自哈佛医学院的研究人员通过小鼠实验揭示了甲状腺激素对大脑的新见解。研究表明,甲状腺激素可以改变大脑回路,促进探索行为的发生。通过改变大脑回路和代谢率,研究人员发现甲状腺激素能在关键时刻协调大脑和身体的功能,比如在小鼠需要寻找配偶或储备资源的时候。相关研究结果于2024年8月22日在线发表在Cell期刊上,论文标题为“Thyroid hormone remodels cortex to coordinate body-wide metabolism and exploration”。
论文的第一作者,哈佛医学院布拉瓦特尼克研究所的神经生物学研究员Daniel Hochbaum博士指出,甲状腺激素不仅能调节代谢,还能通过直接影响大脑来调节探索行为。
这些发现有助于解释低水平的甲状腺激素为何会导致抑郁状态,表现为探索欲望降低;而高水平的甲状腺激素则可能导致躁狂状态,表现为过度活跃的探索欲望。因此,这项研究为理解甲状腺激素水平异常如何引发某些精神疾病提供了重要线索。
2.全球超一般女性会得的细菌性阴道病有新进展!Cell:科学家发现油酸竟可恢复健康的阴道微生物组
doi:10.1016/j.cell.2024.07.029
全球超过一半的女性在其一生中至少会经历一次细菌性阴道病(BV),这是一种由于生殖道内天然微生物失衡而导致的常见疾病。BV会引起不适的症状,如疼痛和异常分泌物,并且虽然可以通过抗生素治疗,但常常容易复发。若不加以治疗,BV还可能引发孕期并发症,并增加性传播感染(包括HIV)的风险。
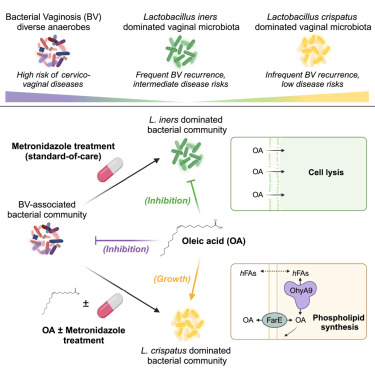
图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.029
在一项新的研究中,来自布罗德研究所、拉根研究所和圣犹大儿童研究医院的研究人员发现,油酸(oleic acid)——人体内最丰富的脂肪酸之一,能在细菌性阴道病实验室模型中恢复阴道微生物的健康平衡。相关研究结果于2024年8月19日在线发表在Cell期刊上,论文标题为“Vaginal Lactobacillus fatty acid response mechanisms reveal a metabolite-targeted strategy for bacterial vaginosis treatment”。
研究结果显示,油酸及其他几种不饱和长链脂肪酸(uLCFA)不仅构成细胞膜的重要部分,还具有抗菌特性,能够抑制与不良健康结果相关的阴道微生物生长,同时促进与健康女性生殖道相关的其他微生物种类的生长。这种促进微生物平衡的治疗方法未来或许可以帮助预防阴道反复感染。
3.4年后再发Cell论文,科学家首次提供直接证据表明新型糖偶联物glycoRNA确实存在
doi:10.1016/j.cell.2024.07.044
在对细胞表面生物学的深入探索中,波士顿儿童医院干细胞与再生生物学助理教授瑞安·弗林(Ryan Flynn)揭示了RNA在细胞外部的惊人功能。Flynn发现某些RNA与细胞表面的复杂碳水化合物——聚糖——通过化学键结合在一起。2021 年,Flynn研究团队首次报告了细胞外也存在RNA的现象(Cell, 2021, doi:10.1016/j.cell.2021.04.023)。
Flynn指出,“这一发现尤其令人兴奋的是,核酸(如RNA)传统上被认为局限于细胞内,与细胞表面的糖类物质在物理上是分离的。”但这一发现对长期以来核酸仅限于细胞内环境的观点提出了挑战,揭示了细胞表面生物学中此前未被认知的复杂性。
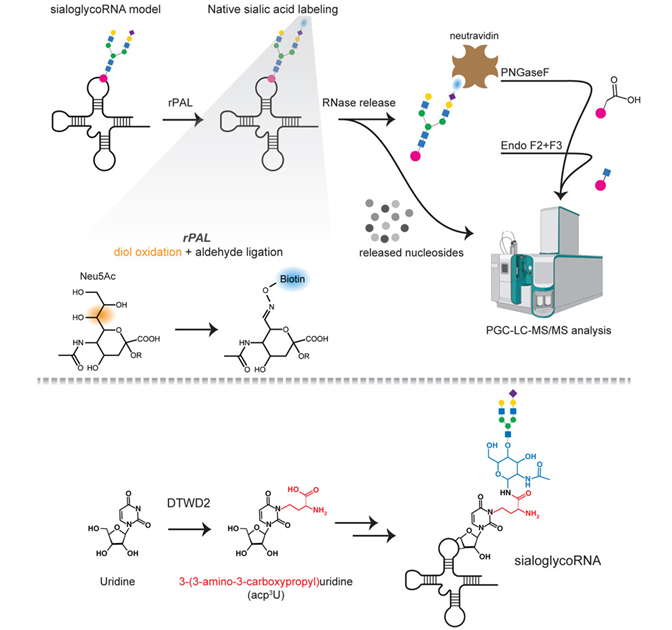
图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.044
在一项新的研究中,Flynn及其同事们发现了 RNA 与 N-聚糖的化学连接机制。在此之前,人们只知道蛋白质和脂质可以与聚糖结合。Flynn团队如今又将 RNA 加入了这一名单,这一发现对于理解细胞生物学具有重要意义。相关研究结果于2024年8月21日在线发表在Cell期刊上,论文标题为“The modified RNA base acp3U is an attachment site for N-glycans in glycoRNA”。
Flynn表示,“我们的研究表明实际上有三类糖偶联物:蛋白质、脂质和RNA。这一发现不仅扩展了已知糖偶联物的种类,而且还为研究这些糖化RNA的功能开辟了新的方向。”
4.伤口愈合背后的‘液态’真相!Cell:皮肤修复过程中的组织液态化对伤口愈合至关重要
doi:10.1016/j.cell.2024.07.031
修复受伤组织的能力对于所有动物来说都是至关重要的生存技能。当身体受伤时,皮肤会通过激活、迁移及分裂皮肤干细胞的方式来完成自我修复。如果人体的伤口愈合机制出现问题,那么就可能导致慢性伤口的发生,带来严重的医疗挑战和巨大的经济成本。
在一项新的研究中,布鲁塞尔自由大学干细胞与癌症实验室主任Cédric Blanpain教授领导的一个研究团队发现:在伤口愈合的过程中,皮肤的物理状态会发生从固态到液态的转变,这种变化对于组织修复极为关键。相关研究结果于2024年8月20日在线发表在Cell期刊上,论文标题为“Dynamic regulation of tissue fluidity controls skin repair during wound healing”。

图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.031
为了深入理解伤口愈合时皮肤物理性质的变化及其背后的分子机制,研究团队采用了包括单细胞水平干细胞行为分析、数学模型建立、生物物理学研究以及功能性实验在内的多种研究手段。通过实时追踪体内单个荧光标记的皮肤干细胞,研究人员观察到,在伤口愈合初期,皮肤表层的物理属性经历了动态调整,变得像液体一样,使得干细胞得以扩散。随后,皮肤组织又逐渐恢复至原有的固态结构,有利于组织的再生与修复。
进一步的分子分析帮助团队识别出了组织修复早期阶段的基因表达模式。他们发现,使用药物干预这些基因活动的不同组成部分,可以显著阻碍伤口愈合过程,并干扰组织从液态向固态的转变。这说明了在伤口愈合过程中,保持固态与液态之间平衡的重要性。
doi:10.1016/j.cell.2024.07.027
人类的肠道内平均含有大约100万亿个细菌,这些微生物为了生存而竞争有限的资源。宾夕法尼亚大学工程与应用科学学院生物工程系助理教授César de la Fuente说:“这是一个非常激烈的环境。所有这些细菌共存的同时也在互相竞争。而这种环境恰恰能够激发微生物产生新的机制。”
在这种冲突中,de la Fuente实验室看到了新抗生素的潜力,如果肠道内的细菌为了生存必须发展出新的策略,那么为什么不利用这些策略来对抗它们呢?
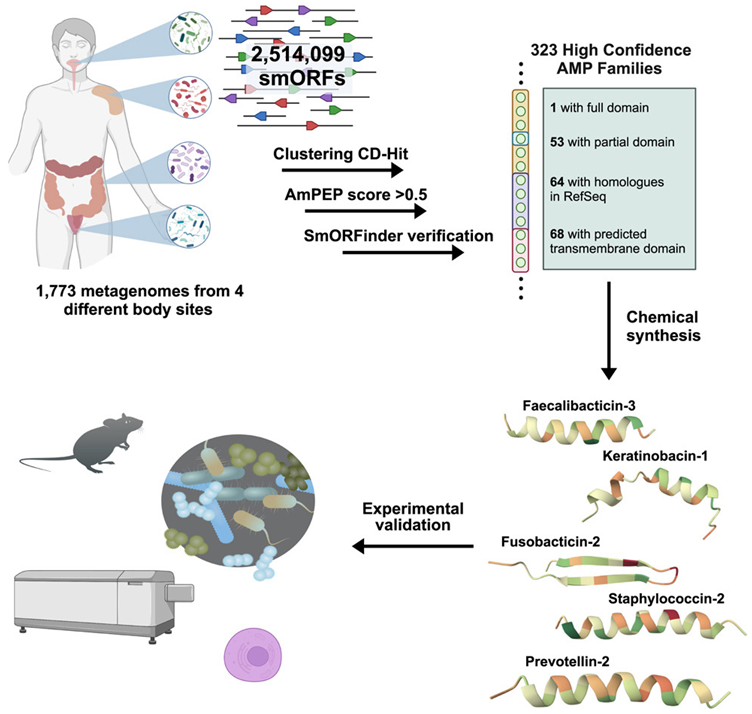
图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.027
在一项新的研究中,de la Fuente实验室和斯坦福大学的Ami S. Bhatt教授对近 2000 人的肠道微生物组(gut microbiome)进行了调查,发现了数十种潜在的新抗生素。相关研究结果于2024年8月19日在线发表在Cell期刊上,论文标题为“Mining human microbiomes reveals an untapped source of peptide antibiotics”。
研究团队专注于肽,即氨基酸短链,这类物质之前被证明有潜力成为新的抗生素。他们通过计算分析了超过40万种蛋白质,利用人工智能读取遗传密码,并通过训练来预测哪些遗传序列可能具有抗菌特性。
当然,这些预测需要通过实验来验证。在筛选出数百种候选抗生素后,研究团队选择了78种进行实际细菌测试。在合成这些多肽之后,他们让细菌培养物接触到每种多肽,并观察哪种肽能成功抑制细菌生长。此外,他们还在动物模型中测试了这些候选抗生素。结果表明超过一半的肽有效,即它们抑制了有益或有害细菌的生长,而主要候选抗生素prevotellin-2的抗感染能力与FDA批准的抗生素多粘菌素B相当,显示出人类肠道微生物组可能蕴藏着未来可用于临床治疗的抗生素。
6.维护表观遗传记忆的关键机制!Cell:揭示Mrc1蛋白能够在DNA复制的滞后链和前导链之间移动组蛋白
doi:10.1016/j.cell.2024.07.017
众所周知,Mrc1(Mediator of Replication Checkpoint 1)是一种在DNA复制过程中扮演重要角色的裂殖酵母蛋白。
最近,由哥本哈根大学的Genevieve Thon教授和Anja Groth教授领导的一项国际合作研究,揭示了有关Mrc1蛋白的新发现。相关研究结果于2024年8月1日在线发表在Cell期刊上,论文标题为“The fork protection complex promotes parental histone recycling and epigenetic memory”。
文章的第一作者之一,Sebastian Charlton博士已经在Thon实验室研究Mrc1多年,他表示:“我们了解到这种蛋白质对于维持细胞中的异染色质状态至关重要,尽管我们已经有一定的理论认识和实验数据,但在分子水平上的验证一直是我们的一个挑战。”
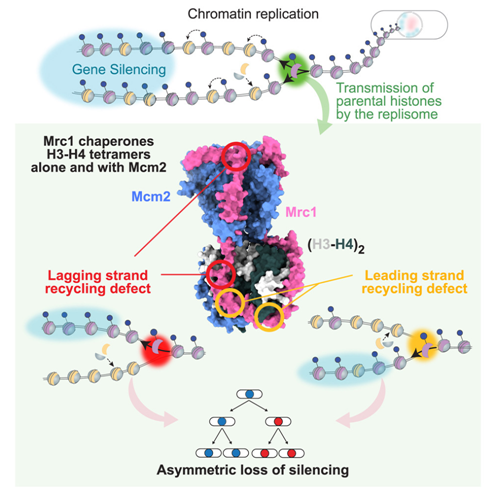
图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.017
为了验证他们的假设,Charlton博士与来自Groth实验室的共同第一作者Valentin Flury博士合作,利用Groth实验室开发的先进基因组学技术。此外,他们还与其他机构的科学家们合作,包括诺和诺德基金会蛋白研究中心的结构生物学家,以及东京都医学科学研究所和胡伯勒支研究所的研究人员。这种跨学科的合作不仅验证了他们的假设,还揭示了Mrc1功能的另一面。
研究团队利用AlphaFold进行结构预测,并通过生化和功能分析验证了Mrc1和Mcm2协作结合H3-H4四聚体的过程。结果显示,Mrc1的特定结构域在组蛋白与Mcm2的连接中起到了关键作用,形成了辅助伴侣蛋白复合物(co-chaperone complex),保证组蛋白在DNA复制过程中正确地分配到滞后链上。
7.Cell:新研究指出在遭受压力时,小鼠大脑会向肠道发送信息,从而减少有益细菌的水平
doi:10.1016/j.cell.2024.07.019
在一项新的研究中,来自美国西奈山伊坎医学院、德国马克斯-普朗克生物控制论研究所、马克斯-普朗克生物研究所和中国广州市第一人民医院等研究机构的研究人员研究了小鼠大脑与小鼠肠道中的十二指肠布氏腺(Brunner's glands,也称为duodenal glands,即十二指肠腺)之间的通讯,发现当小鼠感到压力时,它的大脑会向布氏腺发出信号,导致一种细菌被消灭,从而防止炎症和不必要的免疫反应。相关研究结果于2024年8月8日在线发表在Cell期刊上,论文标题为“Stress-sensitive neural circuits change the gut microbiome via duodenal glands”。
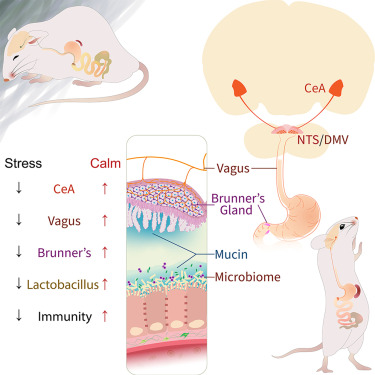
图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.019
他们着重关注了位于小肠壁上的布氏腺。先前的研究已表明,它们的功能是产生粘液,帮助物质通过肠道。但是,由于它们还容纳着许多神经细胞,他们猜测它们还可能发挥更多作用。
他们发现,移除布氏腺会降低抵御细菌感染的能力。这还会导致炎症和免疫化学物质过量产生。他们注意到人类在因肿瘤生长而切除十二指肠腺后也有类似的经历。
他们还发现移除布氏腺会使一种已知能诱导在肠道内壁上形成一道防线从而防止肠道内的不良物质进入血液的蛋白产生的细菌消失。没有了这种细菌,肠壁就会出现渗漏,使不良物质进入血液,从而导致免疫反应,这也会引起炎症。
8.重大进展!中性粒细胞在过敏条件下成为肥大细胞的“猎物”?!Cell:活体显微镜技术的应用,使科学家首次实现实时观察肥大细胞与中性粒细胞间的微妙互动
doi:10.1016/j.cell.2024.07.014
肥大细胞,作为免疫系统中的关键角色,因触发过敏反应而闻名。它们在遭遇过敏原时释放出化学信号,引起诸如肿胀、炎症等典型的过敏症状。
如今,来自马克斯-普朗克免疫生物学与表观遗传学研究所和明斯特大学的研究人员发现了肥大细胞的一个隐藏天赋:它们可以捕获并利用另一种叫做中性粒细胞的免疫细胞。这一惊人发现为人们了解免疫系统,尤其是过敏反应的原理提供了新的思路。相关研究结果于2024年8月2日在线发表在Cell期刊上,论文标题为“Neutrophil trapping and nexocytosis, mast cell-mediated processes for inflammatory signal relay”。
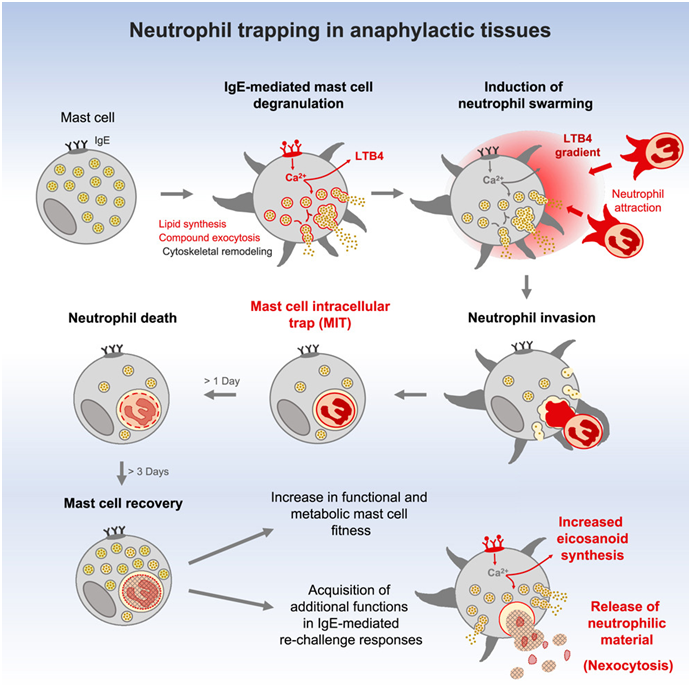
图片来自Cell, 2024, doi:10.1016/j.cell.2024.07.014
肥大细胞,作为组织中的哨兵,蕴藏着丰富的促炎颗粒,是触发炎症反应的核心。当这些细胞感知到威胁,不论是真实的病原体还是误判的过敏原,它们便会释放颗粒中的内容物,引发一系列炎症反应。尤其在某些敏感体质中,即便是日常环境中看似无害的因素,也能激起肥大细胞的过敏警报。目前,肥大细胞与过敏反应部位其他免疫细胞之间的相互作用在很大程度上尚未得到研究。
在本研究中,研究团队利用活体小鼠模型和先进的显微技术,实时观察到了过敏反应中肥大细胞与其他细胞的动态交互。
这一突破性发现由明斯特大学医学生物化学研究所的研究团队于2023年首度揭示,他们惊讶地在肥大细胞内部观测到了中性粒细胞的存在。“我们目瞪口呆,”研究领头人Lämmermann感慨道,“活生生的中性粒细胞竟然躲进了活生生的肥大细胞体内。这一发现超乎寻常,若非借助活体显微镜技术,恐怕难以捕捉到如此微妙的细胞间互动,这充分证明了活体显微镜技术的非凡实力。”
9.三篇Cell:科学家揭示免疫疗法协同作用促进黑色素瘤患者机体中T细胞反应背后的分子机制
doi:10.1016/j.cell.2024.07.018; doi:10.1016/j.cell.2024.07.016; doi:10.1016/j.cell.2024.06.036
近日,发表在国际杂志Cell上的研究报告中,来自匹兹堡大学等机构的科学家们通过研究揭示了靶向作用免疫检查点PD1和LAG3的免疫疗法如何共同发挥作用来激活宿主机体的免疫反应,相关研究结果揭示了为何靶向作用两种检查点的组合性疗法相比仅作用PD1的单一疗法能改善黑色素瘤患者的治疗结局。
在第一项研究中,研究者Vignali等人进行了一项临床试验来调查接受relatlimab、纳武单抗或两种药物的黑色素瘤患者机体的免疫反应。通过分析其血液和肿瘤样本,研究人员发现,相比只接受一种药物治疗的患者而言,接受这两种药物的患者机体中CD8+ T细胞的反应会增强,这与改善其机体癌症杀伤效能直接相关,尽管细胞保留了耗竭的特征。
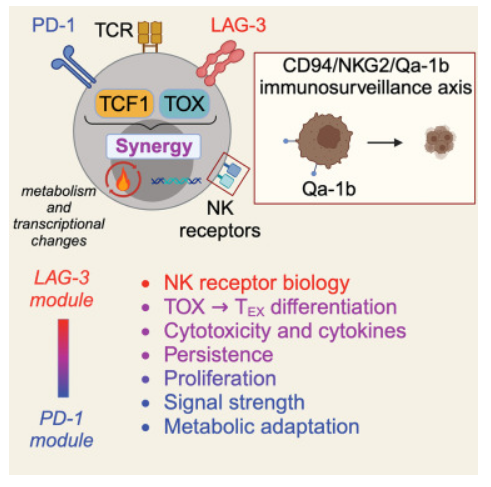
科学家揭示免疫疗法协同作用促进黑色素瘤患者机体中T细胞反应背后的分子机制
图片来源:Cell (2024). DOI:10.1016/j.cell.2024.07.018
在第二项研究中,研究人员利用经过遗传工程化改造的小鼠进行研究,以便其机体中CD8+ T细胞并不会产生PD1、LAG3或两者兼有。在黑色素小鼠模型中,相比缺乏PD1或LAG3的T细胞相比,缺乏两种免疫检查点的T细胞会增强对肿瘤的清除并改善小鼠的生存率,这就增强了临床试验的结果,此外,研究人员还揭示了PD1和LAG3如何协同作用从而阻碍机体抗肿瘤免疫力背后的分子机制。
发表在Cell杂志上的另一项研究中,研究者Vignali作为其中的合作者,他们所得到的研究结果与上述研究结果一致,同时还提供了关于LAG3和PA1如何以不同的方式促进T细胞耗竭的新见解。综上,这三篇研究报告提供了LAG3和PD1如何单独发挥功能以及联合作用背后的分子机制,并强调了利用其进一步进行临床研发的新机会。
10.Cell:揭示OLAH酶驱动人类致死性呼吸道病毒感染疾病背后的分子机制
doi:10.1016/j.cell.2024.07.026
呼吸道感染对于一些人群而言是严重的,甚至是致命性的,但对于其他人而言却不是。近日,一篇发表在国际杂志Cell上题为“High expression of oleoyl-ACP hydrolase underpins life-threatening respiratory viral diseases”的研究报告中,来自墨尔本大学等机构的科学家们通过研究揭示了致命性呼吸道病毒感染背后的早期分子驱动因素。
研究者表示,油酰-ACP-水解酶(OLAH,Oleoyl-ACP-hydrolase)是一种主要参与脂肪酸代谢的特殊酶类,其会驱动严重的疾病后果。由于多种原因,OLAH在机体免疫应答中的重要作用目前尚未被研究人员认识到,包括在健康组织中缺乏明显的表达以及很难在感染前后反映OLAH的表达情况;这项研究中,研究人员将多年间跨越多种疾病的合作项目整合在一起创建了理解OLAH如何发挥作用所需的综合性数据集。
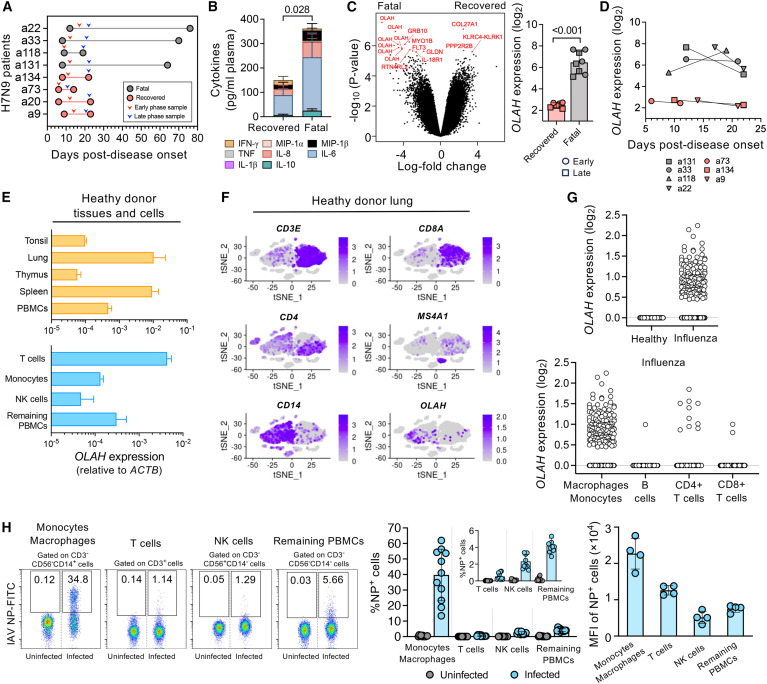
揭示OLAH酶驱动人类致死性呼吸道病毒感染疾病背后的分子机制
图片来源:Cell (2024). DOI:10.1016/j.cell.2024.07.026
研究者Jeremy Chase Crawford说道,OLAH直接影响多种全球相关但不同病毒感染的疾病的严重程度,我们从禽流感这种非常具体的疾病背景开始,但通过形成这些合作我们就能为这种生物学机制揭示更为广泛的疾病背景。第一个指向OLAH作为致死性疾病驱动因素的线索来自于对H7N9禽流感的研究,转录组学分析将OLAH的表达与患者入院后早期致死性H7N9感染联系了起来,如果患者的疾病进展到致死性阶段,那么其机体中的OLAH水平仍然会很高。
研究者表示,从感染中恢复的患者在住院期间机体中的OLAH水平较低,这一发现或许就能扩大其合作,从而在经历感染的患者及疾病小鼠模型的多种不同队列中寻找OLAH的表达。通过多年间对不同患者队列的研究,研究人员从几个不同的项目中生成了转录组学数据集,OLAH的发现就是研究人员开始看到不同疾病之间惊人的关联。基于本文研究,研究人员指出,在患有危及生命的季节性流感、SARS-CoV-2、呼吸道合胞病毒和多系统炎性综合征的患儿机体中的OLAH的表达水平较高,但在轻度疾病中则没有;对小鼠模型的进一步研究结果表明,在不表达OLAH的小鼠模型中,原本致命的感染实际上能让小鼠存活下来。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


