和黄医药第二个药物面市在即!
来源:新浪医药新闻 2019-12-14 19:56
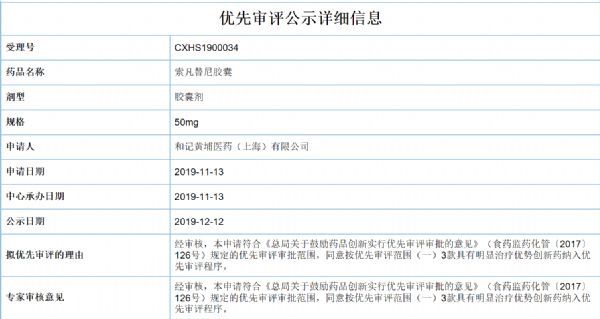
2019年12月12日,国家药品监督管理局药品审评中心(CDE)官网公示,和记黄埔医药(上海)有限公司(简称“和黄医药”)的索凡替尼(Surufatinib)被纳入拟优先审评品种,这是和黄医药第二个即将获批上市的产品。索凡替尼是一种新型的口服抗血管生成-免疫调节激酶抑制剂,可选择性抑制参与肿瘤血管生成和免疫逃逸的血管内皮生长因子受体(VEGFR)、成纤维细胞
2019年12月12日,国家药品监督管理局药品审评中心(CDE)官网公示,和记黄埔医药(上海)有限公司(简称“和黄医药”)的索凡替尼(Surufatinib)被纳入拟优先审评品种,这是和黄医药第二个即将获批上市的产品。
索凡替尼是一种新型的口服抗血管生成-免疫调节激酶抑制剂,可选择性抑制参与肿瘤血管生成和免疫逃逸的血管内皮生长因子受体(VEGFR)、成纤维细胞生长因子受体(FGFR)和集落刺激因子-1受体(CSF-1R)这三种关键酪氨酸激酶的活性。其中,对VEGFR信号通路和FGFR信号通路的抑制作用可以阻止血管生成及肿瘤周围脉管系统的生长,从而使肿瘤缺乏迅速生长所需的营养和氧气;而对CSF-1R信号通路的抑制作用,则可调节肿瘤相关巨噬细胞,促进机体对肿瘤细胞的免疫应答。
索凡替尼研发历程回顾:
2009年6月申报临床;
2019年6月SANET-ep三期临床因提前达到主要研究终点而终止;
2019年11月13日提交NMPA上市申请;
2019年11月21日被FDA授予孤儿药资格;
2019年12月12日被CDE纳入拟优先审评名单。
作为和黄医药自主研发的抗肿瘤新药,索凡替尼从一个化学式到如今走了近10年。2009年6月9日索凡替尼获得第一个临床受理号CXHL0900178,2019年6月15日和黄医药宣布以晚期非胰腺神经内分泌瘤为适应症的III期临床研究(SANET-ep)成功达到主要临床终点无进展生存期(PFS),提前终止研究。近日索凡替尼也是喜讯频传,11月13日上市申请获受理;11月21日被美国FDA授予孤儿药资格,用于治疗胰腺神经内分泌肿瘤;再到日前拟被纳入优先审评名单。
目前,索凡替尼除了针对晚期胰腺神经内分泌瘤的III期临床(CTR20150737)和晚期非胰腺神经内分泌瘤III期临床(CTR20150760),还有一项针对二线胆道癌的III期临床(CTR20181945)也已进入受试者招募阶段。此外,和黄医药还启动了一项Surufatinib联合特瑞普利单抗治疗晚期实体瘤的II期临床研究(CTR20191865),开启了索凡替尼联合免疫治疗的探索。
和黄医药官网显示,截止2019年9月30日,其研发管线有8项产品,包括Savolitinib (c-MET抑制剂)、Fruquintinib (VEGFR 1/2/3抑制剂)、Surufatinib、HMPL-523(Syk抑制剂)、HMPL-689(PI3Kδ抑制剂)、Epitinib (EGFR抑制剂)、Theliatinib (EGFR抑制剂)、HMPL-453(FGFR1/2/3抑制剂)。其中,Fruquintinib(呋喹替尼)作为和黄医药第一个上市的产品,于2018年9月4日获NMPA批准上市,用于治疗转移性结直肠癌,前不久通过医保谈判成功入选2019版医保模板乙类范围。
此次索凡替尼被纳入拟优先审评品种,将加速打破其依靠呋喹替尼单一品种的困局,未来的盈利能力得到了保障。 (生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->