两篇Science子刊:治疗实体瘤的智能细胞疗法出炉
来源:本站原创 2021-05-10 06:57
2021年5月10日讯/生物谷BIOON/---抗击癌症的免疫疗法对许多患者来说是一种拯救生命的进步,但是这种方法只对少数类型的恶性肿瘤有效,对大多数患有实体瘤的癌症患者来说,几乎没有治疗选择。如今,在两项新的研究中,来自美国加州大学旧金山分校的研究人员展示了如何设计能够有效地对抗实体瘤的智能免疫细胞,从而为治疗长期以来无法用免疫疗法治疗的一系列癌症打开了大
2021年5月10日讯/生物谷BIOON/---抗击癌症的免疫疗法对许多患者来说是一种拯救生命的进步,但是这种方法只对少数类型的恶性肿瘤有效,对大多数患有实体瘤的癌症患者来说,几乎没有治疗选择。如今,在两项新的研究中,来自美国加州大学旧金山分校的研究人员展示了如何设计能够有效地对抗实体瘤的智能免疫细胞,从而为治疗长期以来无法用免疫疗法治疗的一系列癌症打开了大门。相关研究结果近期发表在Science Translational Medicine期刊上,论文标题分别为“SynNotch-CAR T cells overcome challenges of specificity, heterogeneity, and persistence in treating glioblastoma”和“SynNotch CAR circuits enhance solid tumor recognition and promote persistent antitumor activity in mouse models”。


通过将基本的计算能力“编程”到旨在攻击癌症的免疫细胞(T细胞)中,这些作者已经克服了一些主要障碍,这些障碍至今仍使这些策略无法进入临床。这两篇新论文显示,由此产生的“智能”疗法比以前的方法更精确、更灵活、更彻底,而且这种方法可能在不久的将来就可以进行临床试验。
胶质母细胞瘤是一种影响成人和儿童的最具侵略性的脑癌,由于这种肿瘤的复杂性,医生们还没有用免疫疗法成功地加以治疗。在第一篇论文中,这些作者在胶质母细胞瘤中测试了这种新的系统。他们发现,它采用两步法猎杀癌细胞,可以完全清除小鼠大脑中的人类患者来源的肿瘤,没有危险的副作用,也没有目前与实体瘤免疫治疗有关的高复发风险。
在第二篇论文中,这些作者发现这种系统的组分可以像可更换的螺丝刀的头一样被换掉,以靶向身体其他部位中难以治疗的癌症。他们还确定了一套特别重要的“螺丝刀头(screwdriver heads)”,它们可以成为对付卵巢癌、肺癌和其他器官癌症的有力工具。
此外,这两篇论文都解决了所谓的“T细胞衰竭(T-cell exhaustion)”问题,这是一个长期存在的挑战,即传统的CAR-T细胞---在一些最有前途的癌症免疫疗法背后,通过重新编程来寻找入侵者的T细胞---在与癌症进行长期的斗争时疲惫了。由此产生的新型智能细胞在整个战斗过程中始终保持强大,在不直接与癌症打交道时,通过切换到待机模式来保存能量。这些发现解决了所有一直阻碍着为患有这些癌症的患者开发免疫疗法的关键挑战。这种新策略已经准备好向临床试验迈进。
将免疫疗法扩展至致命的脑癌
胶质母细胞瘤是一种特别悲惨的癌症,到目前为止,患者还无法从CAR-T细胞中获益。每年,美国有超过2万名成年人被诊断为胶质母细胞瘤或其他类型的恶性脑癌,而在目前的治疗方法下,这些癌症的预后是很糟糕的。脑瘤也是儿童癌症相关死亡和发病的主要原因。这些作者希望能改变这种状况。
以前的研究工作已经确定了一种经常在胶质母细胞瘤细胞表面上发现的分子,这让科学家们希望CAR-T细胞能够靶向这种分子,从而清除这种致命的癌症。尽管这种策略在杀死一些胶质母细胞瘤细胞方面很有效,但是并非所有胶质母细胞瘤细胞都显示这种分子。这使得一些癌细胞能够躲避CAR-T细胞疗法,并最终导致癌症复发。
靶向其他分子会带来相反的但同样危险的问题。虽然有些分子存在于胶质母细胞瘤细胞表面上,但它们也存在于健康的非脑组织(比如肝脏、肾脏、食道和生殖器官)表面上。用CAR-T细胞靶向显示这些分子的细胞,可能会损害健康组织并使患者处于危险之中。这个问题让临床医生没有一种理想的分子靶点,这个普遍存在的问题阻碍了CAR-T在大多数实体瘤中的应用。
这些作者通过采用一种名为synNotch的系统为这个问题设计了一种可定制的解决方案。synNotch系统可以让科学家们对CAR-T细胞进行编程,使之检测在癌细胞表面上发现的特定分子,从而确保CAR-T细胞只有在遇到它们靶向的分子时才会攻击癌细胞。
为了杀死胶质母细胞瘤,这些作者采取了一种新颖的两步法。第一步使用第一组synNotch使CAR-T细胞有能力仔细判断它们靶向的分子是否在肿瘤中,而不是在身体的其他部位,而第二组synNotch确保强大和全面的肿瘤杀伤反应。一旦CAR-T细胞确认它们靶向的分子在肿瘤中,第二组synNotch就会被激活,使CAR-T细胞能够根据多种脑瘤分子检测并杀死胶质母细胞瘤细胞。这个两步过程导致了更彻底的肿瘤杀伤,并防止肿瘤细胞积累简单的使它们能够逃避CAR-T细胞的突变。
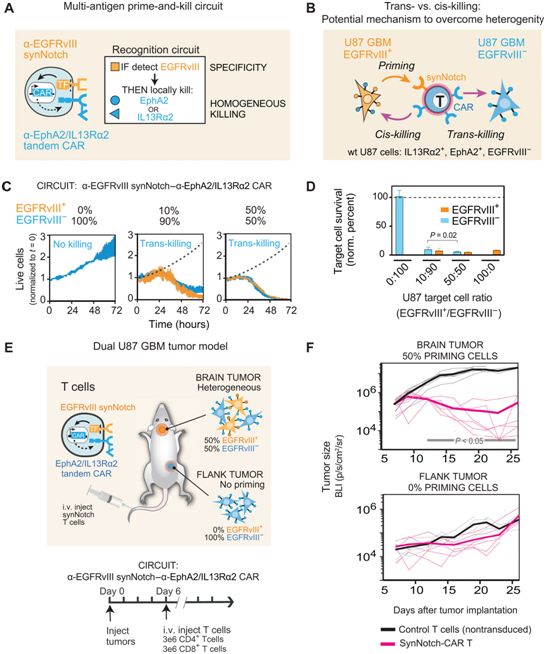
T细胞中的多抗原prime-and-kill回路提供了一种克服抗原异质性同时仍然保持较高的肿瘤特异性的总体策略。图片来自Science Translational Medicine, 2021, doi:10.1126/scitranslmed.abe7378。
第一篇论文中描述的实验表明,这种策略是有效的。在患有人类患者来源的胶质母细胞瘤的小鼠中,synNotch CAR-T细胞消灭了正常T细胞或传统CAR-T细胞无法清除的肿瘤,而且没有危险副作用的迹象。
这些作者表示,他们应该把这些细胞看成是计算机--足够聪明,能够整合多个数据点并做出复杂的选择。如今,他们观察到这在一种对成人和儿童都非常致命的癌症的真实世界模型中发挥作用。
SynNotch是一种灵活、强大的系统,用于构建更聪明的免疫疗法
第二篇论文通过为synNotch系统确定额外的分子靶标,进一步证明了这种方法的有效性。这些作者搜索了公共癌症数据库,以便寻找在肿瘤细胞中发现的在靶向当前难治性疾病的CAR-T疗法中可能是有用的的分子。他们发现了一种叫做ALPPL2的分子,它在许多形式的癌症中都很常见,包括石棉驱动的间皮瘤以及卵巢、胰腺和睾丸恶性肿瘤。重要的是,该分子很少在健康组织中发现。
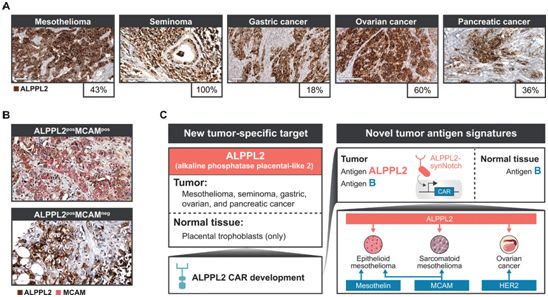
ALPPL2是一种特异性高、应用广泛的肿瘤抗原,可与synNotch CAR-T细胞联合识别实体瘤。图片来自Science Translational Medicine, 2021, doi:10.1126/scitranslmed.abd8836。
在对设计用于检测ALPPL2的synNotch的测试中,CAR-T细胞能够精确地识别并杀死间皮瘤和卵巢癌细胞。这些作者表示,这是一种完全可行的临床级抗原,他们可以用来构建用于人体的细胞疗法。
这两篇论文的一个引人注目的发现是,synNotch CAR-T细胞在整个杀癌过程中保持了稳定的活性水平,消除了T细胞衰竭的挑战,而这种衰竭阻碍了传统的CAR-T疗法。这些作者认为,T细胞衰竭的发生是因为传统的CAR-T细胞经设计后持续表达一种杀伤开关,这意味着它们总是处于开启状态,并最终耗尽其资源,导致这些细胞没有做太多事情。
这些作者发现,令人惊讶的是,他们的synNotch系统并不是这样的。他们发现,synNotch CAR-T细胞一直处于待机状态,保存它们的能量,直到它们识别出癌症。这两篇论文显示,基于多种原因,这些synNotch T细胞可能比目前最先进的CAR-T细胞技术表现更好。(生物谷 Bioon.com)
参考资料:
Joseph H. Choe et al. SynNotch-CAR T cells overcome challenges of specificity, heterogeneity, and persistence in treating glioblastoma. Science Translational Medicine, 2021, doi:10.1126/scitranslmed.abe7378.
Axel Hyrenius-Wittsten et al. SynNotch CAR circuits enhance solid tumor recognition and promote persistent antitumor activity in mouse models. Science Translational Medicine, 2021, doi:10.1126/scitranslmed.abd8836.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


