Nature:科学家发现一种能调节机体脊髓损伤后疤痕形成的特殊通路
来源:生物谷原创 2024-10-02 12:33
本文研究中,研究人员提出了一种旁分泌信号通路,其中能表达同源配体前啡肽的邻近细胞群或能通过释放κ-阿片样物质来刺激脑脊液接触神经元并抑制室管膜的增殖。
当脊髓发生损伤后,附近的细胞会快速行动,在受损区域周围形成保护性疤痕组织从而发挥稳定和保护的作用;但随着时间推移,过多的疤痕就会阻断神经组织再生,从而阻碍愈合过程并导致永久性的神经损伤、感觉丧失或瘫痪。近日,一篇发表在国际杂志Nature上题为“Endogenous opioid signalling regulates spinal ependymal cell proliferation”的研究报告中,来自加利福尼亚大学等机构的科学家们通过研究揭示了一种很少被研究的细胞类型如何控制脊髓损伤中疤痕组织的形成,通过对小鼠进行研究后,研究者发现,激活这些细胞中一种特殊的分子通路或许能让其控制脊髓疤痕的水平。
研究者David Julius博士说道,通过阐明脊髓疤痕形成背后的基本信号生物学特性,或许有望未来一天能从药理学角度微调疤痕形成的程度。脊髓损伤往往是由诸如交通事故、跌倒或运动碰撞等身体创伤所引起的,其会损伤沿脊髓延伸的神经组织,这些神经负责协调大脑和机体其它部位之间的信息传递,目前的疗法主要围绕外科手术和支架来稳定脊柱,利用药物来控制机体疼痛和肿胀,同时还辅助使用物理疗法。
研究者Julius及其同事研究了一组鲜为人知的神经元的功能,即脑脊液接触神经元(cerebrospinal fluid contacting neurons),这些神经元能沿着贯穿脊髓中心的中空通道被发现,其能延伸到填充通道的脊髓液中。随后研究人员开发了一种新方法来标记这些神经元,他们分离到了这些神经元并测定细胞中哪些基因处于活跃状态,结果发现,细胞能表达一种感知κ-阿片样物质的受体,κ-阿片样物质是人类机体自然产生的物质。随后研究人员继续识别能产生κ-阿片样物质的脊髓细胞,并揭示了这些分子是如何激发脑脊液接触神经元的功能的。进一步的实验结果表明,当发生脊髓损伤后,通过这些κ-阿片样物质的信号传导将会减少,从而就会将附近的细胞转化为疤痕组织从而产生保护效应。
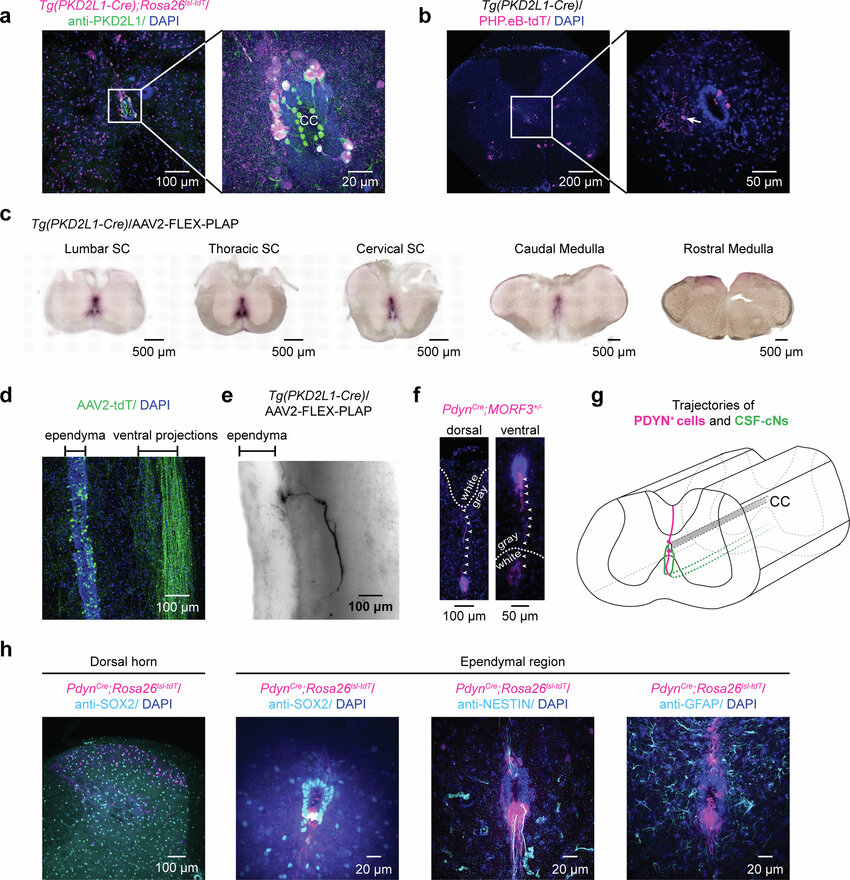
科学家发现一种能调节机体脊髓损伤后疤痕形成的特殊通路
图片来源:Nature (2024). doi:10.1038/s41586-024-07889-w
这项研究中,研究人员尝试给小鼠喂食κ-阿片样物质,结果发现,小鼠机体的疤痕组织减少了,但其脊髓损伤或许更严重了,这些小鼠机体的运动协调能力也并没有恢复。Wendy Yue博士指出,κ-阿片样物质或许能给我们提供一种方法,当发生脊髓损伤后,其会从药理学角度调节产生足够疤痕组织和过度疤痕组织形成之间的微妙平衡。
重要的是,κ-阿片样物质与诸如羟考酮(oxycodone)和氢可酮(hydrocodone)等商业化的阿片样药物不同,其通常并不会让人上瘾。科学家们必须进行更多的研究来理解为何κ-阿片样物质的水平会在机体脊髓损伤后下降,以及支持最佳愈合的疤痕的理想水平到底是多少,当然在脊髓损伤患者机体中测试κ-阿片样物质之前,研究人员还需要进一步进行临床前的研究。研究者Julius指出,这项新的研究发现强调了研究多种细胞类型和信号分子发挥作用及机理的基础科学研究的重要性;我们并不是在寻找控制脊髓愈合的方法,而是我们对这种神秘的细胞类型提出了疑问,随后还发现了一种既有趣而又具有治疗潜能的特殊生物学机制。
综上,本文研究中,研究人员提出了一种旁分泌信号通路,其中能表达同源配体前啡肽的邻近细胞群(PDYN+ cells)或能通过释放κ-阿片样物质来刺激脑脊液接触神经元并抑制室管膜的增殖,这或许就揭示了一种能调节脊髓损伤后疤痕形成的内源性机制和潜在的药理性策略。(生物谷Bioon.com)
参考文献:
Yue, W.W.S., Touhara, K.K., Toma, K. et al. Endogenous opioid signalling regulates spinal ependymal cell proliferation. Nature (2024). doi:10.1038/s41586-024-07889-w
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


