Devel Cell:科学家揭示通过Kras癌基因介导的驱动肿瘤形成的分子机制
来源:本站原创 2022-02-12 23:51
来自杜克大学等机构的科学家们通过研究就解答了上述问题,研究者发现,Kras突变会促进细胞内的染色质重排,这种重排会促进组织细胞恢复到早期发育或者干细胞样的状态,并会错误地开始再生新生组织,从而引发肿瘤。
2022年2月13日 讯 /生物谷BIOON/ --癌症是由快速生长且形状异常的细胞所组成的,其能够渗透并破坏健康组织,并能游走到机体的其它部位中同时形成更多的肿瘤组织;部分原因是其快速和侵入性的特征,目前癌症仍然是美国人群死亡的第二大主要原因,同时也是全球人群死亡的主要原因。肿瘤的形成往往是由名为癌基因的基因所驱动的,这些基因通常主要参与了细胞生长、增殖和死亡的正常过程,但其也会发生突变并高水平表达,从而就能驱动癌细胞的增殖。
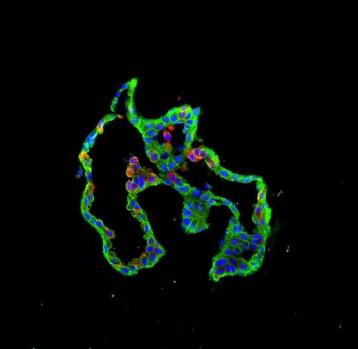
科学家揭示通过Kras癌基因介导的驱动肿瘤形成的分子机制。
图片来源:Duke University, Developmental Cell
突变的癌基因往往能以多种方式发挥作用,包括靶向作用细胞的染色质、DNA紧凑密集的结构以及选定的蛋白质分子;癌基因还能与多种多样的蛋白质复合体一起发挥作用,这些复合体能通过结合到DNA的特定区域上来关闭或开启特定基因的表达。Kras是一种最著名的癌基因,突变的Kras在大约20%的人类癌症中都存在,包括97%的胰腺导管癌、45%的结直肠癌和30%的肺癌等。
尽管近年来科学家们重点研究了Kras突变的肿瘤的形成机制,但关于Kras突变为何对癌变如此重要依然是科学家们需要一直研究的问题;传统观点认为,Kras突变只会促进细胞的增殖,然而,由于很多基因能促进细胞的增殖,那么到底是什么样的机制能让Kras如此致命且难以治疗呢?近日,一篇发表在国际杂志Developmental Cell上题为“Epigenetic basis of oncogenic-Kras-mediated epithelial-cellular proliferation and plasticity”的研究报告中,来自杜克大学等机构的科学家们通过研究就解答了上述问题,研究者发现,Kras突变会促进细胞内的染色质重排,这种重排会促进组织细胞恢复到早期发育或者干细胞样的状态,并会错误地开始再生新生组织,从而引发肿瘤。
研究者发现,Kras所诱导的染色质的重塑是一种由名为AP-1的蛋白复合体所介导的,该复合体能结合并打开染色质从而重新构建细胞的命运;AP-1所介导的染色质的可及性机制似乎是肿瘤开启的常见过程,包括肺部、皮肤和肠道等,研究者指出,抑制AP-1的小分子药物或能阻断癌基因的表达和细胞增殖,从而就能提供一种治疗Kras突变肿瘤的有潜力的方法,这一点尤为重要,因为目前大部分的Kras肿瘤是无法利用药物来治疗的。

图片来源:https://www.cell.com/developmental-cell/fulltext/S1534-5807(22)00006-5?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS1534580722000065%3Fshowall%3Dtrue
然而,更吸引人的是,Kras/AP-1诱导的染色质重塑或许会被灌注一定的可塑性,或者会拥有对突变做出反应的不同细胞特征的能力,因此,来自不同来源的Kras突变细胞(比如肺部中的肺泡细胞和气道中的细胞)就会开始掩盖其细胞身份并变得彼此相似,这或许就为阐明肺癌的起源提供了新的线索和思路。研究者Shen博士说道,本文研究阐明了Kras或能利用遗传重编程来使得细胞更具有干细胞样特征或可塑性,这就解决了长期以来研究人员关于Kras在肿瘤形成中为何如此特殊的争论,研究人员揭示了AP-1复合体作为染色质重塑的效应子或有望帮助开发靶向作用Kras的治疗性策略,Kras是一种非常难以靶向作用的靶点。
理解参与肿瘤形成的复杂过程对于设计新型药物疗法并进行癌症平台的筛选至关重要;综上,本文研究结果表明,肿瘤或能通过细胞类型特异性的转录因子来保留其原始细胞的表观遗传学记忆,而且一种跨组织的依赖保守AP-1的染色质重塑程序或能调节癌症的发生。(生物谷Bioon.com)
原始出处:
Preetish Kadur Lakshminarasimha Murthy,Rui Xi,Diana Arguijo, et al. Epigenetic basis of oncogenic-Kras mediated epithelial-cellular proliferation and plasticity, Developmental Cell (2022). DOI:10.1016/j.devcel.2022.01.006
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


