2019年12月Cell期刊不得不看的亮点研究
来源:本站原创 2019-12-31 23:36
2019年12月31日讯/生物谷BIOON/---2019年12月份即将结束了,12月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。1.Cell:经过基因改造的大肠杆菌也可通过摄入空气中的二氧化碳进行生长doi:10.1016/j.cell.2019.11.009在一项新的研究中,来自以色列魏茨曼科学研究所的研究人员对大肠杆菌进行
2019年12月31日讯/生物谷BIOON/---2019年12月份即将结束了,12月份Cell期刊又有哪些亮点研究值得学习呢?小编对此进行了整理,与各位分享。
1.Cell:经过基因改造的大肠杆菌也可通过摄入空气中的二氧化碳进行生长
doi:10.1016/j.cell.2019.11.009
在一项新的研究中,来自以色列魏茨曼科学研究所的研究人员对大肠杆菌进行基因改造,使得它们通过吸收二氧化碳就可以生长。相关研究结果近期发表在Cell期刊上,论文标题为“Conversion of Escherichia coli to Generate All Biomass Carbon from CO2”。
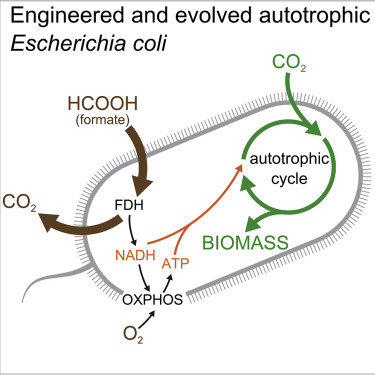
大肠杆菌通常是异养生物(heterotroph),即摄入葡萄糖等有机化合物作为食物的有机物,但是这项新的研究表明它们可以转化为自养生物(autotroph),从大气中吸收二氧化碳并将它转化为生物量(biomass)。
美国加州大学伯克利分校生物化学家Dave Savage(未参与这项新的研究)说,“我发现一种经过数十亿年进化进行异养生活的有机体能够如此快速地和彻底地转变成自养生物,这实在是太神奇了。这表明代谢极具可塑性。”
2.两篇Cell从结构上揭示牛痘病毒增殖机制,有望开发出更好地用于治疗癌症的病毒载体
doi:10.1016/j.cell.2019.11.024; doi:10.1016/j.cell.2019.11.023
为了让病毒增殖,它们通常需要被感染细胞的支持。在许多情况下,在感染附近的其他细胞之前,只有在宿主细胞的细胞核中才能找到它们复制它们自己的遗传物质所需的分子。但是并非所有病毒都能进入细胞核中。一些病毒停留在细胞质中,因此必须能够独立地复制它们的遗传物质。为此,它们必须带上它们自己的“加工零件”。在这个过程中起关键作用是一种由各种亚基组成的特殊酶---RNA聚合酶---完成的。这种酶从病毒基因组中读取遗传信息,并将它转录为信使RNA(mRNA),并利用mRNA作为基因组中编码蛋白的蓝图。
在两项新的研究中,来自德国维尔茨堡大学生物中心和马克斯普朗克生物物理化学研究所的研究人员如今首次成功过地在原子分辨率下解析出牛痘病毒RNA聚合酶(Vaccinia RNA polymerase, vRNAP)的三维结构。牛痘病毒属于痘病毒家族,对人类无害,并构成所有天花疫苗的基础。由于它的良好特性,它当前用于溶瘤病毒疗法的测试中,其中溶瘤病毒疗法是一种抵抗癌症的新策略。相关研究结果近期发表在Cell期刊上,论文标题分别为“Structural Basis of Poxvirus Transcription: Vaccinia RNA Polymerase Complexes”和“Structural Basis of Poxvirus Transcription: Transcribing and Capping Vaccinia Complexes”。这两篇论文的通讯作者为维尔茨堡大学的Utz Fischer博士和马克斯普朗克生物物理化学研究所的Patrick Cramer博士。
这些新发现如今使得开发抑制剂和调节剂来影响病毒增殖周期成为可能。鉴于牛痘病毒复制发生在细胞质中,因此这些研究人员还希望它具有治疗潜力。当前,全世界都在进行牛痘病毒用于抗癌的研究。Genelux公司已经在动物实验和患者中证实了经过特殊优化的牛痘病毒在缩小肿瘤和检测最小转移灶方面的潜力。此外,这些研究人员期待对相关的非病毒RNA聚合酶复合物的功能有新的令人兴奋的见解。
3.Cell:许多精神疾病源自相同的基因变异
doi:10.1016/j.cell.2019.11.020
在一项新的研究中,来自美国麻省总医院(MGH)和精神病基因组学联盟(Psychiatric Genomics Consortium)的研究人员发现许多不同的精神疾病具有相同的遗传结构。在给定的年份中,精神疾病影响超过25%的人群。在这项同类研究中规模最大的研究中,他们鉴定出100多种会影响一种以上精神疾病风险的基因变异。相关研究结果近期发表在Cell期刊上,论文标题为“Genomic Relationships, Novel Loci, and Pleiotropic Mechanisms across Eight Psychiatric Disorders”。

论文通讯作者、麻省总医院精神病与神经发育遗传学部门主任Jordan W. Smoller博士说,鉴定出影响一种以上精神疾病风险的基因变异是改善诊断和治疗这些疾病的重要一步。“理解特定的基因变异如何导致一系列疾病,可能告诉我们有关这些疾病具有相同生物学特性的程度。”
为了鉴定出这些多效性的基因变异,这些研究人员使用了一种称为全基因组关联的技术来分析来自494162名健康对照者和232964名经诊断患有八种常见精神疾病中至少一种的患者的遗传数据。这种分析鉴定出109种影响一种以上精神疾病风险的基因变异。
某些疾病具有许多共同的基因变异,这使得这些研究人员可以将这些精神疾病分成三组遗传相关的疾病:以强迫行为为特征的障碍(神经性厌食症、强迫症以及程度较轻的图雷特综合征);情绪和精神障碍(躁郁症、重度抑郁症和精神分裂症);早期发作的神经发育障碍(自闭症谱系障碍、多动症和图雷特综合征)。这些研究人员还发现有证据表明与多种精神疾病相关的基因从妊娠中期开始增加表达,并且似乎在大脑发育中起重要作用。
4.Cell:人胶质母细胞瘤类器官可重现肿瘤特征,并可用于评价药物和CAR-T细胞的疗效
doi:10.1016/j.cell.2019.11.036
胶质母细胞瘤是最为侵袭性的最为常见的脑癌形式。由患者自身的胶质母细胞瘤培育而成的实验室大脑类器官可能为如何最好地治疗它提供了答案。在一项新的研究中,来自美国宾夕法尼亚大学的研究人员发现胶质母细胞瘤类器官可能可以作为有效的模型来快速地测试个性化治疗策略。相关研究结果于2019年12月26日在线发表在Cell期刊上,论文标题为“Genomic Relationships, Novel Loci, and Pleiotropic Mechanisms across Eight Psychiatric Disorders”。
在这项新研究中,这些研究人员从52名患者中取出了新鲜的肿瘤样本,以便在实验室中“培养出”相应的肿瘤类器官。在两周内,产生胶质母细胞瘤类器官的总成功率为91.4%,其中66.7%的肿瘤显示出IDH1突变,75%的复发性肿瘤显示出IDH1突变。这些胶质母细胞瘤类器官也可以在生物库中存储,以便用于以后的分析。
这些研究人员还在12名患者中进行了遗传、组织学和分子分析,以便确定这些新的胶质母细胞瘤类器官在很大程度上保留了患者原发性肿瘤的特征。他们将8例胶质母细胞瘤类器官样本成功地移植到成年小鼠的大脑中,它们的大脑显示出癌细胞的快速侵袭性浸润,并且在三个月后维持关键的突变基因表达。重要的是,在小鼠模型中观察到了胶质母细胞瘤的一种主要特征---肿瘤细胞浸润到周围的大脑组织中。
为了模拟手术后的治疗方法,这些研究人员对胶质母细胞瘤类器官进行了标准治疗和靶向治疗,包括来自临床试验的药物和嵌合抗原受体(CAR)T细胞(CAR-T)免疫疗法。对于每种疗法,他们发现这些类器官对治疗作出的反应是不同的,而且治疗的有效性与患者肿瘤中的基因突变相关。这种模型为基于患者肿瘤对不同药物反应进行个体化治疗的未来临床试验提供了可能性。
5.Cell:新研究揭示为何开发通用流感疫苗如此之难
doi:10.1016/j.cell.2019.11.032
每年我们都被提醒要去药房进行流感疫苗接种。为何我们不能像麻疹疫苗或脊髓灰质炎疫苗那样拥有能提供长期保护的流感疫苗?这是因为流感病毒持续进化,因此我们第一年建立的免疫反应可能在第二年甚至在当年感染的流感病毒上都无法起作用。结果就是流感病毒仍然很危险:去年,仅在美国,它就造成了6万多人死亡。
在一项新的研究中,来自美国洛克菲勒大学的研究人员揭示了为何制造一种能够预防所有类型流感病毒的通用疫苗如此困难的原因:免疫系统对新流感病毒变种的免疫反应是从头开始建立的,主要是利用对这种病毒没有记忆的免疫细胞建立的,而不是改善对之前的流感病毒版本的免疫记忆。相关研究结果近期发表在Cell期刊上,论文标题为“Restricted Clonality and Limited Germinal Center Reentry Characterize Memory B Cell Reactivation by Boosting”。
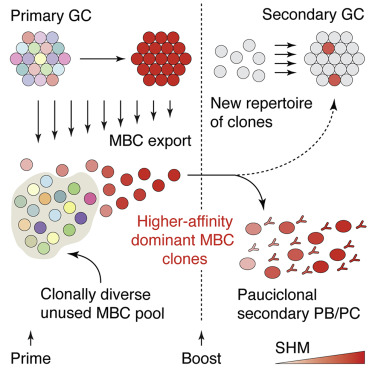
他们在第一次接种疫苗时利用荧光染料对小鼠的生发中心进行遗传标记,因此他们可以在第二次接种疫苗时追踪它们的后代的行为。令他们吃惊的是,第二次接种疫苗时进入生发中心的B细胞中有90%以上是未标记的,这表明它们是新来者。遗传分析还显示,这些细胞没有经历生发中心中的B细胞通常经历的突变过程,这进一步表明它们是首次出现在这个部位。
但是,新手训练营的退伍军人大多不存在。第一次疫苗接种时进入生发中心的数百种B细胞中,只有少数能够在第二次疫苗接种时返回到生发中心,不过它们中的多数能够结合入侵的病毒。似乎只有选定的少数B细胞才会在第二次疫苗接种时返回到生发中心。
6.Cell:挑战常规!神经系统不仅检测肠道中的沙门氏菌,而且还积极地抵御这种有害细菌
doi:10.1016/j.cell.2019.11.014
在一项新的研究中,来自美国哈佛医学院的研究人员发现小鼠肠道中的神经系统不仅感知沙门氏菌的存在,而且还可以通过部署两道防线积极地抵御这种有害细菌的感染。相关研究结果近期发表在Cell期刊上,论文标题为“Gut-Innervating Nociceptor Neurons Regulate Peyer’s Patch Microfold Cells and SFB Levels to Mediate Salmonella Host Defense”。
这项研究针对一种传统观点---神经系统仅起着看门狗的作用,即发现危险并提醒身体注意危险的存在---提供了新的视角。这些研究结果表明通过直接干扰沙门氏菌感染肠道的能力,神经系统不仅是危险的检测者,而且也是抵抗危险的防御者。
论文通讯作者、哈佛医学院布拉瓦特尼克研究所助理教授、神经免疫学者Isaac Chiu说,“我们的结果表明神经系统不仅仅是一种简单的传感器和警报系统。我们还发现肠道中的神经细胞的功能远不止这些。它们调节肠道免疫力,维持肠道稳态,并积极抵御感染。”
具体而言,这些实验表明,嵌入到小肠中的疼痛感知神经元和派尔集合淋巴结(Peyer's patch)上的细胞可被沙门氏菌的存在所激活,其中作为一种食源性细菌,沙门氏菌导致全球四分之一的细菌性腹泻病。一旦被激活,这些神经元就会采取两种防御策略来阻止沙门氏菌感染肠道并扩散到身体的其他部位。首先,它们调节允许微生物和各种物质进出小肠的细胞通道。其次,它们增加了称为分节丝状菌(segmented filamentous bacteria, SFB)的保护性肠道细菌的数量,其中SFB是小肠微生物组的一部分。
7.Cell:重磅!科学家发现了一种调节基因表达的新方法—EMATS
doi:10.1016/j.cell.2019.11.002
日前,一项刊登在国际杂志Cell上的研究报告中,来自麻省理工学院的科学家们通过研究发现了一种调节基因表达的新方式。
一旦DNA被转录成为RNA,RNA转录物就会在其翻译成蛋白质或在细胞内扮演多种角色之前被加工处理,而加工过程的重要组分就是剪接作用(splicing),在剪接过程中,特定的核苷酸序列(内含子)就会从新制造的RNA转录物中被移除,而外显子区域则会被保留,依赖于RNA被剪接的方式,单个基因往往会产生多种多样的转录物。
为了能够开启转录,分子机器就必须被招募到DNA的特定序列中,即启动子;有些启动子往往能够更加擅长地招募分子机器,因此其也会经常性地开启转录过程;然而,不同的启动子可以从一个基因中产生路由不同的转录物,这或许有助于增强基因的表达并产生转录多样性,甚至在仅仅几秒钟或几分钟后所发生的剪接过程也是如此。研究者并不确定新的外显子能够增强基因表达,但从理论上来讲,新的启动子确实会这样;基于进化学数据和研究人员在实验室所进行的研究,如今他们观察到,无论哪里有新的外显子,其附近总会有新的启动子,当外显子被剪接时,新的启动子就会变得异常活跃。
研究者将这种现象称之为“外显子介导的转录激活启动”(EMATS,exon-mediated activation of transcription starts),其提出了一种新型模型,其中与新外显子相关的剪接机器会将转录机器招募到附近,从而激活附近启动子的转录过程,研究人员推测,这一过程将会帮助调节跨物种的数千个哺乳基因的表达。研究者Fiszbein认为,EMATS会在进化过程中增强基因组的复杂性,或许也会产生物种的特殊差异,比如小鼠和大鼠的基因组就非常相似,但EMATS会帮其产生新的启动子,从而产生调节性改变,并驱动大鼠和小鼠机体在结构和功能上的差异。EMATS同时还会诱发相同有机体不同组织之间表达产生差异。
8.Cell:基因剔除研究或能帮助识别多个疟原虫靶点 有望开发新型抗疟疗法
doi:10.1016/j.cell.2019.10.030
近日,一项刊登在国际杂志Cell上的研究报告中,来自伯尔尼大学等机构的科学家们通过研究鉴别出了多个疟原虫的新型作用靶点,他们对疟原虫进行全基因组剔除研究,尤其是移除了1300多个单一基因,同时观察其对疟原虫整个生命周期的而影响。文章中,研究者利用已经建立的疟原虫模型进行研究,上述1300多个基因中的每一个基因都会被一个单独的遗传代码所替代,从而帮助分析去除这些单一基因对疟原虫的影响,利用这些单一代码就能帮助研究人员将同时对更多寄生虫进行分析,这就大大缩短了进行分析的时间。
在进行了长达3年的研究后,研究人员成功地系统性地筛选了疟原虫生命周期各个阶段的基因组,进行剔除筛选研究能帮助研究者识别出数百个靶点,尤其是针对疟原虫代谢的特殊靶点等。为了分析大量已经鉴别出的代谢基因,研究人员通力合作,利用来自疟原虫基因组筛选的数据开发出了特殊的模型来揭示疟原虫细胞中基本代谢通路,在这些模型的帮助下,研究人员才有可能预测哪些未知基因对于疟原虫非常重要,以及其如何作为开发控制疟原虫传播感染的新型疗法。
9.Cell:揭示Ω-3脂肪酸促进脂肪干细胞分裂产生更多脂肪细胞机制
doi:10.1016/j.cell.2019.11.005
多年来,科学家们已知道初级纤毛存在缺陷与肥胖和胰岛素抵抗有关。如今,在一项新的研究中,来自美国斯坦福大学医学院的研究人员发现一类微小的称为初级纤毛(primary cilium)的毛发状附属物感知饮食中的Ω-3脂肪酸,而且这种信号直接影响脂肪组织中的干细胞如何分裂并转变为脂肪细胞。相关研究结果近期发表在Cell期刊上,论文标题为“Omega-3 Fatty Acids Activate Ciliary FFAR4 to Control Adipogenesis”。论文通讯作者为Peter Jackson博士。论文第一作者为博士后研究员Keren Hilgendorf博士。

Jackson和他的同事们发现当Ω-3脂肪酸与脂肪干细胞的初级纤毛表面上的一种称为FFAR4的受体结合时,它会促使脂肪干细胞分裂,从而导致更多的脂肪细胞产生。这为身体提供了更多的脂肪细胞来储存能量,这比在现有的脂肪细胞中储存过多的脂肪更健康。Jackson说:“你需要的是更多的较小的脂肪细胞,而不是更少的较大的脂肪细胞。较大的脂肪细胞不是健康的脂肪细胞。”他补充道,较大的脂肪细胞与胰岛素抵抗、糖尿病和炎症有关。
饱和脂肪的存在或FFAR4受体纤毛信号转导的阻断并不会导致脂肪干细胞更多地产生新的脂肪细胞,而是使得现有的脂肪细胞增加脂肪储存。Hilgendorf说,“我们没有探究饮食与健康的关系,而是从分子到受体再到细胞来证实‘健康的脂肪’为何是有益的,‘不健康的脂肪’为何导致疾病产生。我们揭示了一种机制来解释为何Ω-3脂肪酸对维持健康的脂肪平衡至关重要,饱和脂肪应当受到限制。”
10.Cell:科学家鉴别出隐藏在机体免疫反应背后的新型分子机制
doi:10.1016/j.cell.2019.11.001
近日,一项刊登在国际杂志Cell上的研究报告中,来自德国慕尼黑大学等机构的科学家们通过研究发现,先天性免疫反应中的一种中心组分或能被两种短链RNAs激活,而这些RNAs是通过前体RNA分子的位点特异性切割所产生,其衍生物也能被相同的酶类所产生。
先天性免疫反应常常被认为是机体抵御外来病原体的第一道防线,细胞拥有特殊的受体,其能区分来自外源性细胞所产生的RNAs和自身的RNAs,识别出外源性的RNAs后就会激活机体适当的免疫反应来清除入侵者;然而目前研究人员并不清楚其背后的分子机制;这项研究中,研究人员通过联合研究发现,一种名为TLR8的受体的激活或能通过结合到两个特殊的RNA片段(外源性RNA降解所产生)上而被介导,而外源性RNA的破碎产物也能被名为RNase T2的单一酶类所产生。
研究者Hornung表示,此前研究结果表明,外源性RNA分子并不被视为一个整体,在其被机体先天性免疫系统识别之前必须被切割成为小型碎片;为了深入阐明先天性免疫系统识别的机制,研究者从人类细胞模型中剔除了单一Rnases的基因,随后他们分析了缺失每一种Rnases如何影响TLR8的激活,TLR8被认为是人类细胞中细菌RNA的重要感应器,研究人员选择对人类细胞模型进行研究,因为在小鼠机体中,该受体的版本会以一种不同的方式来发挥作用。
研究者发现,仅仅RNase T2基因表达缺失的细胞才不会诱发TLR8所介导的细菌RNA反应,这就阐明了该酶在激活受体表达过程中的重要角色;值得注意的是,酶类RNase T2在进化过程中高度保守,实际上其在所有有机体中都存在,而且其在结构上并没有改变;这种高度的保守结构就表明,其能够发挥最基本的细胞功能,而且其中的机制在其它物种中也扮演着非常关键的角色。(生物谷 Bioon.com)
1.Cell:经过基因改造的大肠杆菌也可通过摄入空气中的二氧化碳进行生长
doi:10.1016/j.cell.2019.11.009
在一项新的研究中,来自以色列魏茨曼科学研究所的研究人员对大肠杆菌进行基因改造,使得它们通过吸收二氧化碳就可以生长。相关研究结果近期发表在Cell期刊上,论文标题为“Conversion of Escherichia coli to Generate All Biomass Carbon from CO2”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.11.009。
大肠杆菌通常是异养生物(heterotroph),即摄入葡萄糖等有机化合物作为食物的有机物,但是这项新的研究表明它们可以转化为自养生物(autotroph),从大气中吸收二氧化碳并将它转化为生物量(biomass)。
美国加州大学伯克利分校生物化学家Dave Savage(未参与这项新的研究)说,“我发现一种经过数十亿年进化进行异养生活的有机体能够如此快速地和彻底地转变成自养生物,这实在是太神奇了。这表明代谢极具可塑性。”
2.两篇Cell从结构上揭示牛痘病毒增殖机制,有望开发出更好地用于治疗癌症的病毒载体
doi:10.1016/j.cell.2019.11.024; doi:10.1016/j.cell.2019.11.023
为了让病毒增殖,它们通常需要被感染细胞的支持。在许多情况下,在感染附近的其他细胞之前,只有在宿主细胞的细胞核中才能找到它们复制它们自己的遗传物质所需的分子。但是并非所有病毒都能进入细胞核中。一些病毒停留在细胞质中,因此必须能够独立地复制它们的遗传物质。为此,它们必须带上它们自己的“加工零件”。在这个过程中起关键作用是一种由各种亚基组成的特殊酶---RNA聚合酶---完成的。这种酶从病毒基因组中读取遗传信息,并将它转录为信使RNA(mRNA),并利用mRNA作为基因组中编码蛋白的蓝图。
在两项新的研究中,来自德国维尔茨堡大学生物中心和马克斯普朗克生物物理化学研究所的研究人员如今首次成功过地在原子分辨率下解析出牛痘病毒RNA聚合酶(Vaccinia RNA polymerase, vRNAP)的三维结构。牛痘病毒属于痘病毒家族,对人类无害,并构成所有天花疫苗的基础。由于它的良好特性,它当前用于溶瘤病毒疗法的测试中,其中溶瘤病毒疗法是一种抵抗癌症的新策略。相关研究结果近期发表在Cell期刊上,论文标题分别为“Structural Basis of Poxvirus Transcription: Vaccinia RNA Polymerase Complexes”和“Structural Basis of Poxvirus Transcription: Transcribing and Capping Vaccinia Complexes”。这两篇论文的通讯作者为维尔茨堡大学的Utz Fischer博士和马克斯普朗克生物物理化学研究所的Patrick Cramer博士。
这些新发现如今使得开发抑制剂和调节剂来影响病毒增殖周期成为可能。鉴于牛痘病毒复制发生在细胞质中,因此这些研究人员还希望它具有治疗潜力。当前,全世界都在进行牛痘病毒用于抗癌的研究。Genelux公司已经在动物实验和患者中证实了经过特殊优化的牛痘病毒在缩小肿瘤和检测最小转移灶方面的潜力。此外,这些研究人员期待对相关的非病毒RNA聚合酶复合物的功能有新的令人兴奋的见解。
3.Cell:许多精神疾病源自相同的基因变异
doi:10.1016/j.cell.2019.11.020
在一项新的研究中,来自美国麻省总医院(MGH)和精神病基因组学联盟(Psychiatric Genomics Consortium)的研究人员发现许多不同的精神疾病具有相同的遗传结构。在给定的年份中,精神疾病影响超过25%的人群。在这项同类研究中规模最大的研究中,他们鉴定出100多种会影响一种以上精神疾病风险的基因变异。相关研究结果近期发表在Cell期刊上,论文标题为“Genomic Relationships, Novel Loci, and Pleiotropic Mechanisms across Eight Psychiatric Disorders”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.11.020。
论文通讯作者、麻省总医院精神病与神经发育遗传学部门主任Jordan W. Smoller博士说,鉴定出影响一种以上精神疾病风险的基因变异是改善诊断和治疗这些疾病的重要一步。“理解特定的基因变异如何导致一系列疾病,可能告诉我们有关这些疾病具有相同生物学特性的程度。”
为了鉴定出这些多效性的基因变异,这些研究人员使用了一种称为全基因组关联的技术来分析来自494162名健康对照者和232964名经诊断患有八种常见精神疾病中至少一种的患者的遗传数据。这种分析鉴定出109种影响一种以上精神疾病风险的基因变异。
某些疾病具有许多共同的基因变异,这使得这些研究人员可以将这些精神疾病分成三组遗传相关的疾病:以强迫行为为特征的障碍(神经性厌食症、强迫症以及程度较轻的图雷特综合征);情绪和精神障碍(躁郁症、重度抑郁症和精神分裂症);早期发作的神经发育障碍(自闭症谱系障碍、多动症和图雷特综合征)。这些研究人员还发现有证据表明与多种精神疾病相关的基因从妊娠中期开始增加表达,并且似乎在大脑发育中起重要作用。
4.Cell:人胶质母细胞瘤类器官可重现肿瘤特征,并可用于评价药物和CAR-T细胞的疗效
doi:10.1016/j.cell.2019.11.036
胶质母细胞瘤是最为侵袭性的最为常见的脑癌形式。由患者自身的胶质母细胞瘤培育而成的实验室大脑类器官可能为如何最好地治疗它提供了答案。在一项新的研究中,来自美国宾夕法尼亚大学的研究人员发现胶质母细胞瘤类器官可能可以作为有效的模型来快速地测试个性化治疗策略。相关研究结果于2019年12月26日在线发表在Cell期刊上,论文标题为“Genomic Relationships, Novel Loci, and Pleiotropic Mechanisms across Eight Psychiatric Disorders”。
在这项新研究中,这些研究人员从52名患者中取出了新鲜的肿瘤样本,以便在实验室中“培养出”相应的肿瘤类器官。在两周内,产生胶质母细胞瘤类器官的总成功率为91.4%,其中66.7%的肿瘤显示出IDH1突变,75%的复发性肿瘤显示出IDH1突变。这些胶质母细胞瘤类器官也可以在生物库中存储,以便用于以后的分析。
这些研究人员还在12名患者中进行了遗传、组织学和分子分析,以便确定这些新的胶质母细胞瘤类器官在很大程度上保留了患者原发性肿瘤的特征。他们将8例胶质母细胞瘤类器官样本成功地移植到成年小鼠的大脑中,它们的大脑显示出癌细胞的快速侵袭性浸润,并且在三个月后维持关键的突变基因表达。重要的是,在小鼠模型中观察到了胶质母细胞瘤的一种主要特征---肿瘤细胞浸润到周围的大脑组织中。
为了模拟手术后的治疗方法,这些研究人员对胶质母细胞瘤类器官进行了标准治疗和靶向治疗,包括来自临床试验的药物和嵌合抗原受体(CAR)T细胞(CAR-T)免疫疗法。对于每种疗法,他们发现这些类器官对治疗作出的反应是不同的,而且治疗的有效性与患者肿瘤中的基因突变相关。这种模型为基于患者肿瘤对不同药物反应进行个体化治疗的未来临床试验提供了可能性。
5.Cell:新研究揭示为何开发通用流感疫苗如此之难
doi:10.1016/j.cell.2019.11.032
每年我们都被提醒要去药房进行流感疫苗接种。为何我们不能像麻疹疫苗或脊髓灰质炎疫苗那样拥有能提供长期保护的流感疫苗?这是因为流感病毒持续进化,因此我们第一年建立的免疫反应可能在第二年甚至在当年感染的流感病毒上都无法起作用。结果就是流感病毒仍然很危险:去年,仅在美国,它就造成了6万多人死亡。
在一项新的研究中,来自美国洛克菲勒大学的研究人员揭示了为何制造一种能够预防所有类型流感病毒的通用疫苗如此困难的原因:免疫系统对新流感病毒变种的免疫反应是从头开始建立的,主要是利用对这种病毒没有记忆的免疫细胞建立的,而不是改善对之前的流感病毒版本的免疫记忆。相关研究结果近期发表在Cell期刊上,论文标题为“Restricted Clonality and Limited Germinal Center Reentry Characterize Memory B Cell Reactivation by Boosting”。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.11.032。
他们在第一次接种疫苗时利用荧光染料对小鼠的生发中心进行遗传标记,因此他们可以在第二次接种疫苗时追踪它们的后代的行为。令他们吃惊的是,第二次接种疫苗时进入生发中心的B细胞中有90%以上是未标记的,这表明它们是新来者。遗传分析还显示,这些细胞没有经历生发中心中的B细胞通常经历的突变过程,这进一步表明它们是首次出现在这个部位。
但是,新手训练营的退伍军人大多不存在。第一次疫苗接种时进入生发中心的数百种B细胞中,只有少数能够在第二次疫苗接种时返回到生发中心,不过它们中的多数能够结合入侵的病毒。似乎只有选定的少数B细胞才会在第二次疫苗接种时返回到生发中心。
6.Cell:挑战常规!神经系统不仅检测肠道中的沙门氏菌,而且还积极地抵御这种有害细菌
doi:10.1016/j.cell.2019.11.014
在一项新的研究中,来自美国哈佛医学院的研究人员发现小鼠肠道中的神经系统不仅感知沙门氏菌的存在,而且还可以通过部署两道防线积极地抵御这种有害细菌的感染。相关研究结果近期发表在Cell期刊上,论文标题为“Gut-Innervating Nociceptor Neurons Regulate Peyer’s Patch Microfold Cells and SFB Levels to Mediate Salmonella Host Defense”。
这项研究针对一种传统观点---神经系统仅起着看门狗的作用,即发现危险并提醒身体注意危险的存在---提供了新的视角。这些研究结果表明通过直接干扰沙门氏菌感染肠道的能力,神经系统不仅是危险的检测者,而且也是抵抗危险的防御者。
论文通讯作者、哈佛医学院布拉瓦特尼克研究所助理教授、神经免疫学者Isaac Chiu说,“我们的结果表明神经系统不仅仅是一种简单的传感器和警报系统。我们还发现肠道中的神经细胞的功能远不止这些。它们调节肠道免疫力,维持肠道稳态,并积极抵御感染。”
具体而言,这些实验表明,嵌入到小肠中的疼痛感知神经元和派尔集合淋巴结(Peyer's patch)上的细胞可被沙门氏菌的存在所激活,其中作为一种食源性细菌,沙门氏菌导致全球四分之一的细菌性腹泻病。一旦被激活,这些神经元就会采取两种防御策略来阻止沙门氏菌感染肠道并扩散到身体的其他部位。首先,它们调节允许微生物和各种物质进出小肠的细胞通道。其次,它们增加了称为分节丝状菌(segmented filamentous bacteria, SFB)的保护性肠道细菌的数量,其中SFB是小肠微生物组的一部分。
7.Cell:重磅!科学家发现了一种调节基因表达的新方法—EMATS
doi:10.1016/j.cell.2019.11.002
日前,一项刊登在国际杂志Cell上的研究报告中,来自麻省理工学院的科学家们通过研究发现了一种调节基因表达的新方式。
一旦DNA被转录成为RNA,RNA转录物就会在其翻译成蛋白质或在细胞内扮演多种角色之前被加工处理,而加工过程的重要组分就是剪接作用(splicing),在剪接过程中,特定的核苷酸序列(内含子)就会从新制造的RNA转录物中被移除,而外显子区域则会被保留,依赖于RNA被剪接的方式,单个基因往往会产生多种多样的转录物。
为了能够开启转录,分子机器就必须被招募到DNA的特定序列中,即启动子;有些启动子往往能够更加擅长地招募分子机器,因此其也会经常性地开启转录过程;然而,不同的启动子可以从一个基因中产生路由不同的转录物,这或许有助于增强基因的表达并产生转录多样性,甚至在仅仅几秒钟或几分钟后所发生的剪接过程也是如此。研究者并不确定新的外显子能够增强基因表达,但从理论上来讲,新的启动子确实会这样;基于进化学数据和研究人员在实验室所进行的研究,如今他们观察到,无论哪里有新的外显子,其附近总会有新的启动子,当外显子被剪接时,新的启动子就会变得异常活跃。
研究者将这种现象称之为“外显子介导的转录激活启动”(EMATS,exon-mediated activation of transcription starts),其提出了一种新型模型,其中与新外显子相关的剪接机器会将转录机器招募到附近,从而激活附近启动子的转录过程,研究人员推测,这一过程将会帮助调节跨物种的数千个哺乳基因的表达。研究者Fiszbein认为,EMATS会在进化过程中增强基因组的复杂性,或许也会产生物种的特殊差异,比如小鼠和大鼠的基因组就非常相似,但EMATS会帮其产生新的启动子,从而产生调节性改变,并驱动大鼠和小鼠机体在结构和功能上的差异。EMATS同时还会诱发相同有机体不同组织之间表达产生差异。
8.Cell:基因剔除研究或能帮助识别多个疟原虫靶点 有望开发新型抗疟疗法
doi:10.1016/j.cell.2019.10.030
近日,一项刊登在国际杂志Cell上的研究报告中,来自伯尔尼大学等机构的科学家们通过研究鉴别出了多个疟原虫的新型作用靶点,他们对疟原虫进行全基因组剔除研究,尤其是移除了1300多个单一基因,同时观察其对疟原虫整个生命周期的而影响。文章中,研究者利用已经建立的疟原虫模型进行研究,上述1300多个基因中的每一个基因都会被一个单独的遗传代码所替代,从而帮助分析去除这些单一基因对疟原虫的影响,利用这些单一代码就能帮助研究人员将同时对更多寄生虫进行分析,这就大大缩短了进行分析的时间。
在进行了长达3年的研究后,研究人员成功地系统性地筛选了疟原虫生命周期各个阶段的基因组,进行剔除筛选研究能帮助研究者识别出数百个靶点,尤其是针对疟原虫代谢的特殊靶点等。为了分析大量已经鉴别出的代谢基因,研究人员通力合作,利用来自疟原虫基因组筛选的数据开发出了特殊的模型来揭示疟原虫细胞中基本代谢通路,在这些模型的帮助下,研究人员才有可能预测哪些未知基因对于疟原虫非常重要,以及其如何作为开发控制疟原虫传播感染的新型疗法。
9.Cell:揭示Ω-3脂肪酸促进脂肪干细胞分裂产生更多脂肪细胞机制
doi:10.1016/j.cell.2019.11.005
多年来,科学家们已知道初级纤毛存在缺陷与肥胖和胰岛素抵抗有关。如今,在一项新的研究中,来自美国斯坦福大学医学院的研究人员发现一类微小的称为初级纤毛(primary cilium)的毛发状附属物感知饮食中的Ω-3脂肪酸,而且这种信号直接影响脂肪组织中的干细胞如何分裂并转变为脂肪细胞。相关研究结果近期发表在Cell期刊上,论文标题为“Omega-3 Fatty Acids Activate Ciliary FFAR4 to Control Adipogenesis”。论文通讯作者为Peter Jackson博士。论文第一作者为博士后研究员Keren Hilgendorf博士。

图片来自Cell, 2019, doi:10.1016/j.cell.2019.11.005。
Jackson和他的同事们发现当Ω-3脂肪酸与脂肪干细胞的初级纤毛表面上的一种称为FFAR4的受体结合时,它会促使脂肪干细胞分裂,从而导致更多的脂肪细胞产生。这为身体提供了更多的脂肪细胞来储存能量,这比在现有的脂肪细胞中储存过多的脂肪更健康。Jackson说:“你需要的是更多的较小的脂肪细胞,而不是更少的较大的脂肪细胞。较大的脂肪细胞不是健康的脂肪细胞。”他补充道,较大的脂肪细胞与胰岛素抵抗、糖尿病和炎症有关。
饱和脂肪的存在或FFAR4受体纤毛信号转导的阻断并不会导致脂肪干细胞更多地产生新的脂肪细胞,而是使得现有的脂肪细胞增加脂肪储存。Hilgendorf说,“我们没有探究饮食与健康的关系,而是从分子到受体再到细胞来证实‘健康的脂肪’为何是有益的,‘不健康的脂肪’为何导致疾病产生。我们揭示了一种机制来解释为何Ω-3脂肪酸对维持健康的脂肪平衡至关重要,饱和脂肪应当受到限制。”
10.Cell:科学家鉴别出隐藏在机体免疫反应背后的新型分子机制
doi:10.1016/j.cell.2019.11.001
近日,一项刊登在国际杂志Cell上的研究报告中,来自德国慕尼黑大学等机构的科学家们通过研究发现,先天性免疫反应中的一种中心组分或能被两种短链RNAs激活,而这些RNAs是通过前体RNA分子的位点特异性切割所产生,其衍生物也能被相同的酶类所产生。
先天性免疫反应常常被认为是机体抵御外来病原体的第一道防线,细胞拥有特殊的受体,其能区分来自外源性细胞所产生的RNAs和自身的RNAs,识别出外源性的RNAs后就会激活机体适当的免疫反应来清除入侵者;然而目前研究人员并不清楚其背后的分子机制;这项研究中,研究人员通过联合研究发现,一种名为TLR8的受体的激活或能通过结合到两个特殊的RNA片段(外源性RNA降解所产生)上而被介导,而外源性RNA的破碎产物也能被名为RNase T2的单一酶类所产生。
研究者Hornung表示,此前研究结果表明,外源性RNA分子并不被视为一个整体,在其被机体先天性免疫系统识别之前必须被切割成为小型碎片;为了深入阐明先天性免疫系统识别的机制,研究者从人类细胞模型中剔除了单一Rnases的基因,随后他们分析了缺失每一种Rnases如何影响TLR8的激活,TLR8被认为是人类细胞中细菌RNA的重要感应器,研究人员选择对人类细胞模型进行研究,因为在小鼠机体中,该受体的版本会以一种不同的方式来发挥作用。
研究者发现,仅仅RNase T2基因表达缺失的细胞才不会诱发TLR8所介导的细菌RNA反应,这就阐明了该酶在激活受体表达过程中的重要角色;值得注意的是,酶类RNase T2在进化过程中高度保守,实际上其在所有有机体中都存在,而且其在结构上并没有改变;这种高度的保守结构就表明,其能够发挥最基本的细胞功能,而且其中的机制在其它物种中也扮演着非常关键的角色。(生物谷 Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->


