肠道微生物组研究进展(第8期)
来源:本站原创 2021-05-30 23:18
随着科学家们研究的不断深入,近年来肠道微生物组相继得到全球多国科学家的重点关注和研究,很多研究都发现肠道微生物组与机体多方面健康和疾病都密切相关,本文中,小编就整理了多篇重要文章,共同解读科学家们肠道微生物组研究方面取得的新进展,与大家一起学习! 癌性恶病质与临床病理特征的比较图片来源:https://doi.org/10.1038/s41396-
随着科学家们研究的不断深入,近年来肠道微生物组相继得到全球多国科学家的重点关注和研究,很多研究都发现肠道微生物组与机体多方面健康和疾病都密切相关,本文中,小编就整理了多篇重要文章,共同解读科学家们肠道微生物组研究方面取得的新进展,与大家一起学习!
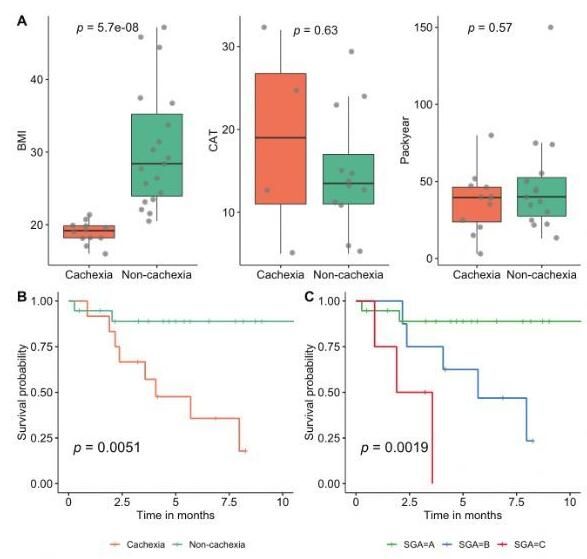
癌性恶病质与临床病理特征的比较
图片来源:https://doi.org/10.1038/s41396-021-00998-8
doi:10.1038/s41396-021-00998-8
近日,莱布尼茨天然产物研究和感染生物学研究所在ISME J杂志上发表了题为"Distinct composition and metabolic functions of human gut microbiota are associated with cachexia in lung cancer patients"的文章。该研究在临床环境中证明了恶病质宿主代谢与特定肠道微生物种类和功能之间的联系,提示肠道微生物区系可能对恶病质产生影响,具有可能的治疗应用。
如今科学家们已经提出了几种治疗癌症恶病质的方法,包括靶向分解代谢因子、刺激食欲和肌肉再生;然而,这些方法的疗效有限。营养素如欧米茄-3脂肪酸(二十碳五烯酸和二十二碳六烯酸)可以减轻炎症,亮氨酸和牛奶蛋白可以促进蛋白质合成,也被认为是潜在的治疗方案。然而,没有一种单一的治疗方法足以治疗这种多因素疾病,可能需要考虑营养、运动和药理学因素的多模式治疗。
文章中,作者对31例人类肺癌患者的血浆代谢组、肠道细菌分类和功能进行了深入分析,方法是将非靶向代谢组学应用于患者血浆样本,并应用鸟枪式元基因组学收集粪便样本。特定的代谢物、肠道微生物种类及其代谢途径与恶病质状态有关。为了全面了解肠道微生物群在恶病质中的作用,作者随后将分类学和功能特征与代谢组学数据相结合。考虑到微生物区系特征的组合效应,开发了恶病质和非恶病质患者的机器学习分类器,并进一步支持肠道微生物区系的假设作用。在这里,作者的目标是确定微生物群与恶病质的关系,为这一影响癌症治疗结果的危重疾病开辟新的治疗选择的道路。
【2】Br J Pharmacol:肠道微生物区系在系统性红斑狼疮遗传性小鼠模型高血压发病中的作用
doi:10.1111/bph.15512
格拉纳达大学在英国药理学杂志上发表了题为"Gut microbiota contributes to the development of hypertension in a genetic mouse model of systemic lupus erythematosus"的文章。该研究发现了由遗传性系统性红斑狼疮背景引起的T细胞群、内皮功能、血管炎症和高血压的改变可以通过抗生素诱导的肠道微生物区系的改变来改变。高血压系统性红斑狼疮(SLE)微生物区系引起的血管改变是由Th17在血管系统的浸润介导的。
系统性红斑狼疮(SLE)被认为是危害最大的自身免疫性炎症性疾病之一。它的特点是自身抗体的产生,促使免疫复合物的形成和沉淀,进而损害许多器官和组织。系统性红斑狼疮与发生肾脏和心血管疾病的高风险有关,这是导致系统性红斑狼疮患者死亡的最主要原因。它主要影响育龄年轻女性,这一人群患动脉粥样硬化性心脏病的相对风险最低。这种疾病被认为与高血压的高发病率有关。
作者的研究表明:1)与年龄匹配的对照组相比,高血压系统性红斑狼疮小鼠的肠道微生物区系不同,2)这种肠道微生物区系驱动NZBWF1血压的变化,抗生素治疗和FMT证明了这一点,3)这是由于促炎Th17细胞的激活。血浆抗ds-DNA抗体和LPS均不是肠道微生物区系诱导的SLE小鼠血压调节的关键介质。系统性红斑狼疮是一种女性偏向疾病,女性患病率几乎是男性的9:1。到目前为止显示的结果是从雌性小鼠身上获得的。考虑到有一些证据支持肠道微生物区系因性别不同而不同,应该分析肠道微生物区系在雄性小鼠血压控制中的作用。本研究结果为通过调节肠道微生物区系组成预防系统性红斑狼疮相关心血管并发症提供了新的可能性。然而,由于动物和人类微生物群的特征之间的潜在差异,在将这些发现外推到人类时应该谨慎。
【3】mBio:人类机体的肠道微生物组为何会因人而异?科学家们为你揭秘!
doi:10.1128/mBio.00548-21
人类肠道微生物组的组成是高度可变的,研究人员发现这种变化与人类机体健康之间存在着千丝万缕的关系;然而,目前研究人员并不清楚微生物变化的来源到底是什么,尤其是在人类生命早期;因此了解生命早期机体微生物组的改变尤为重要,因为儿童时期机体的微生物组状态会影响个体一生的健康。日前,一篇刊登在国际杂志mBio上题为“Shared Environment and Genetics Shape the Gut Microbiome after Infant Adoption”的研究报告中,来自俄勒冈大学等机构的科学家们通过研究发现,共同的家庭环境或是人类微生物组相似性最强的预测因素,或者说是生活在我们体内的微生物群落之间的共同点。
本文研究结果表明,早期生活的家庭环境或能极大地改变个体儿童时期的肠道微生物组;研究者表示,人类拥有与之相关的丰富多样的微生物生命,其能以多种方式来促进机体的健康;而其中一个奥秘就是为何微生物群落的差异因人而异;本文研究中,研究人员就通过研究阐明了到底是环境因素还是遗传因素在确定与机体相关的微生物方面更加重要。该研究计划始于5年前研究者Leve提出的一个简单的问题,即当两个兄弟姐妹从出生就在不同的家庭中长大时,其机体的微生物组到底有什么不同?
基于此前研究结果,本文研究结果或能为研究人员提供一幅完整的图谱来阐明疾病发生的过程,以及如何基于机体微生物菌群的组成来预防疾病,最终或有望帮助开发更有效的干预性策略来改善人类机体早期的健康状况。综上,本文研究结果表明,个体生命早期的家庭环境或会明显改变儿童时期机体的肠道微生物组,尤其是可能会改变健康结局或不良健康结果的风险。而更好地理解儿童时期肠道微生物组改变的驱动因素或有望帮助开发有效的措施来改善个体生命早期的机体整体健康状况。
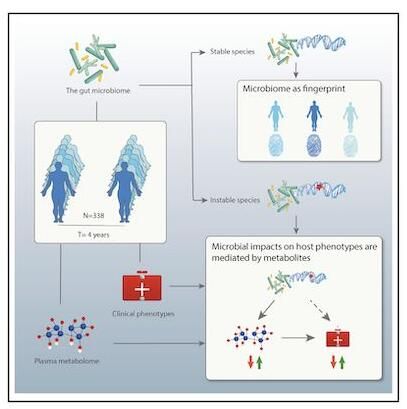
图片来源:www.cell.com
doi:10.1016/j.cell.2021.03.024
人的肠道具有多种多样的微生物群落,它们之间存在较大差异。此前的交叉-横断面分析已将这些变异与人类健康和疾病表型相关联。肠道微生物群也会在个体的生命过程中发生变化,该变化与宿主健康和疾病状况之间存在互为因果的多重联系。此前多项研究评估了微生物分类学组成的时间变化,并为针对宿主与微生物组串扰对健康和疾病的后果进行针对性的机制性研究奠定了基础,包括早期的研究儿童期,早发1型和2型糖尿病和炎症性肠病等。
然而,关于肠道微生物组的时间变化趋势的几个重要问题仍需要得到进一步揭示。首先,除了肠道微生物组成外,微生物基因组的遗传组成也会随时间动态变化。物种演化和菌株替代导致的微生物基因组变化,例如单核苷酸突变和基因组区域的获得或丢失,与人类疾病的发展有关。然而,关于微生物遗传组成的时间变化的研究仍然缺乏。其次,尽管横断面关联分析报告了许多与宿主健康和疾病之间存在关联的微生物群组特征,但其普遍缺乏纵向(即时序性)验证。第三,鉴于近几十年来抗生素的广泛使用,包括抗生素耐药性和毒力因子等在内的其它细菌衍生物已成为主要关注的问题。然而,相关微生物衍生物随时间的变化趋势尚无得到清晰揭示,这阻碍了细菌感染的有效预防和治疗。
对此,在最近发表在《Cell》杂志上的一项研究中,来自荷兰格罗宁根大学的Jingyuan Fu课题组对囊括338位志愿者的Lifelines-DEEP、队列进行了肠道微生物组的长期随访分析,比较了相隔4年的样本。作者表征了肠道微生物组成和遗传组成的长期时间稳定性,并试图回答以下两种类型的问题:(1)哪些细菌特征既具有个体特异性又具有时间稳定性?是否可以将这些功能用作“指纹”来区分同一个人的样本? (2)哪些细菌特征表现出较大的时间变化?它们的时间变化是否可以与宿主的临床表型和生活方式的变化联系在一起?作者还对微生物的遗传学特征以及代谢谱系变化趋势进行了详尽的分析,在此不再赘述。综上,作者通过跟踪志愿者群体4年之间肠道微生物组各项变化趋势,血浆代谢产物水平,以及志愿者个人生理表型变化特征等,表征了微生物的稳定性和与宿主生理相关的变异。利用这些个体特异性和时间稳定的微生物谱(包括细菌SNP和结构变异),作者开发了一种微生物指纹图谱方法,显示出高达85%的准确度。例如,有190个微生物纵向变化特征与宿主表型相关,而519个微生物纵向变化特征与血浆代谢产物相关。
【5】Cell Host & Micro:有意思!个体出生的头5年里机体中的肠道菌群是如何发展的?
doi:10.1016/j.chom.2021.02.021
肠道菌群在个体出生时就已经被建立了,然而不同的细菌是通过怎样的演替方式进入到机体肠道菌群的,至今科学家们仍然并不清楚;近日,一篇发表在国际杂志Cell Host & Microbe上题为“Developmental trajectory of the healthy human gut microbiota during the first 5 years of life”的研究报告中,来自哥德堡大学等机构的科学家们就通过研究发现,人类机体的肠道菌群在其5岁时就基本能够达到成年人机体的组成了,但重要的差异仍然会存在;一些与人类健康相关的细菌群落是在儿童时期晚期所获得的,到5岁时其并未达到成年时的水平或数量。
研究者Josefine Roswall表示,长期以来科学家们一直关注婴儿期机体的肠道微生物组,其对肠道微生物组和其它生理和生物学过程而言都是一个非常重要的发展时期;然而,科学家们并不是非常清楚个体在出生后几年里肠道微生物组是如何进行发育的。为了解决这一研究空白,本文中,科学家们对来自瑞典从出生至5岁的471名儿童进行追踪分析,他们使用16SrRNA基因测序技术分析了参与者在出生四个月、1年、3年和5年时收集的粪便中的微生物,随后将这些儿童机体的微生物群落与其母亲以及瑞典成年人机体的微生物群落进行对比研究。
综上,研究人员利用了一个纵向出生队列描述了个体在出生后5年时间里机体中肠道菌群的发育情况,一些与人类健康相关的菌群是儿童在童年晚期所获得的,而且在其5岁时并未达到成年人机体的水平;此外,研究者还观察到,正常儿童机体中的肠道菌群会沿着微生物菌群的发展轨迹以特定的速度来进行发展,这就强调了考虑人类机体中微生物菌群动态变化的重要性。
【6】Cancer Cell:肠道菌群如何导致结直肠癌向肝脏的转移?
doi:10.1016/j.ccell.2021.03.004
癌症的恶化与转移(Metastasis)会受到一种名为“促转移龛(premetastatic niche)”结构的形成而加速发生,而后者主要由原发部位肿瘤相关因子的刺激形成。此前研究发现,结直肠癌细胞往往会向肝脏转移。在最近发表在Cancer Cell杂志上的一篇文章中,来自意大利Humanitas研究医院的Maria Rescigno教授等人发现肝脏中促转移龛的形成依赖于结肠癌原发部位附近的细菌扩散,而该过程是由于肠道血管屏障的损伤导致的。由于PV-1是指征肠道血管屏障损伤的标志物,因此其有希望作为预测结肠癌细胞向肝脏转移的诊断标记。
在这项研究中,作者首先调查了结肠癌患者肠道血管屏障损伤的情况。为此,作者收集了179名未转移结直肠癌患者以及10名健康人的肠切片样本,并进行了染色分析。结果显示,PV-1的表达水平在结肠癌原发部位以及周围健康组织中并无明显差异。进一步,作者将患者样本根据其后期进展情况分为两组,其中100名患者没有发生转移与恶化,另外79名患者则发生了转移与恶化。分析结果显示,发生转移与恶化的患者样本中PV-1的表达量明显高于前者。该结果预示着PV-1可能是预测患者肠癌进展的新型标志物。
作者建立了AOM-DSS诱导的小鼠自发性肠癌模型,并且给与小鼠抗生素处理。结果显示,抗生素处理并不会影响原发部位的肿瘤数量,但是会显著影响其向肝脏的转移效率。综上,作者首次揭示了肠道菌群促进结直肠癌细胞向肝脏转移并促进其促转移龛形成的内在机制,并且提供了诊断结直肠癌恶化风险的新型标志物,这些发现对于将来结直肠癌的研究与临床治疗均有特殊的意义。
图片来源:Pixabay/CC0 Public Domain
【7】Cell:科学家有望利用人类机体的肠道微生物组来开发治疗神经系统疾病的新型靶向性疗法!
doi:10.1016/j.cell.2021.02.009
当我们想到诱发神经系统疾病的原因以及如何治疗时,我们通常会想到针对大脑来进行研究;但这到底是不是最佳的方法或者唯一的方向呢?日前,一篇发表在国际杂志Cell上题为“Dissecting the contribution of host genetics and the microbiome in complex behaviors”的研究报告中,来自美国贝勒医学院等机构的科学家们通过研究发现,肠道中的微生物或许会诱发与复杂神经系统疾病相关的某些疾病症状,因此基于微生物的疗法未来或有望帮助治疗人类的神经系统疾病。
研究者Mauro Costa-Mattioli说道,机体不同的异常行为或许是由宿主的基因和其机体的微生物组进行相互依存调节的,具体而言,在神经发育障碍小鼠模型中,其多动行为是由宿主机体的遗传特性所空的,而社会行为缺陷则是由肠道微生物组所介导的。更重要的是,从治疗学的角度来讲,利用促进肠道中生物喋呤家族中特定化合物产生的特定微生物进行治疗,或者利用一种代谢活性的生物喋呤分子进行治疗,就能够改善机体的社会行为,但并不能改善机体的运动活性。
本文研究是否能激发科学家们治疗人类神经系统疾病的新突破呢?虽然现在说还为时尚早,但研究人员对其研究结果非常有信心,本文研究有望帮助研究人员开发安全且有效的新型疗法,利用选择性的益生菌菌株或细菌诱导的药物来靶向作用肠道微生物组。虽然研究人员对这些细菌作用机制研究越来越深入,他们将能够更精确、更加有效地利用这种力量来帮助治疗人类神经系统疾病。本文研究代表了该研究领域的一项中大奖金很赞,因为很多人类疾病,尤其是影响大脑的疾病目前仍然非常难以治疗。
尽管研究人员取得了一定的科学进步和关于基因操作的承诺,但目前仍然很难通过调节人类基因来治疗疾病,但调节机体的微生物组却是非常有趣且能作为一种非侵入性的替代策略;实际上,研究人员目前正在开展一项临床试验,旨在利用罗伊氏乳杆菌来治疗自闭症患儿。基于本文研究结果,后期研究人员将会继续深入研究开发基于微生物的新型策略来帮助治疗人类神经系统障碍或疾病。
【8】Cell Metabolism: 高膳食纤维通过改变肠道微生物改善母代肥胖引起子代认知和社交功能障碍
doi:10.1016/j.cmet.2021.02.002
据报道母亲在怀孕期间出现肥胖症状与后代的认知和神经发育障碍密切相关。然而,其根本机制仍不清楚且缺乏有效的干预措施。近日,来自西北农林科技大学的刘学波教授、刘志刚教授联合上海交通大学侯敏教授在Cell Metabolism杂志上发表题为High-fiber diet mitigates maternal obesity-induced cognitive and social dysfunction in the offspring via gut-brain axis的文章,发现高膳食纤维饮食可以通过影响肠道菌群及代谢产物,从而改善母代肥胖引起的子代认知和社交功能障碍。
这项以778名7-14岁儿童为对象的研究表明,母亲肥胖与儿童的低认知和社交能力密切相关。此外,小鼠模型中研究表明,母鼠的肥胖会破坏后代的社交行为和认知能力。接下来作者发现高纤维饮食可以通过减轻突触损伤和小胶质细胞成熟缺陷来恢复后代的社交行为和肠道微生物群。该研究表明,微生物-代谢-脑轴可能是母亲肥胖导致的子代认知和社会功能障碍的基础,高膳食纤维摄入量可能是一种有前景的干预措施。
【9】Science子刊解读!母爱的表现或源于母体机体的肠道菌群!
doi:10.1126/sciadv.abe6563
近日,一篇刊登在国际杂志Science Advances上题为“Microbiota control of maternal behavior regulates early postnatal growth of offspring”的研究报告中,来自Salk生物研究所等机构的科学家们通过对小鼠进行研究发现,母爱或源于机体肠道。也许没有什么比一个忽视自己孩子的母亲更加令人心碎和困惑的了;2017年,美国大约由67.5万名儿童遭受了虐待,其中75%的儿童处于被忽视的状态;出生后的最早几个月对于确保机体适当的生理和心理发育至关重要,在这一阶段被忽视的儿童往往会经历发育不良以及行为和学习的问题,那么有什么可能会颠覆母亲照顾其孩子的本能呢?
科学家们发现了一些生物和环境因素,其能够影响多种哺乳动物的母性行为,而且许多研究也都指出了催产素的不足,催产素是一种在分娩和哺乳期间母体机体中释放的激素,其有助于建立母子之间的联系,而血清素的缺乏也会干扰母性的本能,血清素是一种能调节机体情绪和抑郁症的关键神经递质。这项研究中,研究人员报道了一种影响母性行为的新的因素,即居住在母体肠道中的肠道菌群,这是一项耐人寻味的研究,研究人员利用小鼠的母亲及其后代进行了相关研究,他们发现了微生物从根本上改变自身行为的一种方式,包括一种本能,比如母性养育等。
目前还没有证据表明,这种大肠杆菌菌株在人类机体中发挥的作用与小鼠机体中的一样,从而影响母亲对其后代的关注度;此外,该研究是研究人员利用无菌小鼠进行的,而且小鼠体内仅有一种大肠杆菌菌株。尽管如此,这些研究发现还值得进一步研究人类母亲体内的微生物菌群如何影响可能影响后代福利的行为;如今看来,最佳的婴儿护理不仅仅需要关注婴儿的饮食,后期研究人员还需要考虑母亲体内微生物菌群的组成。医生普遍认为,健康的微生物菌群能通过合理的饮食来培养,包括丰富的纤维和发酵食物,以及定期锻炼等。
【10】Nature子刊解读!科学家在肠道微生物组中寻找能指示机体肝癌风险的特殊“标记”!
doi:10.1038/s41467-020-20422-7
近日,一篇刊登在国际杂志Nature Communications上题为“Gut microbiota impact on the peripheral immune response in non-alcoholic fatty liver disease related hepatocellular carcinoma”的研究报告中,来自新南威尔士大学等机构的科学家们通过研究发现,非酒精相关肝癌患者机体中存在一种特殊的肠道微生物组,其或能帮助预测患者的疾病风险。研究者指出,与非酒精性脂肪肝(NAFLD)相关的肝癌患者机体中特殊的肠道微生物组或是预测某些人群患癌症风险的关键。
研究者表示,肠道微生物组能够调节非酒精性脂肪肝肝癌患者机体的免疫反应,从而促进癌症的存活;虽然这项研究尚处于早期阶段,但这一发现或有望为患有非酒精性脂肪肝相关肝癌患者开发有效的预防性和治疗性策略。人们在肥胖和携带代谢性风险因素(糖尿病、高血压和高胆固醇)的情况下易患非酒精性脂肪肝。Amany Zekry说道,我们对最常见的原发性肝癌—肝细胞癌(HCC)进行了研究,其是全球人群癌症相关死亡的第三大原因。慢性肝炎或肝硬化(或肝脏疤痕)是患肝癌的关键,而且非酒精性脂肪肝是一个常见的风险因素;因此,由于全球肥胖和2型糖尿病的流行,目前非酒精性脂肪肝慢慢成为诱发肝脏疾病和肝癌的原因,尤其是在西方国家。(生物谷Bioon.com)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


