梗阻性肥厚型心肌病(oHCM)创新药!Camzyos补充新药申请在美国进入审查:减少对室间隔减容术的需求!
来源:生物谷原创 2022-10-26 16:33
Camzyos是美国FDA批准的首个心肌肌球蛋白抑制剂,靶向oHCM病理生理学。

图片来源:摄图网
2022年10月26日讯 /生物谷BIOON/ --百时美施贵宝(BMS)近日宣布,美国食品和药物管理局(FDA)已受理Camzyos(mavacamten)的补充新药申请(sNDA),以扩大适应症:用于减少对室间隔减容术(septal reduction therapy,SRT)的需要。FDA已将《处方药申报者付费法案》(PDUFA)的目标日期定为2023年6月16日。
Camzyos是一种新型、口服、心肌肌球蛋白选择性的别构可逆性抑制剂,于2022年4月获得美国FDA批准:用于治疗纽约心脏协会(NYHA)心功能分级为II-III级的有症状梗阻性肥厚型心肌病(oHCM)成人患者,以改善功能和症状。
值得一提的是,Camzyos是美国FDA批准的首个心肌肌球蛋白抑制剂,靶向oHCM病理生理学。oHCM是一种高发病率的慢性心脏病。此前,FDA授予了Camzyos治疗oHCM的突破性药物资格。联拓生物(LianBio)获得了百时美施贵宝旗下全资子公司MyoKardia的许可授权,在大中华区、泰国和新加坡对mavacamten进行开发和商业化。2022年2月,国家药监局药品审评中心(CDE)授予了mavacamten治疗oHCM的“突破性治疗药物”认证。
此次sNDA基于VALOR-HCM 3期研究(NCT04349072)的结果。这是一项随机、双盲、安慰剂对照、多中心3期研究,在符合2011年ACC/AHA SRT指南标准、且已被转诊进行侵入性手术的有症状梗阻性HCM、(NYHA III-IV级)患者中对Camzyos进行了评估。该研究共入组了100多例患者,这些患者以1:1的比例随机分配,接受mavacamten或安慰剂治疗。该研究包括3个治疗期,共128周:16周安慰剂对照期,16周积极治疗期(所有患者将接受mavacamten治疗),96周长期扩展期(所有患者继续接受mavacamten治疗)。
该研究的主要终点是:mavacamten治疗组与安慰剂组相比,第16周之前或第16周决定进行SRT的患者人数以及第16周仍然符合SRT指南标准(LVOT梯度≥50mmHg和NYHA III-IV级)的患者人数的复合。关键次要终点包括:治疗第16周对运动梯度LVOT、NYHA分级、堪萨斯城心肌病问卷(KCCQ)、生物标志物的影响。
结果显示,VALOR-HCM研究达到了主要终点和所有次要终点,具有高度统计学意义。mavacamten的安全性与之前的研究一致,未观察到新的安全信号。
百时美施贵宝全球药物开发高级副总裁兼心血管开发主管Roland Chen表示:“目前,推荐许多严重的有症状梗阻性肥厚型心肌病患者进行室间隔减容术(SRT)。这通常需要心脏直视手术或间隔消融手术,这2种都是专有的护理选择。今年早些时候,Camzyos的批准标志着一个重要里程碑。此次FDA受理这一扩大适应症的申请,有潜力加强Camzyos的特征,同时进一步加强我们向患者提供变革性心血管治疗的承诺。”
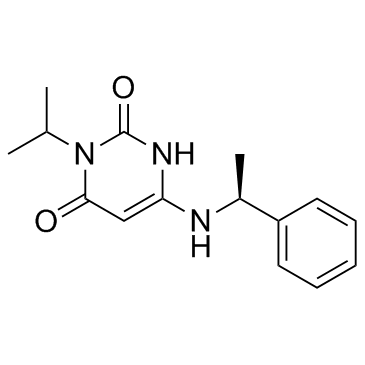
mavacamten化学结构式(图片来源:chemsrc.com)
肥厚型心肌病(HCM)是一种由心肌过度收缩和左心室血液充盈受阻引起的慢性进行性疾病,可导致衰弱症状和心脏功能障碍。据估算,全球每500人中就有1位HCM患者。HCM最常见的原因是心肌肌节蛋白的突变。在梗阻性或非梗阻性HCM患者中,劳力可导致疲劳或呼吸困难,影响患者的日常生活。HCM还与房颤、中风、心力衰竭和心源性猝死风险的增加有关。
梗阻性HCM(obstructive HCM,oHCM)是最常见的HCM类型,血液离开心脏的左心室流出道(LVOT)被增大的心肌阻塞。据估计,在全球范围内,oHCM影响40000-600000人,但许多患者仍未确诊和/或无症状。
mavacamten是一种首创的(first-in-class)、口服、心肌肌球蛋白别构调节剂,用于治疗以心脏过度收缩和心脏舒张充盈受损为内在原因的疾病。mavacamten通过抑制过度的肌球蛋白-肌动蛋白横桥(myosin-actin cross-bridge)的形成来降低心肌收缩力,而过度的肌球蛋白-肌动蛋白横桥的形成可导致心肌收缩过度、左心室肥厚和顺应性降低。在临床和临床前研究中,mavacamten持续表现出降低心壁应力的生物标志物,减轻过度的心肌收缩、增加舒张顺应性。
mavacamten最初开发用于治疗有症状的梗阻性肥厚型心肌病(oHCM)。基于其作用机制和治疗活性证据,mavacamten也正在临床上研究用于治疗有症状的非梗阻性HCM和射血分数保留的心力衰竭(HFpEF)。
mavacamten(MYK-461)由MyoKardia公司开发。2020年10月,百时美施贵宝宣布以131亿美元现金、溢价60%将MyoKardia收购,该笔交易于2020年11月完成。值得注意的是,2020年8月11日,由投资公司Perceptive Advisors孵化的联拓生物(LianBio)正式成立,同日宣布达成2项重要合作,一项为引进BridgeBio Pharma的产品管线到中国,另一项即为引进MyoKardia公司的mavecamten到中国。
2022年2月,联拓生物宣布,国家药品监督管理局(NMPA)药品审评中心(CDE)授予mavacamten“突破性治疗药物”认证,用于治疗梗阻性肥厚型心肌病(oHCM)。目前,中国估计约有110万至280万肥厚型心肌病患者,除有限的症状缓解治疗方法外,尚无有效药物治疗选择。在全球3期临床试验中,mavacamten显示出改变oHCM患者病程和恢复心脏功能的潜力。(生物谷Bioon.com)
原文出处:U.S. Food and Drug Administration (FDA) Accepts Supplemental New Drug Application for CAMZYOS? (mavacamten) in Symptomatic Obstructive Hypertrophic Cardiomyopathy to Reduce the Need for Septal Reduction Therapy
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


