国产CAR-T!首创FasT CAR-19治疗B细胞急性淋巴细胞白血病完全缓解率95.8%,制备仅需1天!
来源:本站原创 2019-09-20 10:01
2019年09月20日讯 /生物谷BIOON/ --亘喜生物科技集团(Gracell Bio)是一家位于上海的临床阶段免疫细胞治疗公司。近日,该公司公布了一项多中心试点研究的阳性结果,该研究旨在评估其首创(first-in-class)FasT CAR-19(GC007F)研究性细胞基因疗法的安全性和疗效。结果在9月10-13日在波士顿举行的CAR-TCR峰会上公布。目前,抗CD19 CAR-T生

2019年09月20日讯 /生物谷BIOON/ --亘喜生物科技集团(Gracell Bio)是一家位于上海的临床阶段免疫细胞治疗公司。近日,该公司公布了一项多中心试点研究的阳性结果,该研究旨在评估其首创(first-in-class)FasT CAR-19(GC007F)研究性细胞基因疗法的安全性和疗效。结果在9月10-13日在波士顿举行的CAR-TCR峰会上公布。
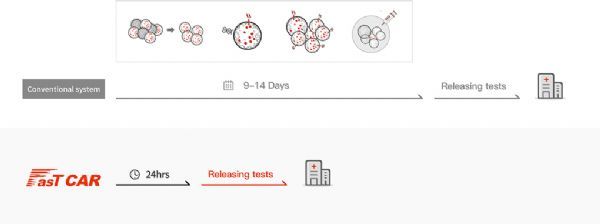
目前,抗CD19 CAR-T生物过程平均需要2周时间来生产、7天时间才能通过质量检测。然而,Gracell公司的FasT CAR解决方案,通过对患者T细胞进行基因修饰以表达CD19特异性嵌合抗原受体(CAR)的定制治疗,制备时间可缩短至一天,制造成功率为26/26(100%),没有1例受试者产品制备失败。
FasT CAR技术也可用于其他免疫细胞项目,如治疗多发性骨髓瘤(MM)和非霍奇金淋巴瘤(NHL)。利用这些优点,FasT CAR-19具有高度的成本效益,并且具有相当大的潜力在CAR-T治疗复发性或难治性B细胞急性淋巴细胞白血病(r/r B-ALL)中成为一种新的标准。
FasT CAR技术相对于常规CAR技术的优势:生产时间由9-14天缩短至1天
这项多中心研究入组了26例年龄在14-70岁之间的青少年和成人患者,他们都患有r/r B-ALL,并且对先前的多个治疗方案都没有反应。截至9月4日,所有患者在淋巴消耗性化疗后接受一次FasT CAR-19的输注。FasT CAR-19的剂量从低到高,分别相当于B-ALL常规CAR-T治疗剂量的1/30-1/10。
在28天的随访中,对24例接受治疗的患者进行了疗效评估,其中:23例(95.8%)取得了有或无完全血细胞计数恢复的完全缓解(CR/CRi);21例(87.5%)检测不到微小残留病(uMRD,骨髓中可检测到的白血病细胞<1/10000个白血细胞)。
在超过三个月的持久缓解期内,FasT CAR-19表现出良好的持久性。在安全性方面,26例患者均能耐受不同剂量的FasT CAR-19单次输注。最常见的安全性问题是细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS),观察到的为轻度至中度副作用。
与高剂量组相比,低至中剂量组的患者出现轻度不良反应。在低至中剂量组的20例患者中,只报告了2例(10%)3级CRS和2例(10%)可管理的3级ICAN;而在高剂量组的6例患者中,有5例(83.3%)3级CRS和1例(16.7%)1-2级ICAN,表明存在剂量限制性毒性。
Gracell首席执行官曹卫博士表示:“我们非常兴奋地看到,在这项研究中,难治性或复发性B-ALL患者从FasT CAR-19治疗中获得了实质性的临床益处。使用FasT CAR平台制造的Dual CAR-T细胞有可能提供更多的临床益处。下一阶段将是通过首次人体试验来释放这些益处。”(生物谷Bioon.com)
原文出处:Gracell Announces Interim Readout of Investigation for First-in-class FasT CAR-19 in patients with Relapsed or Refractory B-cell Acute Lymphoblastic Leukemia and Extension in Use of FasT CAR to Other Immune Cell Programs
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
87%用户都在用生物谷APP 随时阅读、评论、分享交流 请扫描二维码下载->