Nature:揭示APOE4基因导致少突胶质细胞中脂质失调,破坏神经元髓鞘化,从而增加患阿尔茨海默病风险
来源:生物谷原创 2022-11-25 09:35
APOE4基因会让一个人患阿尔茨海默病风险显著增加。在一项新的研究中,来自美国麻省理工学院的研究人员提供了一些新的答案,作为证实APOE4对大脑中不同细胞类型的影响的更广泛研究的一部分。
众所周知,携带APOE4基因变体的一个拷贝会使一个人患阿尔茨海默病的风险增加三倍,携带它的两个拷贝会让这种风险增加十倍左右,但是这其中的根本原因以及做些什么来帮助患者在很大程度上仍是未知。在一项新的研究中,来自美国麻省理工学院的研究人员提供了一些新的答案,作为证实APOE4对大脑中不同细胞类型的影响的更广泛研究的一部分。相关研究结果于2022年11月16日在线发表在Nature期刊上,论文标题为“APOE4 impairs myelination via cholesterol dysregulation in oligodendrocytes”。论文通讯作者为麻省理工学院皮考尔学习与记忆研究所主任Li-Huei Tsai教授和麻省理工学院计算机科学教授Manolis Kellis博士。

这项新研究结合了来自死后人脑、实验室人脑细胞培养物和阿尔茨海默病模型小鼠的证据,显示当人们携带APOE4的一个或两个拷贝,而不是更常见的、风险中性的APOE3基因变体时,称为少突胶质细胞的细胞会错误地管理胆固醇,无法运送这种脂肪分子来包裹神经元投射的长藤状轴突“线路”来建立大脑回路连接。这种称为髓鞘(myelin)的脂肪绝缘层的缺乏可能是导致阿尔茨海默病的病理和症状的一个重要因素,因为没有适当的髓鞘,神经元之间的通信就会退化。
由麻省理工学院皮考尔学习与记忆研究所主任Li-Huei Tsai教授领导的一个研究团队最近的研究已发现APOE4如何破坏关键脑细胞类型(包括神经元、星形胶质细胞和小胶质细胞)处理脂肪分子(称为脂质)的独特方式。在这项新的研究和之前的那些研究中,该团队在实验室中确定了可以校正这些不同问题的化合物,有潜力开发出基于药物的治疗策略。
这项新的研究不仅通过发现APOE4如何破坏髓鞘化而扩展了之前的那项研究,而且还通过使用单核RNA测序(snRNAseq)提供了第一个涉及主要脑细胞类型的系统分析,以比较携带APOE4拷贝的人的基因表达与携带APOE3拷贝的人相比有何不同。
Tsai说,“利用以基因型特定的方式从死后人类大脑中获得的snRNAseq数据,这篇论文非常清楚地显示APOE4对不同脑细胞类型的影响非常明显。我们观察到脂质代谢受到破坏的趋同性,但是当你真正进一步研究不同脑细胞类型中受到破坏的脂质途径类型时,它们都是不同的。我觉得脂质失调可能是我们观察到的许多病理现象背后的非常基本的生物学特性。”
研究髓鞘化的许多方法
死后人脑样本来自于宗教秩序研究(Religious Orders Study)和拉什大学记忆与衰老项目(Rush Memory and Aging Project.)。该团队的snRNAseq数据包含了来自32人前额叶皮层的11种不同类型的16万多个细胞---12人携带两个APOE3拷贝,12人携带一个APOE3拷贝和一个APOE4拷贝,还有8人携带两个APOE4拷贝。携带APOE3/3和携带APOE3/4的死后人脑样本在阿尔茨海默病的诊断、性别和年龄方面是平衡的。所有APOE4/4携带者都患有阿尔茨海默病,总共8人中有5人是女性。
一些结果反映了已知的阿尔茨海默氏症病理,但其他模式是新的。其中的一项结果显示携带APOE4的少突胶质细胞表现出更多的胆固醇合成基因的表达和遭受胆固醇转运破坏。人们携带的APOE4拷贝越多,这种影响就越大。鉴于Tsai和Kellis实验室在2019年的一项先前研究(Nature, 2019, doi:10.1038/s41586-019-1195-2)已显示将阿尔茨海默病与少突胶质细胞中髓鞘化基因的表达减少联系起来,这一点特别有趣。
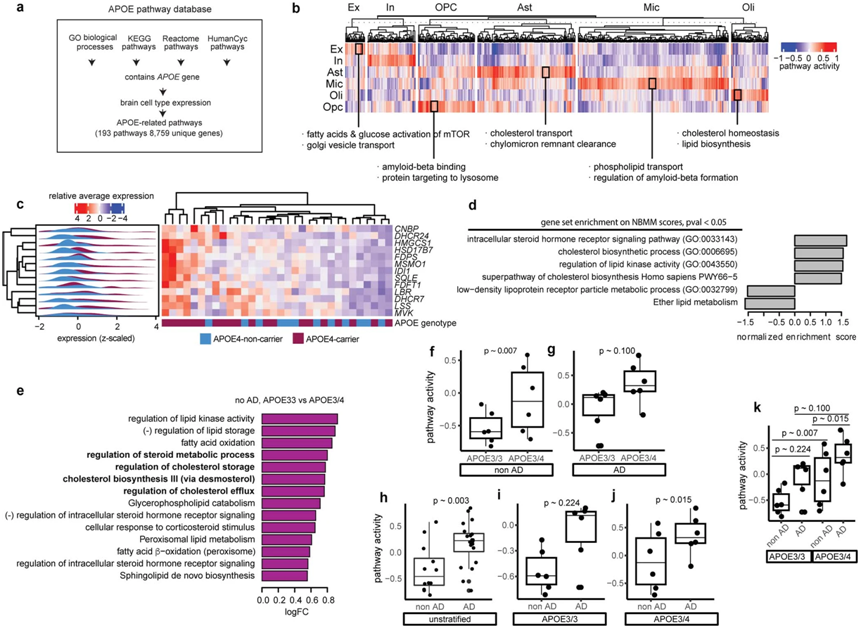
APOE4和阿尔茨海默病中APOE相关的脂质通路变化。图片来自Nature, 2022, doi:10.1038/s41586-022-05439-w。
通过使用多种技术直接观察死后人脑组织,这些作者观察到在携带APOE4的大脑中,异常数量的胆固醇在细胞内积累,特别是少突胶质细胞,但在神经轴突周围相对缺乏。
为了了解其中的原因,这些作者使用患者衍生的诱导性多能干细胞来产生经过基因改造后携带APOE4或APOE3的少突胶质细胞的实验室细胞培养物。同样地,携带APOE4的少突胶质细胞显示出主要的脂质破坏。特别是,携带APOE4的少突胶质细胞在细胞内积累了额外的胆固醇,显示出额外的内部脂肪对在胆固醇运输方面发挥一定作用的称为内质网的细胞器造成了应激,并且确实减少了胆固醇转运到它们的细胞膜。随后,当与神经元共同培养时,携带APOE4的少突胶质细胞未能像携带APO3的少突胶质细胞那样使神经元髓鞘化,而不管神经元携带APOE4或APOE3。
这些作者还观察到,在死后的大脑中,APOE4携带者的髓鞘化程度比APOE3携带者低。例如,在携带APOE4的大脑中,穿过胼胝体(连接大脑半球的结构)的轴突周围的髓鞘明显变薄。同样的情况也发生在经过基因改造后携带人类APOE4的小鼠身上而不是经过基因改造后携带APOE3的小鼠身上。
富有成效的干预措施
因渴望找到一种潜在的干预措施,这些作者专注于影响胆固醇的药物,包括抑制胆固醇合成的他汀类药物和有助于胆固醇转运的环糊精。他汀类药物没有帮助,但将环糊精应用于在培养皿中培养的携带APOE4的少突胶质细胞减少了细胞内胆固醇的积累,并改善了与少突胶质细胞一起培养的神经元的髓鞘化。此外,它在携带APOE4的小鼠身上也有这些效果。
最后,这些作者用环糊精处理了一些携带APOE4的小鼠,其他的携带APOE4的小鼠没有接受这种处理,并让所有携带APOE4的小鼠都接受了两种不同的记忆测试。经环糊精处理的携带APOE4的小鼠在这两项测试中的表现都明显更好,这表明神经元髓鞘化的改善和认知能力的提高之间存在关联。
Tsai说,这些研究结果清晰地表明通过干预措施校正携带APOE4的少突胶质细胞中的特定脂质失调可能有助于抵消APOE4对阿尔茨海默病的促进作用。
Tsai说,“令人鼓舞的是,我们观察到一种在实验室和小鼠模型中拯救少突胶质细胞功能和髓鞘化的方法。但除了少突胶质细胞,我们可能还需要找到临床上有效的方法来处理小胶质细胞、星形胶质细胞和血管,以真正对抗这种疾病。”(生物谷 Bioon.com)
参考资料:
Joel W. Blanchard et al. APOE4 impairs myelination via cholesterol dysregulation in oligodendrocytes, Nature, 2022, doi:10.1038/s41586-022-05439-w.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


