有望成为新标准疗法!长效补体抑制剂获批扩展适应症
来源:药明康德 2019-10-21 12:21
日前,Alexion Pharmaceuticals公司宣布,美国FDA批准该公司的长效C5补体抑制剂Ultromiris(ravulizumab-cwvz)扩展适应症,用于治疗非典型溶血尿毒综合征(aHUS)患者(年龄一个月以上)的补体介导血栓性微血管病(TAM)。这是Ultomiris首次获批用于治疗儿科患者。aHUS是一种罕见疾病,由于补体通路不受控制地被激活,导致血
日前,Alexion Pharmaceuticals公司宣布,美国FDA批准该公司的长效C5补体抑制剂Ultromiris(ravulizumab-cwvz)扩展适应症,用于治疗非典型溶血尿毒综合征(aHUS)患者(年龄一个月以上)的补体介导血栓性微血管病(TAM)。这是Ultomiris首次获批用于治疗儿科患者。
aHUS是一种罕见疾病,由于补体通路不受控制地被激活,导致血管壁损伤和产生血块。患者症状表现为身体重要器官的进行性损伤,最主要的受损器官为肾脏。它能够导致器官功能突然衰竭,或者逐渐丧失,患者可能需要器官移植。aHUS影响成人和儿童患者,其中很多患者病情危急,需要在急救室接受透析等护理。抑制不受控制的补体激活是治疗这一疾病的当务之急。
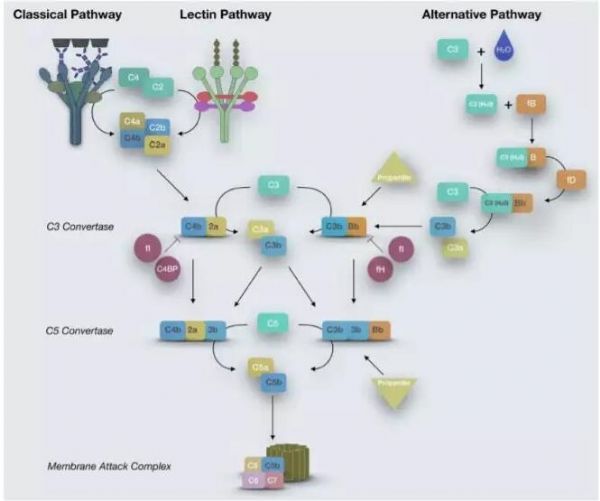
Ultomiris是Alexion公司开发的长效C5补体抑制剂,它通过抑制补体级联通路的效应蛋白C5来抑制补体信号通路的激活。患者只需每8周接受一次注射就可以有效抑制补体信号通路的激活。它已经获得FDA批准,治疗阵发性睡眠性血红蛋白尿症(PNH)。
这一批准是基于两项全球性,单臂开放标签研究的结果,其中包括一项成人临床试验和一项儿科患者临床试验。试验结果表明,在最初为期26周的疗程后,54%的成人患者和71%的儿童患者出现血栓性微血管病(TAM)的完全缓解。而且,
Ultomiris在84%的成人和93%的儿童患者中减少血小板减少症;
在77%的成人和86%的儿童患者中减少溶血;
在59%的成人和79%的儿童患者中改善肾功能(儿童患者数据皆为中期数据)。
“不受控制的补体激活会带来器官衰竭以及死亡的严重后果,对aHUS患者和他们的家人来说,是一个严峻挑战,”Alexion公司执行副总裁兼研发负责人John Orloff医学博士说:“基于3期临床试验数据,我们相信Ultomiris具有成为治疗这一灾难性疾病的新标准疗法的潜力。”(生物谷Bioon.com)
小编推荐会议 2019无锡国际生物医药论坛暨第九届Cell Death & Disease国际研讨会-新药研发
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。