Science子刊:新型RNA靶向化合物有望治疗C9 ALS/FTD
来源:本站原创 2021-10-31 23:23
在一项新的研究中,来自美国斯克里普斯研究所、佛罗里达大学、佛罗里达大西洋大学、梅奥诊所和约翰霍普金斯大学医学院的研究人员利用斯克里普斯研究所化学家Matthew Disney博士实验室设计的一种潜在药物分子成功地治疗了小鼠所患的遗传疾病C9 ALS/FTD。
2021年10月31日讯/生物谷BIOON/---肌萎缩侧索硬化症(ALS)和额颞叶痴呆的最常见遗传形式之一被称为C9 ALS/FTD,因引起该病的9号染色体上的DNA重复序列而得名。在一项新的研究中,来自美国斯克里普斯研究所、佛罗里达大学、佛罗里达大西洋大学、梅奥诊所和约翰霍普金斯大学医学院的研究人员利用斯克里普斯研究所化学家Matthew Disney博士实验室设计的一种潜在药物分子成功地治疗了小鼠所患的这种遗传疾病。相关研究结果发表在2021年10月27日的期刊上,论文标题为“Ribonuclease recruitment using a small molecule reduced c9ALS/FTD r(G4C2) repeat expansion in vitro and in vivo ALS models”。
ALS也被称为路格里克氏病(Lou Gehrig’s disease),它导致运动神经元的逐渐丧失,而运动神经元是连接肌肉和中枢神经系统的细长的神经细胞。随着运动神经元的死亡,瘫痪、肌肉萎缩、吞咽困难和最终呼吸困难都会发生,最终导致死亡。科学家们正在了解ALS有多种原因,其中一些是散发性的,一些是遗传性或家族性的。
额颞叶痴呆同样也有家族性和散发性的原因。它涉及大脑额叶和颞叶神经元的渐进性损害。症状可能包括行走困难或奇怪的行为和情绪状态。与ALS一样,额颞叶痴呆也没有治愈方法。
一种疾病,多种症状
虽然额颞叶痴呆患者在外表上看起来与ALS患者的疾病完全不同,但那些由C9重复序列引起的疾病是相同的。表现形式因受影响的细胞类型而异。序列重复的次数越多,疾病症状就越早、越严重。
这种致病突变涉及核苷酸鸟嘌呤和胞嘧啶的重复,特别是9号染色体上GGGGCC片段的重复,虽然额颞叶痴呆患者在外表上看起来与ALS患者的疾病完全不同,但那些由C9重复序列引起的疾病是相同的。表现形式因受影响的细胞类型而异。序列重复的次数越多,疾病症状就越早、越严重。这种致病性重复序列的数量可以从大约60个到数千个不等。遗传了患病基因的人可以患上成ALS、FTD或两者都有。已有研究估计,约有1/5被诊断为家族性ALS的人,以及约1/10的家族性FTD患者携带C9突变。症状发作的平均年龄为58岁。
Disney说,“这是一种家族性的疾病。根据重复序列的数量,医生可以评估患者是否会受到这种疾病的影响。因此,在患者出现症状之前,你就知道他们有很高的发病可能性,然而却没有任何治疗方法。这使得开发可以一种疾病治疗方法变得更加迫切。”
团队努力
为了评估这种潜在药物分子的有效性,这些作者需要诊断生物标志物和携带C9突变的患者源性神经元。梅奥诊所的Leonard Petrucelli团队已经广泛研究了C9 ALS/FTD,并开发了诊断生物标志物。约翰霍普金斯大学医学院的Jeffrey D. Rothstein团队治疗和研究ALS,并提供了干细胞,然后Disney实验室将这些干细胞转变成显示出致病性GGGGCC重复序列的神经元。
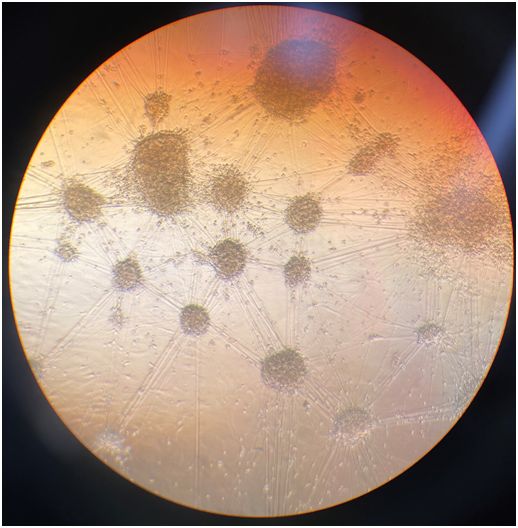
为了研究这种化合物的有效性,科学家们将ALS患者的细胞转化为诱导性多能干细胞,然后将它分化为神经元。图片来自Science Translational Medicine (2021). DOI: 10.1126/scitranslmed.abd5991。
在他们的研究中,Disney团队设计了一种靶向导致该疾病的基因转录所涉及的RNA的化合物。该化合物导致这种致病性RNA和细胞用来消除RNA的途径之间的相互作用。该化合物消除了患有该疾病的小鼠中70%的有毒蛋白片段,并从患者衍生的神经元中消除了该疾病的大多数特征。
论文第一作者、斯克里普斯研究所斯卡格斯化学生物学研究所研究生Jessica Bush说,“在小鼠体内注射一针,在整个研究期间都显示出益处,研究期为六周。”
Bush说,“我认为这非常令人兴奋,我们可以审视像ALS这样的疾病,通过采取不同的方法或新的视角,我们可以打开通往全新的可能性世界的大门,并开始走向治疗之路。”
发现背后的基础科学
Disney通过应用他的团队近15年来在RNA上寻找药物可靶向结构的研究来设计这种化合物,并建立一个能够结合这些药物可靶向结构的化合物文库。
这种成功的化合物通过在多个地方与这种致病性的RNA紧密结合而发挥作用,同时还吸引了一种降解RNA的酶。自然界显然创造了这种降解酶来保卫细胞免受病毒感染,并为蛋白产生提供质量控制。
Disney说,“我们利用一种自然过程来消除致病性RNA。对用该化合物处理的细胞中的RNA的全面分析表明,它是非常特异性和有选择性的。”
Disney补充说,将这项技术推进到可以在人类身上进行测试的程度需要大量的额外测试和完善,这个过程可能需要几年时间。
他说,“我们有可能最终在这些患者出现症状之前对他们进行治疗,但在进入临床之前,这还有很长的路要走。”(生物谷 Bioon.com)
参考资料:
Jessica A. Bush et al, Ribonuclease recruitment using a small molecule reduced c9ALS/FTD r(G 4 C 2 ) repeat expansion in vitro and in vivo ALS models, Science Translational Medicine (2021). DOI: 10.1126/scitranslmed.abd5991.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



