精准击杀多种癌症,“合成致死”新疗法来了!已进入临床阶段
来源:学术经纬 2025-05-01 14:13
研究表明,TNG462对于MTAP缺失的癌症表现出强大的治疗潜力。
编者按:两个基因缺陷协同导致细胞死亡的“合成致死”现象,已经成为癌症治疗的新兴策略。在两项发表于Journal of Medicinal Chemistry的近期研究中,Tango Therapeutics的研究团队报告了一种全新的PRMT5抑制剂——TNG462,并且描述了此类抑制剂的设计机制。
TNG462的设计源自对上一代分子的改造,论文指出,TNG462的效力、选择性更强,分子的DMPK(吸收、分布、代谢、排泄)特性也得到改善。根据论文介绍,药明康德为相关研究的化合物合成、多项体外分析提供了赋能支持。目前,TNG462治疗MTAP缺失的胰腺癌、肺癌等非中枢神经系统肿瘤的I/II 期临床试验正在进行。
1922年,哥伦比亚大学的生物学家Calvin Bridges博士在观察果蝇时,注意到一个有趣的现象:两个基因同时突变失活,会导致果蝇死亡;但是如果只含有其中一个基因缺陷,果蝇的生存却不受影响。这种基因协同导致细胞死亡的现象,在此后被称作合成致死(synthetic lethality)。
如今,合成致死已经成为癌症治疗的新兴热门方向。2014年,首款PARP抑制剂奥拉帕尼(Olaparib)获批上市,用于治疗BRCA1或BRCA2突变的乳腺癌,“合成致死”的概念终于走向了现实。
此后,又有多个基于合成致死机制的靶点问世,PRMT5就是其中的一支“潜力股”。
PRMT5的全称是蛋白质精氨酸甲基转移酶5。作为一种参与调控基因表达、RNA剪接、细胞周期等过程的甲基转移酶,PRMT5在多种癌症中过度表达,促进肿瘤生长。而与PRMT5协同作用的“合成致死搭档”,则是甲硫腺苷磷酸化酶(MTAP)。
MTAP基因缺失是一类常见的癌症突变,大约10%~15%的人类癌症中都有这一突变。MTAP缺失时,细胞内的反应底物甲硫腺苷(MTA)不断积累,它们与PRMT5结合形成PRMT5/MTA复合物,抑制PRMT5的活性。因此,如果能设计一种只在PRMT5-MTA复合物存在时发挥作用的抑制剂,就可以选择性杀死MTAP缺失的癌细胞,同时避免对正常细胞的损伤。

在最新研究中,Tango Therapeutics的研究团队正是基于这一机制开展了药物分子设计。这项研究的起点,是该团队在2024年报告的一种基于MTA协同机制的PRMT5抑制剂。为了进一步提高这款PRMT5抑制剂的体内疗效,研究团队在该初始分子基础上进行优化设计,试图大幅提高活力效力、增加选择性并且延长体内半衰期。
研究团队首先观测了初始分子与PRMT5结合的晶体结构中,从中发现了3个可以重点优化的区域。如下图的A、B、C区域所示,分别是位于MTA结合位点附近的氨基吡啶、靠近哌啶环4号位的疏水小口袋,以及苯并噻唑环附近的极性残基。
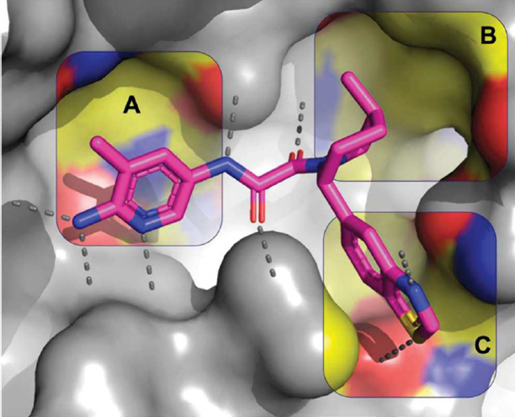
▲研究团队发现了3个可重点优化的结构区域(图片来源:参考资料[1])
接下来,作者依次对3个区域进行了大量优化设计以及化合物筛选。最终,在C区域的一项优化方案——使用N-甲基哌啶环进行取代得到的化合物51,在所有化合物中表现出了最强的效力以及良好的稳定性。而在化合物51基础上微调得到的TNG462,其效力得到进一步的提升,同时还具备高度选择性和良好的稳定性。
在体外实验中,TNG462的选择性达到了初始分子的45倍。而在犬类和食蟹猴模型实验中,研究团队评估了TNG462的药代动力学特征,其表现出中等清除率和生物利用度,并且预测的人体半衰期超过24小时,支持每日一次给药。在小细胞肺癌的异种移植模型中,TNG462表现出了强大的抗肿瘤活性,在不同给药模式下的肿瘤生长抑制率达96%,超过60%的肿瘤消退。最后,研究团队介绍了TNG462的合成路线与工艺优化。
基于上述优势,TNG462对于MTAP缺失的癌症表现出强大的治疗潜力。目前,TNG462治疗MTAP缺失的胰腺癌、肺癌等非中枢神经系统肿瘤的I/II 期临床试验正在进行。此外,根据Tango Therapeutics官网介绍,TNG462分别与RASi、帕博利珠单抗(Pembrolizumab)和SOC化疗联合使用,以及单独治疗胶质母细胞瘤的临床前试验已经完成,计划于2025年进行患者招聘。

值得一提的是,在不久前的另一篇Journal of Medicinal Chemistry论文中,该团队介绍了通过基于结构的设计工作,将S-腺苷-L-甲硫氨酸(SAM)协同的PRMT5抑制剂改造为MTA协同PRMT5抑制剂的策略。MTA与SAM竞争性结合PRMT5,但相对于PRMT5-SAM复合物,PRMT5-MTA复合物的选择性抑制可导致对MTAP缺失癌细胞的选择性杀伤。这项研究也为TNG462等新型MTA协同PRMT5抑制剂的发现奠定了基础。
参考资料:
[1] Cottrell et al., Discovery of TNG462: A Highly Potent and Selective MTA-Cooperative PRMT5 Inhibitor to Target Cancers with MTAP Deletion. Journal of Medicinal Chemistry (2025). DOI: 10.1021/acs.jmedchem.4c03067
[2] Cottrell et al., MTA-Cooperative PRMT5 Inhibitors: Mechanism Switching Through Structure-Based Design. Journal of Medicinal Chemistry (2025). DOI: 10.1021/acs.jmedchem.4c01998
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



