《柳叶刀》:中山大学领衔,中国原创抗癌新药——双抗ADC,晚期鼻咽癌治疗新选择
来源:生物世界 2025-10-22 10:17
这是全球首项在经多线治疗失败的晚期鼻咽癌患者中开展的随机 3 期临床研究,也是首个证明双特异性 ADC 临床获益的 3 期临床研究。
2025 年 10 月 19 日,国际顶尖医学期刊《柳叶刀》发表了一项中国原创抗癌新药的 3 期临床试验结果。
这项由中山大学肿瘤防治中心牵头、全国 55 家医院共同完成的 3 期临床试验显示,新型双特异性抗体偶联药物(bispecific ADC)——伦康依隆妥单抗(izalontamab brengitecan,iza-bren)在经多线治疗失败的晚期鼻咽癌患者中,疗效显著优于标准化疗。
中山大学肿瘤防治中心张力教授为论文通讯作者,中山大学肿瘤防治中心杨云鹏主任医师、周华强副主任医师、唐林泉主任医师、福建省肿瘤医院邱素芳教授、湖南省肿瘤医院韩亚骞教授为论文共同第一作者。

治疗困境:晚期鼻咽癌亟需新方案
鼻咽癌是一种具有明显地域特征的恶性肿瘤,中国尤其是华南地区高发。2022 年全球数据显示,每年新增病例约 12 万例,死亡约 7.3 万例。
虽然早期鼻咽癌患者 5 年生存率可达 85%,但一旦发生复发或转移,治疗就变得异常棘手。目前,铂类化疗药物联合 PD-1/PD-L1 抑制剂是一线标准方案,但多数患者最终会产生耐药。
对于经过多线治疗失败的晚期鼻咽癌患者,现有治疗方案效果有限,预后极差,急需新的治疗选择。
作用机制:双特异性 ADC 的精准杀伤原理
伦康依隆妥单抗(izalontamab brengitecan,iza-bren)是一种 First in Class 的双特异性抗体偶联药物(双抗 ADC),由四川百利天恒药业股份有限公司研发,这也是全球首个进入临床试验阶段的 EGFR×HER3 双特异性抗体偶联药物。
该药物由一个 EGFR×HER3 双特异性抗体通过可裂解连接子与拓扑异构酶 I 抑制剂(Ed-04)有效载荷连接而成。该药物可同时特异性靶向 EGFR 和 HER3 两个肿瘤相关抗原,内化进入肿瘤细胞,释放高效拓扑异构酶 I 抑制剂(Ed-04),破坏 DNA 复制和 RNA 合成,最终诱导肿瘤细胞死亡。其药物-抗体比(DAR)高达 8,意味着每个抗体可携带更多抗癌药物。
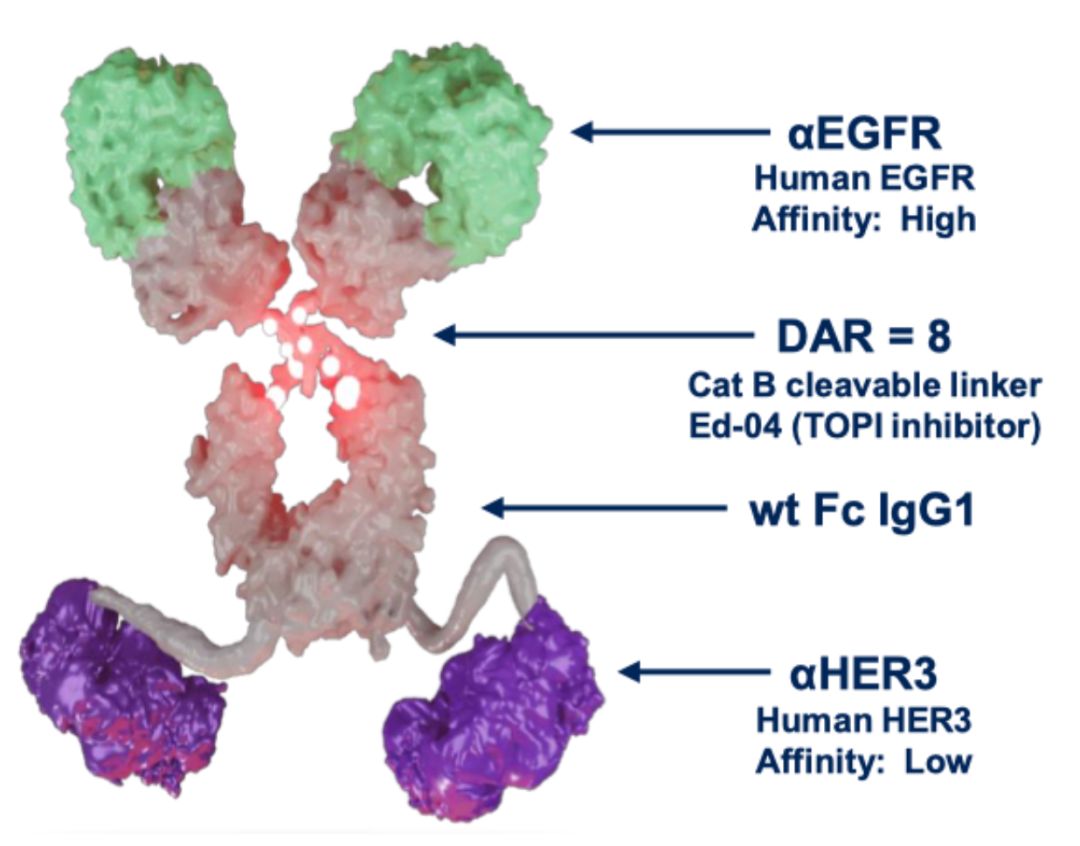
iza-bren 的结构
值得一提的是,该药物与国际制药巨头百时美施贵宝(BMS)达成了总额高达 84 亿美元的合作,高达 8 亿美元的首付款刷新了国产创新药单个项目出海纪录。
突破性结果:有效率翻倍,生存期显著延长
这项多中心、随机、开放标签的 3 期临床试验于 2023 年 12 月至 2025 年 2 月期间,筛选了 522 例患者,最终纳入 386 例符合条件的晚期鼻咽癌患者。
入组患者均为至少接受过两线系统化疗(包括含铂方案和 PD-1/PD-L1 抑制剂)后疾病进展的难治性患者。他们被随机分为两组:191 例接受 Iza-bren 治疗,195 例接受医生选择的化疗(卡培他滨、吉西他滨或多西他赛)。
截至 2025 年 3 月 30 日的数据显示,Iza-bren 治疗组的中位随访时间为 7.66 个月,化疗组为 7.10 个月。
最令人振奋的结果出现在肿瘤缩小率方面:Iza-bren 治疗组的客观缓解率高达 54.6%,而化疗组仅为 27.0%。这意味着超过一半的难治性晚期鼻咽癌患者的肿瘤显著缩小。
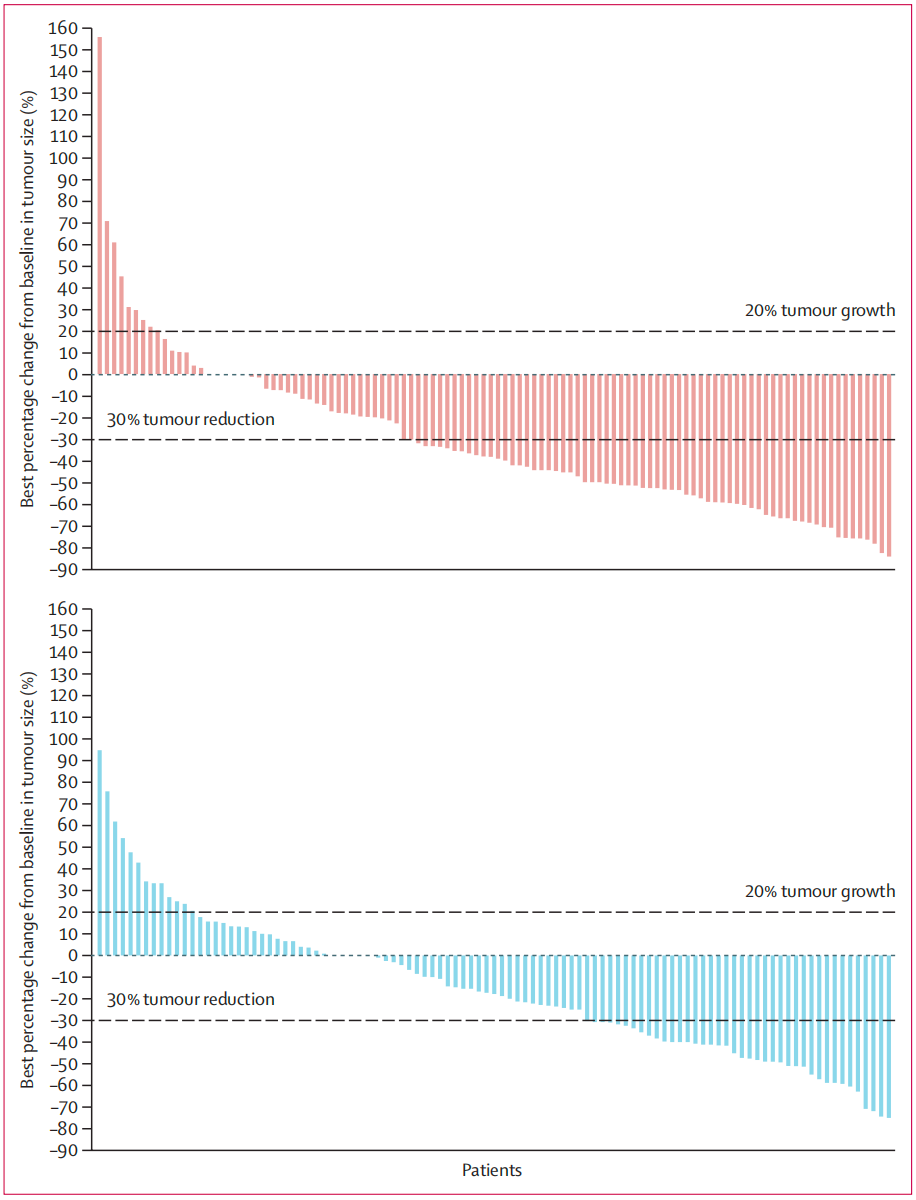
在无进展生存期方面,Iza-bren 治疗组同样表现优异:中位无进展生存期为 8.38 个月,对比化疗组的 4.34 个月,延长了近 4 个月。两组的 6 个月无进展生存率分别为 60.9% 和 29.1%,同样差距明显。
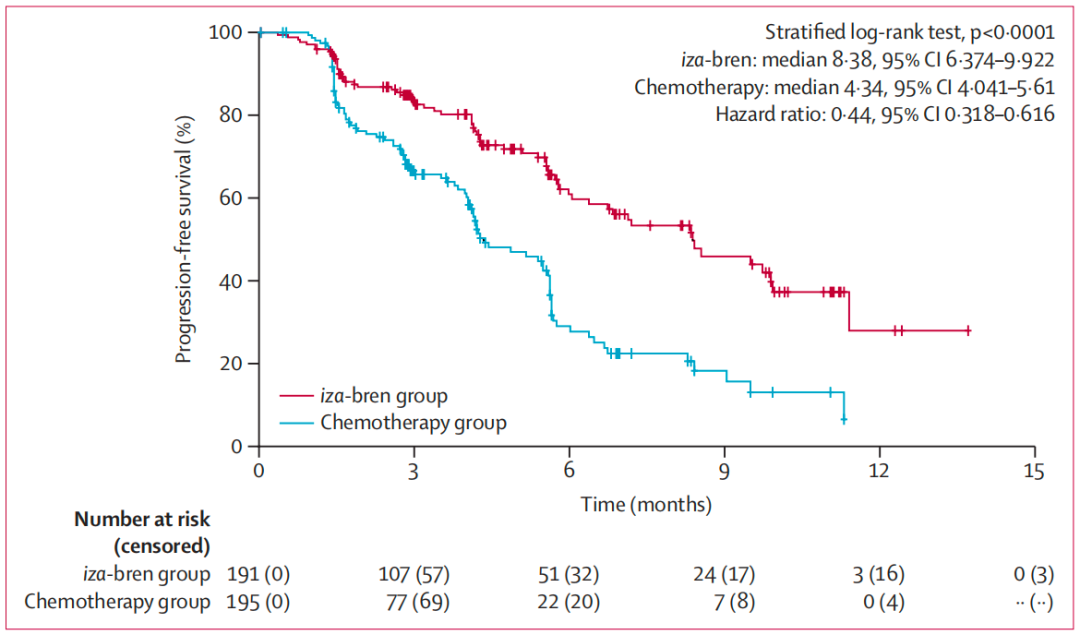
安全性分析:副作用可控,以血液学毒性为主
在安全性方面,Iza-bren 治疗组 80% 的患者出现了 3 级及以上治疗相关不良事件,化疗组为 62%。主要副作用为血液学毒性,包括贫血(50%)、白细胞减少(43%)、血小板减少(43%)和中性粒细胞减少(38%)。
非血液学毒性不良事件大多为 1-2 级,包括乏力、恶心、食欲下降等。Iza-bren 治疗组有 43% 患者出现严重治疗相关不良事件,化疗组为 27%。Iza-bren 治疗组有 4 例(2%)治疗相关死亡,主要与发热性中性粒细胞减少症和血小板减少相关。
虽然血液学毒性发生率较高,但多数不良事件可以通过标准支持治疗控制,中位中性粒细胞恢复时间仅为 4 天,血小板恢复时间为 5 天,整体安全性可控。
临床意义:改变实践,树立新标准
这是全球首项在经多线治疗失败的晚期鼻咽癌患者中开展的随机 3 期临床研究,也是首个证明双特异性 ADC 临床获益的 3 期临床研究。
目前,美国 NCCN 指南对鼻咽癌后线治疗的推荐仅基于小样本 2 期临床研究,缺乏高级别证据。Iza-bren 的出现有望改变这一现状,为晚期鼻咽癌患者提供新的治疗选择,Iza-bren 有望成为经治晚期鼻咽癌的新标准治疗。
相关阅读:
2025 年 7 月 10 日,北京大学肿瘤医院鲁智豪、沈琳、龚继芳等人在国际顶尖医学期刊 Nature Medicine 上发表了题为:A bispecific antibody–drug conjugate targeting EGFR and HER3 in metastatic esophageal squamous cell carcinoma: a phase 1b trial的临床研究论文。

该研究报道了靶向 EGFR 和 HER3 的双特异性抗体偶联药物伦康依隆妥单抗(izalontamab brengitecan,iza-bren)在转移性食管鳞状细胞癌的 1b 期临床试验结果,在转移性食管鳞状细胞癌患者中显示出良好的疗效和可控的安全性。
所有患者的确认客观缓解率(cORR)为 29.3%(24/82),可评估患者中的 cORR 为 32.9%(24/73)。对于剂量为 2.5 mg/kg 的患者,cORR 为 39.6%(21/53),疾病控制率为 79.2%(42/53)。对于剂量为 2.0 mg/kg 的患者,cORR 为 15.0%(3/20),疾病控制率为 50.0%(10/20)。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


