化学分子修饰的益生菌实现肿瘤的光动力-免疫协同治疗
来源:中山大学 2023-10-03 19:14
光动力疗法(Photodynamic Therapy,PDT)是一种非侵入性治疗方式,在个性化医疗中获得了极大的普及。在特定波长光的激发下,光动力疗法的核心——光敏剂将细胞组织
光动力疗法(Photodynamic Therapy,PDT)是一种非侵入性治疗方式,在个性化医疗中获得了极大的普及。在特定波长光的激发下,光动力疗法的核心——光敏剂将细胞组织中的分子氧转化为高细胞毒性的活性氧物种(ROS),从而诱导肿瘤细胞死亡。凭借光稳定性强等优异的光物理性能,过渡金属配合物(钌、铱和铼等)作为光敏剂受到越来越多的关注,其中金属光敏剂的肿瘤靶向递送策略也变得愈发重要。此外,越来越多的研究表明,由于固有的乏氧趋向性,静脉注射的细菌通过血液循环系统能够靶向、穿透肿瘤组织并在肿瘤部位定殖,因此细菌被认为是靶向肿瘤的候选载体。
近日,中山大学化学学院的夏炜教授、毛宗万教授和温州医科大学的沈建良教授合作,开发了一种新型铱(III)光敏剂-细菌杂交体(Ir-HEcN),其能够靶向肿瘤部位,在光照下实现肿瘤的光动力免疫治疗。课题组首先对益生菌E. Coli Nissle 1917 进行基因工程改造,使其表面过表达HaloTag蛋白,并合成了带有氯代正己烷结构的环金属铱(Ⅲ)配合物IrCl。基于HaloTag蛋白与氯代正己烷结构之间形成的共价键,IrCl可以稳定地锚定在Nissle 1917 表面。(图1)
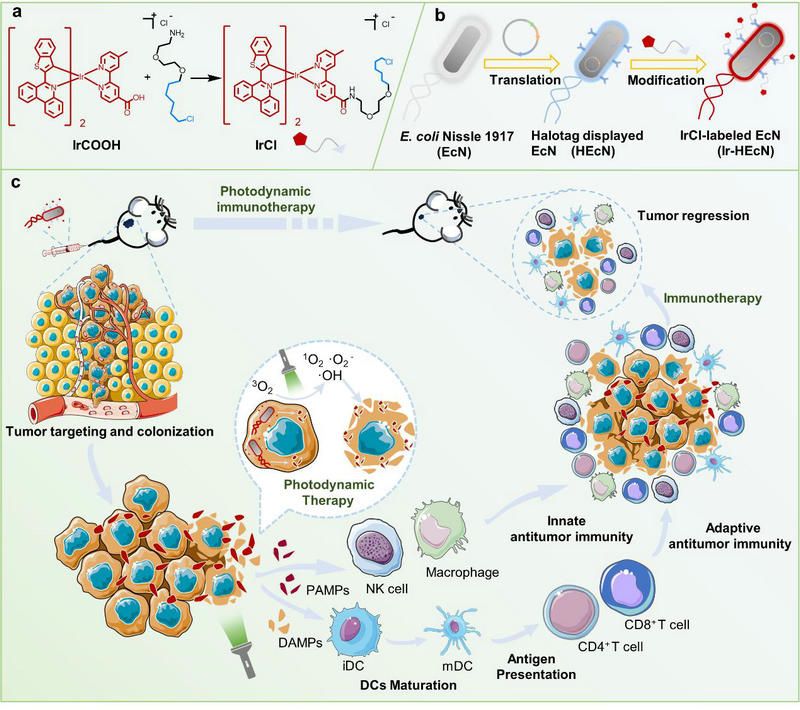
图1 :(a)光敏剂IrCl的合成(b)铱(Ⅲ)光敏剂杂合体的构建(c)通过光动力免疫治疗消除实体瘤的示意图
相比于铱配合物,杂合体具有更优异的肿瘤渗透性。此外,凭借Nissle 1917的肿瘤部位定殖特性,与铱配合物不同的是,杂合体具有更高的肿瘤靶向性。因此,在525 nm绿光的激发下,杂合体能够显著抑制乳腺肿瘤的生长。最后,肿瘤部位的免疫细胞的流式分析结果表明:无论是先天性免疫的巨噬细胞和自然杀伤细胞,还是适应性免疫的树突状细胞、CD4+ T细胞和CD8+ T细胞, 杂合体+光照组都表现出最高的浸润率。(图2)
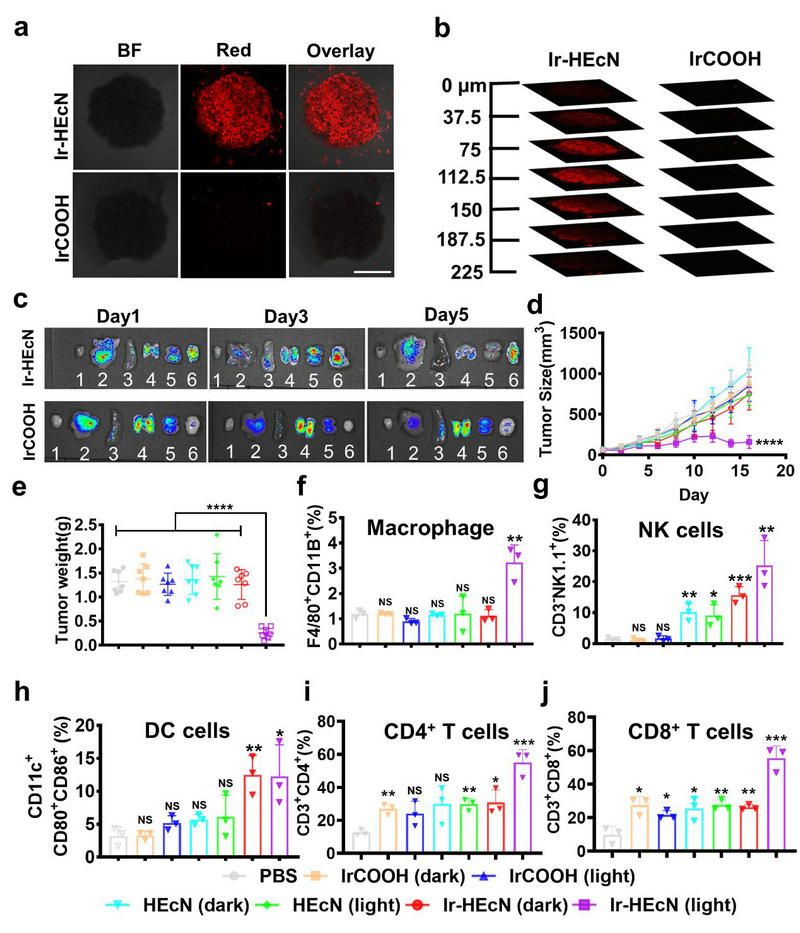
图2. (a)(b)MDA-MB-231细胞球磷光成像 (c)荷瘤小鼠各器官及肿瘤离体成像(d)荷瘤小鼠肿瘤生长曲线(e)荷瘤小鼠肿瘤体积(f)(g)(h)(i)(j)肿瘤部位免疫细胞浸润率
此项工作设计并构建了第一例铱光敏剂修饰的细菌杂合体。在525 nm绿光的激发下,该杂合体会导致肿瘤细胞发生焦亡并促进先天性免疫细胞(巨噬细胞、自然杀伤细胞)和适应性免疫细胞(树突状细胞、CD4+ T细胞和CD8+ T细胞)的浸润,最终实现肿瘤的光动力免疫治疗。此外,该肿瘤靶向策略也可能适用于其他抗肿瘤金属药物。
该研究成果发表在Angewandte Chemie International Edition上,并被评选为热点文章。中山大学化学学院博士研究生林文凯和温州医科大学硕士生刘宇(现为中山大学化学学院博士研究生)为该论文的共同第一作者,温州医科大学的沈建良教授、中山大学化学学院的毛宗万教授和夏炜教授为该论文的通讯作者。本论文受到了国家重点研发计划、国家自然科学基金和浙江省自然科学杰出青年基金等项目的支持。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


