我国学者在Cell发表世界首个现货通用CAR-T成功治疗自身免疫病的临床结果
来源:生物世界 2024-10-08 09:00
该研究中使用的新一代通用型CAR-T产品具有以下临床优势:极大的患者可及性、更高的临床安全性、更优的临床治疗效果,克服了患者自体CAR-T细胞的高度个性化、制备周期长等诸多痛点。
2024年10月4日,Nature 官网头条发布了一篇题为:World-first therapy using donor cells sends autoimmune diseases into remission 的报道,介绍了一项来自中国团队、发表于 Cell 期刊的研究成果。

在这篇 Cell 论文中,来自邦耀生物、海军军医大学附属长征医院、华东师范大学、浙江大学医学院第二附属医院的研究人员合作,利用CRISPR-Cas9基因编辑技术对健康供体来源的、靶向CD19的CAR-T细胞进行基因工程改造,开发出了新一代异体通用型CAR-T疗法,帮助3名患有严重自身免疫病的患者(1名女性、2名男性)达到长期缓解。
值得一提的是,这3名来自中国的患者是世界首批(World-first)使用供体细胞(而不是患者自身细胞)来源的CAR-T细胞疗法治疗的自身免疫病患者,也是国际顶尖学术期刊 Cell 首次发表CAR-T细胞治疗自身免疫疾病的研究。这项突破进展也是大规模生产CAR-T细胞疗法治疗自身免疫病迈出的关键第一步。

该研究利用CRISPR-Cas9基因编辑技术对健康供体来源的、靶向CD19的CAR-T细胞进行基因工程改造,以解决免疫排斥问题,从而开发出了新一代异体通用型CAR-T疗法(TyU19),并成功治疗了1例难治性免疫介导的坏死性肌病患者,以及2例弥漫性皮肤系统性硬化症患者。在治疗后6个月的随访期间,所有3名患者的症状均得到深度缓解,疾病临床反应指数评分显著改善,炎症和器官纤维化也得到逆转,且无细胞因子释放综合征或其他严重不良事件。
这些临床结果表明,现货通用型CAR-T细胞在治疗严重难治性自身免疫疾病方面具有高度安全性和有效性。
来自上海的57岁的龚先生是其中一名接受治疗的患者,他患有系统性硬化症(SSc),这种疾病会影响结缔组织,导致皮肤硬化和广泛的器官损伤。接受治疗三天后,他感觉到了皮肤松弛,可以开始活动手指,并再次张开嘴巴。治疗两周后,他就能回到办公室工作。而现在,接受治疗一年多后,他表示“感觉很好”。
嵌合抗原受体T细胞疗法(CAR-T细胞疗法)的出现,是近年来癌症免疫治疗领域的一大突破,自2017年以来,美国FDA已经批准了6款CAR-T细胞疗法上市,用于治疗白血病、淋巴瘤等血液类癌症。
近年来,CAR-T细胞疗法在系统性红斑狼疮、多发性硬化症等自身免疫病方面也展现了巨大前景,这些疾病是由于不正常的免疫细胞产生并释放了攻击自身组织的自身抗体。但目前已上市的CAR-T细胞疗法均使用来自患者自身的免疫细胞进行基因工程改造,这使得该疗法及其昂贵且耗时耗力。
因此,研究人员开始尝试利用健康捐赠者的免疫细胞来创建现货型CAR-T细胞产品,理论上,一个捐赠者的细胞能够为上百人提供治疗,这奖极大地扩大生产规模、降低生产成本和时间,从而大幅提高CAR-T细胞疗法的可及性,造福更多患者。该方法已被用于癌症患者的临床试验,但迄今为止效果仍然有限。
而这项发表于 Cell 的研究,首次报道了来自供体细胞的现货型CAR-T细胞疗法(该疗法由邦耀生物开发)治疗自身免疫病的结果,接受治疗超过6个月时间,3名患者仍处于持续疾病患者状态。该临床试验的领导者、海军军医大学附属长征医院徐沪济教授表示,还有24名自身免疫病患者接受了该细胞疗法,总体上治疗结果是积极的。
CAR-T细胞疗法通常需要从接受治疗的患者身上提取其自体T细胞,然后通过基因工程技术让这些细胞表达被靶向B细胞的CAR蛋白,再将这些改造而来的CAR-T细胞重新输入患者体内。
基于健康供体捐赠的T细胞的CAR-T细胞与患者自体CAR-T细胞整体上是相似的,研究团队从一名21岁的女性捐赠者的外周血单个核细胞(PBMC)中分离出T细胞,首先用编码抗CD19-CAR的慢病毒转导,构建出靶向CD19的CAR-T细胞,然后使用CRISPR-Cas9基因编辑工具敲除CAR-T细胞中的5个基因(HLA-A、HLA-B、CIITA、TRAC和PD-1),最后,进行磁激活细胞分选以纯化出CD3阴性细胞,以避免同种异体T细胞引起的移植物抗宿主反应。通常,每批次可产生>100例患者的使用量(每次输注1×106/kg CAR阳性细胞)。

2023年5月,一名42岁的免疫介导的坏死性肌病(IMNM)女性患者成为接受该疗法的首位患者,该疾病因患者产生的抗体攻击自身骨骼肌,导致虚弱和疲劳,还可能出现危及生命的全身性症状。2023年6月和8月,龚先生和另一名45岁的男性接受治疗,他们两人患有弥漫性皮肤系统性硬化症(dcSSc)。
一旦被注射到患者体内,这些基因工程改造的CAR-T细胞就开始工作,它们增殖、靶向并摧毁所有的B细胞,包括与自身免疫疾病相关的致病B细胞。这些基因工程改造的CAR-T细胞在患者体内存活数周后基本消失。最终,新的健康的B细胞回来了,而致病B细胞没有再回来。
治疗两个月后,这名免疫介导的坏死性肌病(IMNM)女性患者达到了完全缓解,并在6个月的随访中保持了完全缓解状态,且表现出明显的临床改善,其自身抗体已降至检测不到的水平,肌肉力量和活动能力也得到了显著改善。这两名弥漫性皮肤系统性硬化症(dcSSc)男性患者的症状同样得到了显著改善,包括器官纤维化损伤的逆转,以及自身抗体水平的下降。
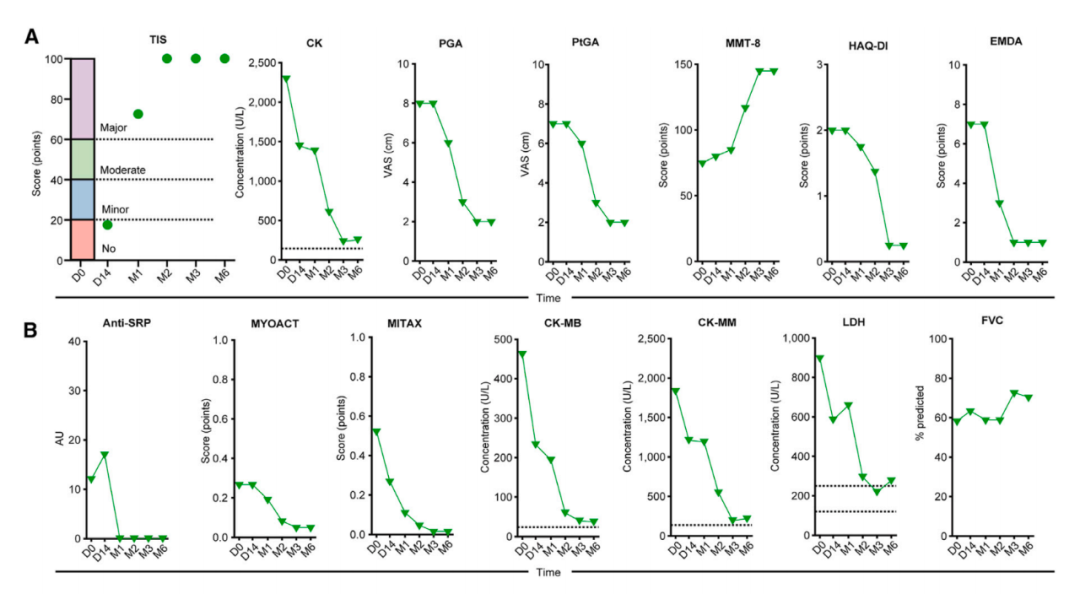
IMNM患者临床评估
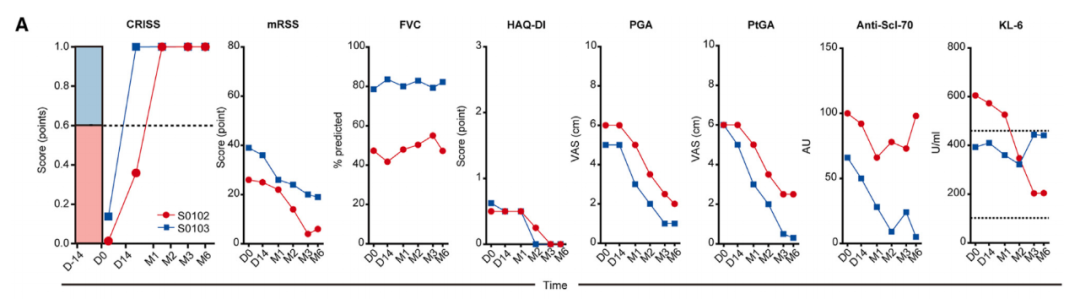
ddSSc患者临床评估
值得一提的是,3名患者的整个治疗过程耐受性良好,未观察到癌症患者在接受CAR-T细胞疗法后常见的细胞因子释放综合征(CRS)、移植物抗宿主病(GvHD)、免疫效应细胞相关神经毒性综合征(ICANS)。
这些临床研究结果展示了现货型通用异体CAR-T细胞产品在治疗难治性自身免疫病方面的巨大潜力。 该研究中使用的新一代通用型CAR-T产品具有以下临床优势:极大的患者可及性、更高的临床安全性、更优的临床治疗效果,克服了患者自体CAR-T细胞的高度个性化、制备周期长、失败风险高且成本极其高昂的诸多痛点,有望引领CAR-T细胞疗法开发的发展方向。
海军军医大学附属长征医院徐沪济教授、华东师范大学生命科学学院/邦耀生物杜冰教授、浙江大学医学院第二附属医院吴华香教授、华东师范大学生命科学学院/邦耀生物刘明耀教授为论文共同通讯作者。海军军医大学附属长征医院王晓冰副教授、吴歆副教授、华东师范大学生命科学学院/邦耀生物谭炳合副教授、浙江大学医学院第二附属医院朱亮副教授为论文共同第一作者。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


