干细胞、类器官与表观遗传学的交响曲!Nat Neurosci:科学家构建单细胞表观基因组图谱,揭示调控细胞命运的关键“开关”
来源:生物谷原创 2024-07-22 10:41
本研究中构建的人类神经类器官发育的单细胞表观基因组图谱,为深入了解人类细胞命运选择提供了宝贵的参考蓝本。

人体内的每个细胞会随着时间推移逐渐发育,最终变得具有特定的功能,这一过程称之为细胞分化或特化(cell specialization),这一过程的核心在于形成多样化的细胞群体,各自承担着不同的生物使命。此前研究结果表明,细胞的命运受到了表观遗传学机制(即基因和环境因素之间的相互作用)的调节,但其中确切细节仍模糊不清。
近日,一篇发表在国际杂志Nature Neuroscience上题为“Single-cell epigenomic reconstruction of developmental trajectories from pluripotency in human neural organoid systems”的研究报告中,来自苏黎世联邦理工学院的科研团队,通过研究人类大脑和源自多能干细胞的视网膜类器官,深入探索了塑造单一细胞发育路径的独特表观遗传学过程,为理解人类细胞命运的决定机制提供了新视角。
研究领导者Fides Zenk博士表示,本研究的初衷在于深化我们对人类大脑和视网膜发育过程中,调控细胞命运选择的表观遗传学机制的认识。研究的首要目标是构建一个详尽的单细胞表观遗传学地图,捕捉从多能干细胞到成熟神经元的蜕变之旅。为了达到这一目标,研究团队致力于绘制一张“蓝图”,揭示组蛋白修饰如何在细胞发育过程中扮演激活与抑制的双重角色,进而调控细胞分化。
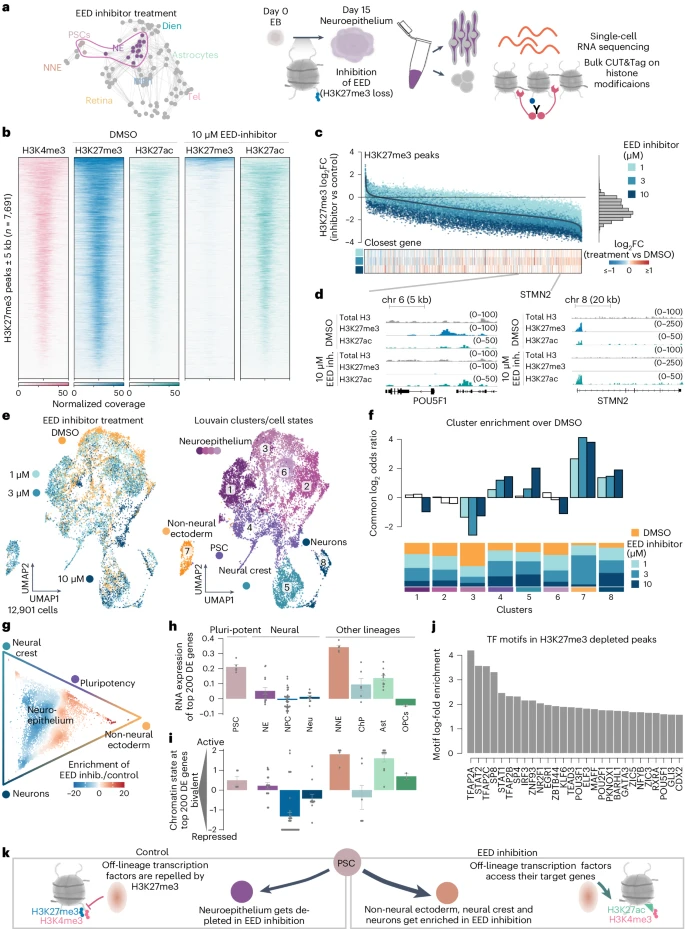
科学家识别出能调节机体单一细胞发育轨迹的表观遗传学开关
图片来源:Nature Neuroscience (2024). DOI:10.1038/s41593-024-01652-0
为了探索人类细胞多样性背后的表观遗传学奥秘,研究团队采用人类大脑和视网膜类器官进行实验。类器官是在实验室环境下,由多能干细胞培育而成的三维微型器官模型。
研究中,Zenk博士和他的同事们专注于三种关键的组蛋白修饰——H3K27ac(激活)、H3K27me3(抑制)和H3K4me3(激活)。借助CUT&Tag技术和单细胞RNA测序(scRNA-seq),研究者能够描绘出这些修饰特征从多能状态到神经分化状态的各个发育阶段的变化情况。
通过表观遗传学技术,研究者跟踪了三种核心组蛋白修饰随细胞发育进程的动态变化,他们成功识别了调控细胞命运选择的表观遗传学“开关”,并构建了人类大脑和视网膜发育的单细胞表观基因组图谱。研究人员发现,抑制与激活的组蛋白修饰转换似乎先于细胞命运的最终决定。此外,研究还显示,若在神经外胚层阶段去除H3K27me3,可能会干扰细胞的命运限定,导致异常的细胞身份。该研究成果不仅增进了科学家们对人类细胞发育及表观遗传学调控机制的理解,未来还有望揭示多种人类神经发育障碍的表观遗传学根源,为疾病模型构建和再生医学新技术的研发提供重要线索。
展望未来,Zenk博士计划进一步探究组蛋白修饰间的交互作用,以阐明其在细胞命运决定中的作用机制,并将单细胞表观基因组图谱的应用范围拓展至其他类器官模型和发育体系。研究团队还致力于探索特定表观遗传学修饰如何促成疾病状态,以及如何通过调节这些标记恢复正常的细胞功能,寻找潜在的治疗干预策略。总之,本研究中构建的人类神经类器官发育的单细胞表观基因组图谱,为深入了解人类细胞命运选择提供了宝贵的参考蓝本。(生物谷Bioon.com)
参考文献:
Zenk, F., Fleck, J.S., Jansen, S.M.J. et al. Single-cell epigenomic reconstruction of developmental trajectories from pluripotency in human neural organoid systems. Nat Neurosci 27, 1376–1386 (2024). doi:10.1038/s41593-024-01652-0
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


