Nature:中丹科学家联手揭示人类去甲肾上腺素转运体的转运和抑制机制
来源:生物谷原创 2024-08-09 10:39
这项新的研究深入揭示了 NET 的转运机制,为开发针对 MAT家族的新型肽基药物奠定了重要的结构基础。它还为开发靶向MAT的药物提供了重要启示,为新药开发提供了有力的理论支持。
去甲肾上腺素(noradrenaline, NA)是神经系统中一种重要的单胺类神经递质。位于突触前膜上的去甲肾上腺素转运体(noradrenaline transporter, NET)可将去甲肾上腺素转运到突触前神经元中。
在临床应用中,多种小分子药物通过抑制NET来增加突触间隙(synaptic cleft)中的去甲肾上腺素浓度,从而增强去甲肾上腺素能神经元的信号传导,以治疗抑郁症和注意力缺陷多动障碍(ADHD)等疾病。然而,人们对NET的底物和与不同药物分子的结合模式仍不完全了解。
在一项新的研究中,中国科学院生物物理研究所的赵岩(Zhao Yan)教授课题组与丹麦哥本哈根大学的合作者一起,利用单颗粒低温电镜技术解析了人类NET及它的多种复合物的高分辨率结构。他们揭示了NET在多种功能状态下的结构特征以及与不同药物分子的结合模式。相关研究结果于2024年7月31日在线发表在Nature期刊上,论文标题为“Transport and inhibition mechanisms of the human noradrenaline transporter”。

他们阐明了处于向内开放状态(inward-open state)的NETapo和NETNA的结构,两者的分辨率均为2.6 Å。NETNA结构揭示了NET如何在其中心结合位点识别底物去甲肾上腺素(NA)。他们还绘制了NET在不同转运状态下的离子结合位点,从而为理解离子结合、底物识别和构象变化之间的偶联机制提供了结构基础。
χ-MrlA是目前已知的唯一一种NET非竞争性抑制剂。通过对 NET和χ-MrlA 形成的复合物的结构分析以及突变体的功能实验,研究者揭示了χ-MrlA 选择性抑制 NET 而不影响血清素转运体(SERT)和多巴胺转运体(DAT)等其他家族成员的重要结构基础。
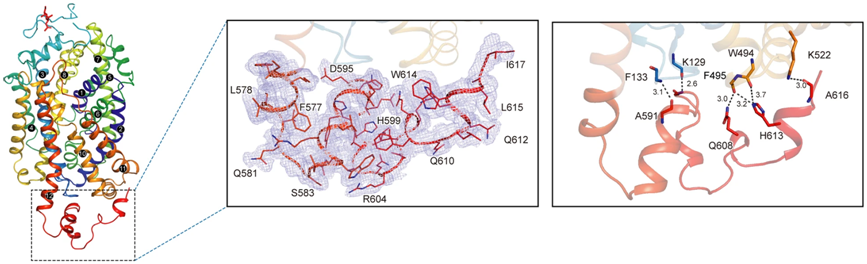
图片来自Nature, 2024, doi:10.1038/s41586-024-07638-z
为了揭示安非他酮(Bupropion)和齐拉西酮(Ziprasidone)这两种常用于临床治疗的抗抑郁药和抗精神病药选择性抑制三种单胺转运体(MAT)——NET、DAT和SERT的分子机制,研究者分析了NET与安非他酮和齐拉西酮所形成的复合物的结构。他们发现安非他酮和齐拉西酮都结合在NET面向细胞内一侧的结合口袋中。
这项新的研究深入揭示了 NET 的转运机制,为开发针对 MAT家族的新型肽基药物奠定了重要的结构基础。它还为开发靶向MAT的药物提供了重要启示,为新药开发提供了有力的理论支持。(生物谷Bioon.com)
参考资料:
Tuo Hu et al. Transport and inhibition mechanisms of the human noradrenaline transporter. Nature, 2024, doi:10.1038/s41586-024-07638-z.
Scientists reveal transport mechanism of norepinephrine transporter and binding mode of small molecule and peptide drugs
https://phys.org/news/2024-08-scientists-reveal-mechanism-norepinephrine-mode.html
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


