Nature子刊:王小龙团队等利用AlphaFold3改造Fanzor系统,实现高效基因编辑
来源:生物世界 2025-05-26 11:24
该研究对真核生物来源的Fanzor系统进行改造,开发出了靶向范围更广、效率更高的微型基因编辑工具,在小鼠体内实现了高效基因编辑,凸显了 Fanzor 系统作为生物学研究和治疗应用的多功能工具箱的潜力。
西北农林科技大学王小龙团队与上海科技大学吴兆韡团队合作,在 Nature 子刊 Nature Chemical Biology 上发表了题为:Engineering eukaryotic transposon-encoded Fanzor2 system for genome editing in mammals 的研究论文。
该研究以张锋团队报道的 Fanzor2 家族中的 NlovFz2 蛋白为对象,通过综合 AI 辅助结构预测引导的 RNA 结构优化、蛋白质工程改造、基因编辑效率评估和全基因组脱靶分析等技术手段,开发了增强型 NlovFz2-ωRNA 系统(enNlovFz2),其基因编辑效率较野生型提升了 11 倍。同时,该系统被成功用于小鼠白化疾病模型的构建及人源化杜氏肌营养不良症(DMD)小鼠模型的基因治疗,展示了真核生物来源的新型微型基因编辑工具在疾病建模和治疗领域的应用潜力。

真核转座子编码的 Fanzor 蛋白因其体积小巧且机制与 TnpB 相似,在基因组工程应用方面展现出巨大潜力。然而,未经改造的 Fanzor 系统在哺乳动物细胞中表现出极低的活性。
研究团队利用 AlphaFold3 预测了 Fanzor2 复合体结构,发现 Fanzor2 家族的 NlovFz2-ωRNA 系统与 Fanzor1 家族的 SpuFz1-ωRNA 系统结构差异较大,而是与 TnpB 系统结构更为相似。
接下来,研究团队对 NlovFz2 蛋白及其 ωRNA 序列进行了改造,构建了增强型 NlovFz2-ωRNA 系统——enNlovFz2,其具有扩展的靶标邻近基序(TAM)识别范围,可识别范围更广的 5'-NMYG(N代表A/C/G/T,M代表C/A,Y代表C/T)序列,相比野生型 NlovFz2 蛋白的 5'-CCG,enNlovFz2 极大地拓宽了在基因组中的靶向范围及应用场景。
更重要的,enNlovFz2 在人类基因组的 26 个靶位点进行了有效编辑,编辑效率大幅提高,插入/删除效率高达 81.2%,与野生型 NlovFz2 相比,enNlovFz2 的基因组编辑效率平均提升了 11.1 倍,与之前报道的两个 IS200 或 IS605 转座子编码的 TnpB 以及两个 CRISPR-Cas12f1 核酸酶编辑效率相当。
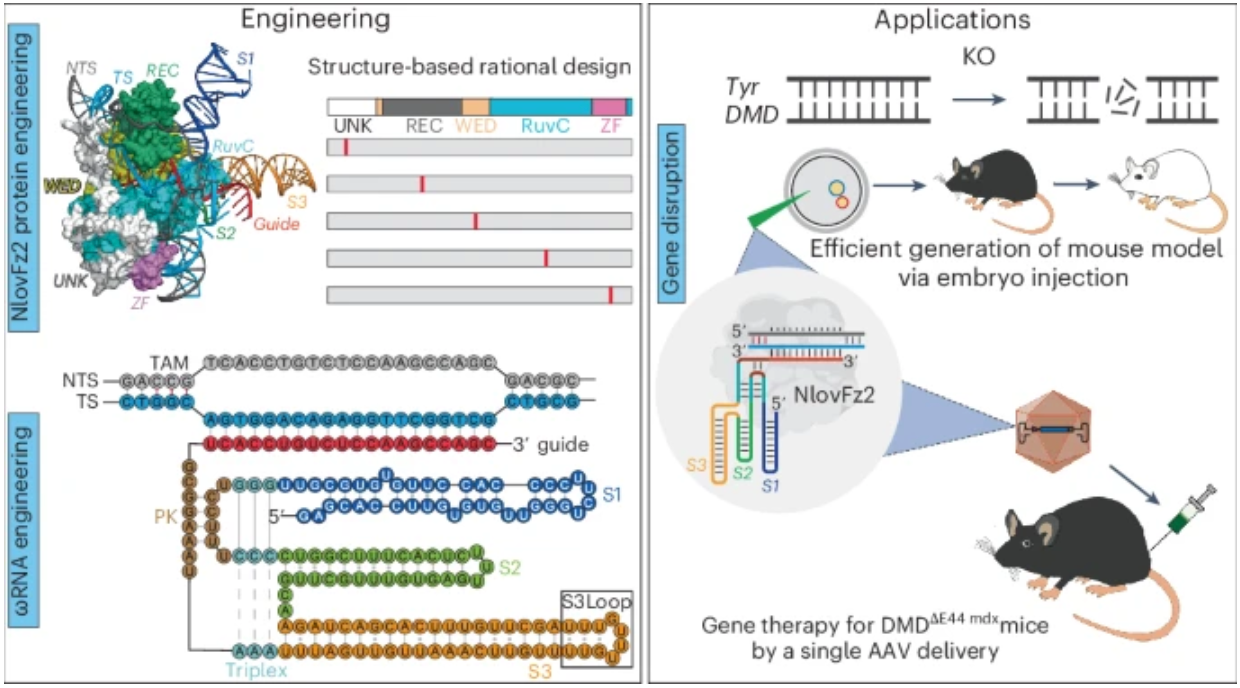
接下来,研究团队通过胚胎注射 enNlovFz2-ωRNA ,编辑小鼠的 Tyr 基因(该基因编码酪氨酸酶,是合成黑色素的关键酶,该基因功能缺失突变会导致白化病),从而成功构建了白化病小鼠模型,对 Tyr 基因的两个编辑位点的体内编辑效率分别为 38.3% 和 48.7%。
此外,在人源化杜氏肌营养不良(DMD)小鼠模型中,肌肉注射单个腺相关病毒(AAV)包装的 enNlovFz2-ωRNA,将小鼠模型肌纤维中抗肌萎缩蛋白的表达水平恢复至正常小鼠的 20%,为 DMD 患者提供了一种潜在基因编辑治疗策略。
总的来说,该研究对真核生物来源的 Fanzor 系统进行改造,开发出了靶向范围更广、效率更高的微型基因编辑工具,在小鼠体内实现了高效基因编辑,凸显了 Fanzor 系统作为生物学研究和治疗应用的多功能工具箱的潜力。
西北农林科技大学魏迎辉教授、博士研究生高鹏飞、硕士研究生陈宇斐、上海科技大学潘登博士及中国科学院上海药物研究所李国玲副研究员为论文共同第一作者。西北农林科技大学王小龙教授、魏迎辉教授、徐坤副教授和上海科技大学吴兆韡副研究员为论文共同通讯作者。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


