《细胞·代谢》:断食模拟饮食要砸癌细胞的饭碗!科学家发现FMD会抑制癌细胞糖酵解,助推最致命亚型乳腺癌患者实现长生存
来源:奇点糕 2024-12-27 15:42
研究结果显示,患者在化疗基础上接受每个周期3周、每周5天的FMD饮食,配合化疗(±二甲双胍)可达到56.6%的pCR率,已接近免疫+化疗新辅助治疗在关键临床研究中的疗效。
意大利米兰国家癌症研究所团队在Cell Metabolism期刊以论文形式正式发表了临床II期BREAKFAST研究结果,证实对早期三阴性乳腺癌(TNBC)患者,以严格限制热量摄入的断食模拟饮食(Fasting-mimicking Diet, FMDs)配合标准新辅助化疗,可取得出色的病理学完全缓解(pCR)率,并转化为患者的长期生存获益,且治疗安全可耐受。
研究结果显示,患者在化疗基础上接受每个周期3周、每周5天的FMD饮食,配合化疗(±二甲双胍)可达到56.6%的pCR率,已接近免疫+化疗新辅助治疗在关键临床研究中的疗效,患者的3年无事件生存(EFS)率则高达86.7%,明显优于历史数据;多组学分析结果显示,FMD下调肿瘤糖酵解能力和丙酮酸代谢水平,可能是实现临床获益的关键机制。
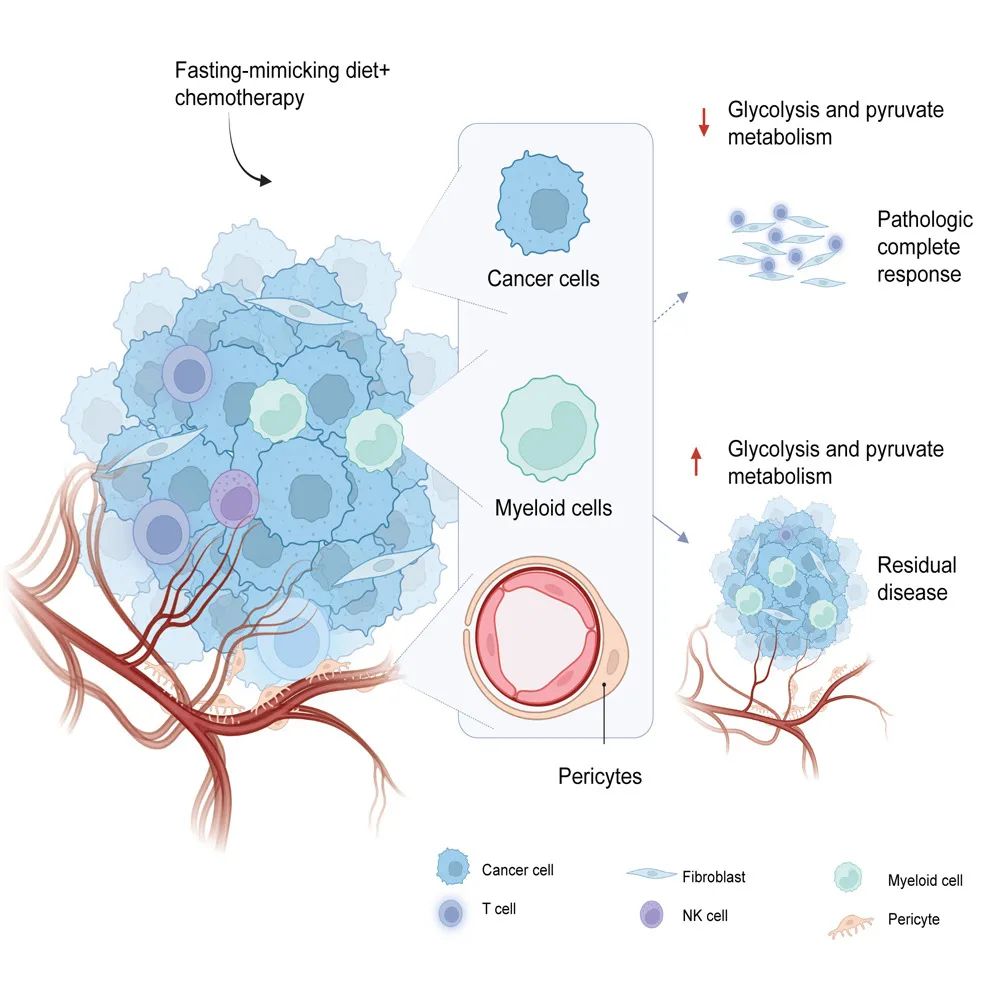
一图总结论文核心内容
从原理上来说,禁食和FMD主要会从两个方面助力抗癌治疗,一方面就是通过减少微环境营养水平,直接让癌细胞“挨饿”,而非常“爱吃糖”的TNBC就成了对FMD干预最敏感的实体瘤之一;另一方面则是调节抗肿瘤免疫应答,例如开展本次研究的意大利团队在2022年发表的临床前研究显示,证实严格限制热量摄入、低碳水低蛋白的FMD,可重塑含TNBC在内的乳腺癌瘤内免疫微环境,这对化疗起效当然也是有利的[2]。
当然,这里还要先介绍一下BREAKFAST研究采用的FMD方案:30名入组患者在每个FMD周期的每周第1天被允许摄入600大卡热量,第2-5天的热量摄入则压低至300大卡,具体食物以植物性为主,蛋白含量较低。研究至多允许患者接受8个为期3周的FMD周期,如患者因反复出现的不良事件需延迟化疗,或体重指数(BMI)未能在FMD周期开始前恢复至20kg/㎡则停止FMD,后者也是入组患者停止FMD的主要原因(7/8)。
这套热量限制FMD方案看起来很严苛,但也是2022年研究中被验证过可行性和耐受性的方案;虽然本次研究期间多达70%的患者报告了3-4级不良事件(AEs),但大多数都是化疗的锅,仅有1例患者的3-4级AEs与FMD有关,且22名患者能够完成8个周期的FMD+化疗,19名患者能够完全配合规定方案控制饮食,几乎不需要进行个体化的调整。
而在FMD的基础上,研究入组的TNBC患者还被分为两组,接受蒽环类+紫杉烷类新辅助化疗±二甲双胍(A/B组)联合治疗,患者整体的pCR率达到56.6%,已高于大多数临床III期研究中单纯新辅助化疗的水平(约15-50%),与免疫+化疗用于TNBC患者的KEYNOTE-522研究差距也不大(64.8%),pCR率在A/B组间则无明显差异。
长期预后的显著改善,更是FMD+新辅助化疗带来的惊喜:中位随访时间超过3年(39.3个月)后,30名入组患者仅有4名出现复发,36个月EFS率高达86.7%,和总生存(OS)率一起超过了既往单纯新辅助化疗的水平(3年EFS率约65%,OS率约80%)。
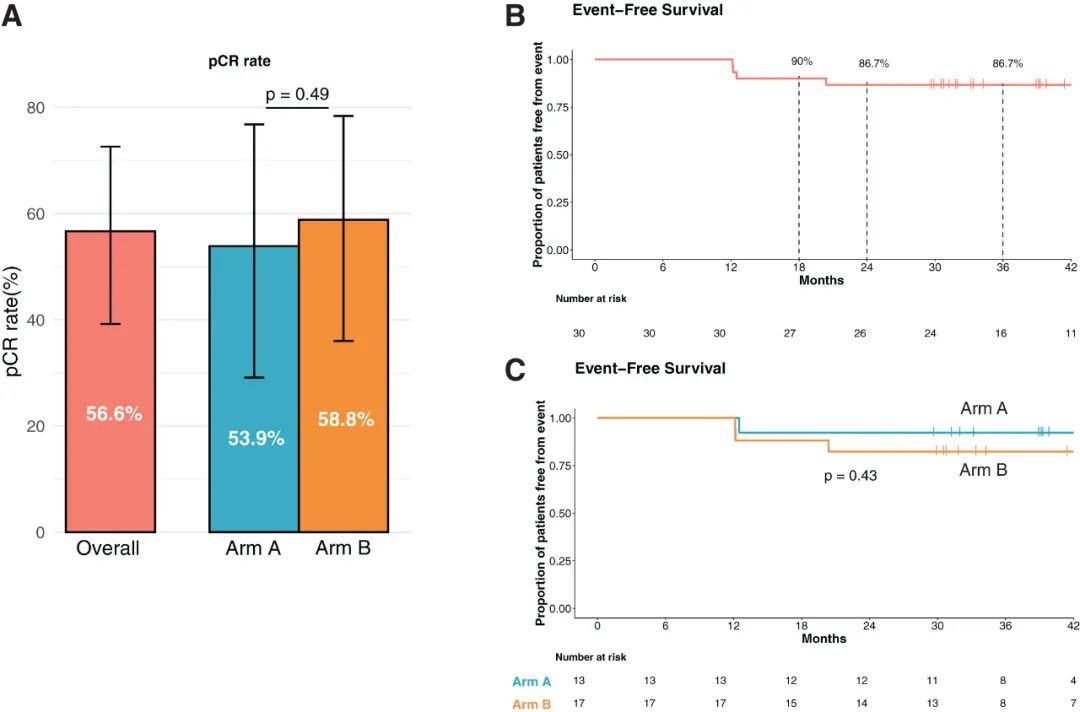
研究主要疗效数据
与多数患者能顺利完成FMD吻合,患者的BMI、体脂水平及多项代谢指标,也在治疗前后有明显的改变,其中乳酸脱氢酶(LDH)的显著下降引起了研究者们的注意,这可能提示FMD有效抑制了肿瘤的糖酵解。
最后,对手术切除肿瘤样本的单细胞RNA测序和转录组学分析显示,癌细胞及部分糖酵解水平较高瘤内细胞(如周细胞)的糖酵解能力和丙酮酸代谢水平,都在FMD+新辅助化疗开始后不久就明显下调,肿瘤微环境的免疫浸润同步发生了显著改善,糖酵解早期下调也是患者经治疗达到pCR的独立预测因子。
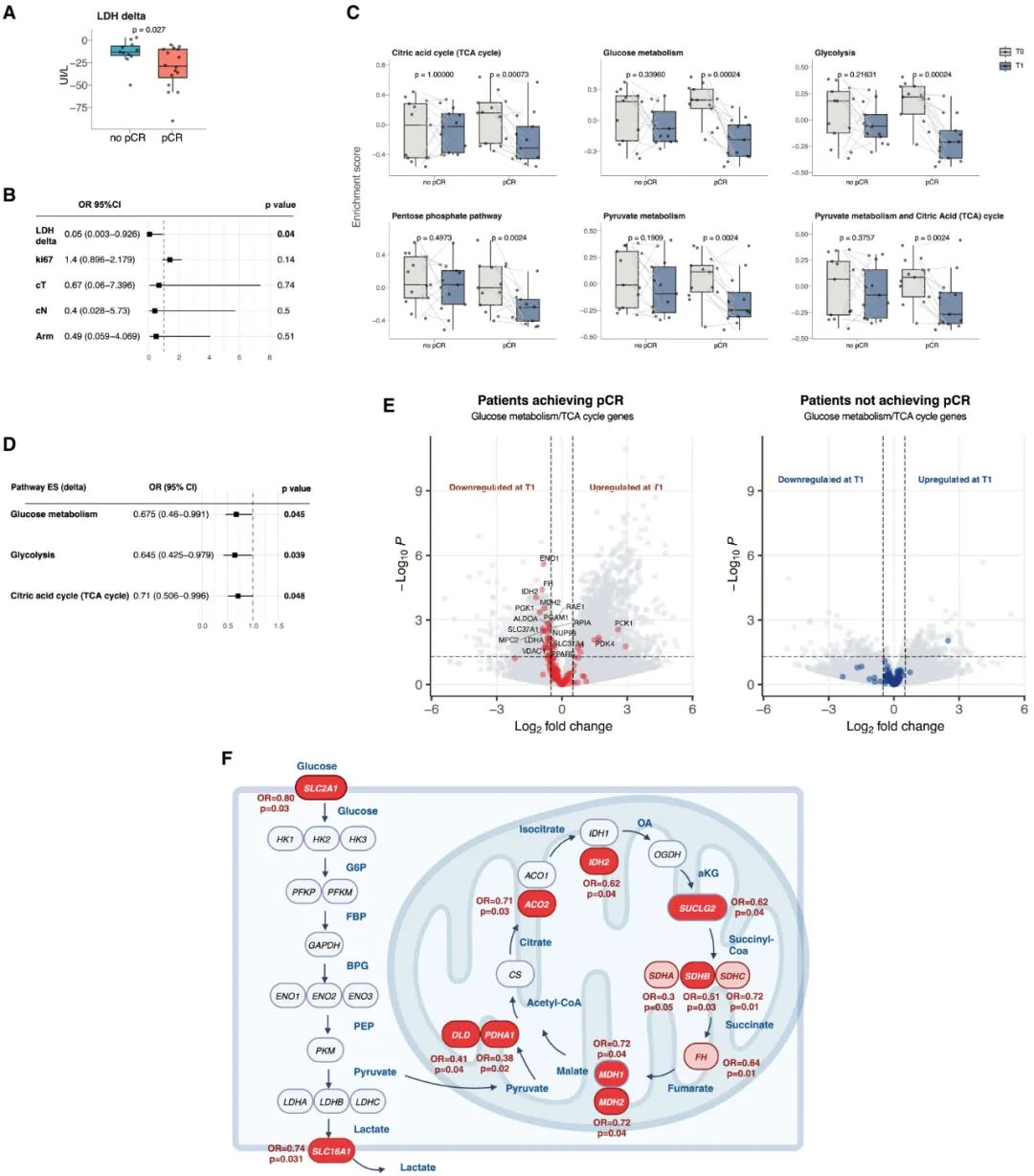
TNBC细胞的糖酵解能力和丙酮酸代谢,都被FMD明显下调
要说BREAKFAST研究有什么遗憾,大概就是“生不逢时”,因为KEYNOTE-522研究恰好是在入组期间取得了阳性结果,让免疫+化疗新辅助治疗成为了TNBC的临床治疗新标准方案,但意大利研究者们也已经启动了验证FMD配合免疫+化疗的BREAKFAST-2研究,断食+化疗+免疫三重打击如果能成功,那癌细胞就要饿着肚子落荒而逃啦。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


