DLL3 ADC峰回路转,SCLC治疗突破有望
来源:医药魔方 2024-11-06 10:57
DLL3是小细胞肺癌(SCLC)极具潜力的治疗靶点,赛道进展一直备受瞩目,只是其药物研发颇为不顺,沉寂多年。随着越来越多的DLL3产品显露治疗实力,这个赛道也将聚集更多的实力玩家。
几乎所有靶点的成药都会走过一段漫长又波折的旅程,Delta样配体3(DLL3)靶点正在经历这样的故事。
DLL3靶点成名于2016年的一笔巨额交易。当时,渴望进军实体瘤领域的艾伯维看中了Stemcentrx管线中的DLL3 ADC产品Rova-T,便出手58亿美元将其收入囊中。遗憾的是,Rova-T最终因设计缺陷未能成药。
2020年安进的CD3/DLL3双抗tarlatamab(AMG 757)传来积极消息,DLL3靶点热度持续升温。今年5月,这款药物已凭借II期研究数据获FDA加速批准上市。近年来,诺华和默沙东接连以大额交易加入DLL3药物研发战也在拉升DLL3赛道的热度。尽管如此,靶向DLL3的ADC药物开发仍然不温不火。
近日,DLL3 ADC赛道终于峰回路转,再鼎医药的ZL-1310公布小细胞肺癌(SCLC)Ia期积极结果。惊艳的客观缓解率(ORR)和安全性数据,让其成为DLL3 ADC领域多年来报道的第一个积极临床结果。同时,ZL-1310也是首个公布数据的国产DLL3 ADC。
DLL3:SCLC的“定制”靶点
肺癌一直是所有肿瘤类型中威胁人类健康的头号杀手。根据最新的统计数据,2022年全球肺癌新增病例约248万例,占全球癌症新增病例总数的12.4%[1]。大约85%的肺癌为非小细胞肺癌(NSCLC)亚型,这类患者已经拥有丰富的治疗选择,但肺癌的另一常见亚型SCLC,治疗选择仍然有限。这类癌症侵袭性极高,预后差,未经治疗的SCLC患者的中位总生存期(OS)仅为2-4个月,治疗手段的突破迫在眉睫。
目前,放化疗仍然是SCLC患者的标准治疗。放化疗虽有效,但SCLC患者很快便会耐药,导致疾病进展。随着免疫疗法的兴起,PD-(L)1药物已成为SCLC的一线治疗方案,但也仅限于广泛期SCLC(ES-SCLC,占比约2/3)。
SCLC的一/二/三线治疗
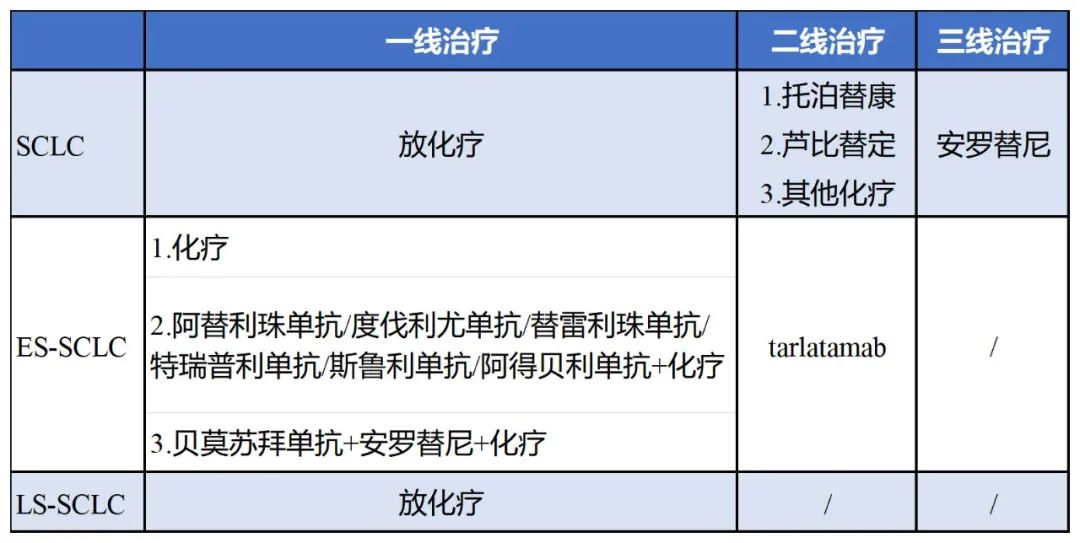
从现有数据来看,PD-(L)1单抗联合化疗的中位OS约为12-15个月[2-7],其生存获益相比标准治疗(约为10-13个月[2-7])已有较大提升。
但是,仍然有许多患者无法从PD-(L)1药物中获益,临床上也缺乏有效的后线治疗选择。所幸,这一局面已经开始好转,tarlatamab在今年获批成为针对ES-SCLC的二线治疗药物。虽然这款药物仍需经过验证性III期研究的检验,但在现阶段足以为SCLC领域的药物研发注入信心。
Tarlatamab靶向的DLL3仅在SCLC这类神经内分泌肿瘤中特异性高表达(85%-94%[8]),在正常细胞上几乎不表达,这使得DLL3看起来几乎是专门为SCLC量身定做的靶点。
DLL3与SCLC的联系源于Notch信号通路。研究表明,DLL3与Notch1受体结合后可抑制Notch信号通路的激活,影响与肿瘤抑制相关基因(如Hes基因、Hey基因[9,10])的表达,最终促进SCLC的发生发展。
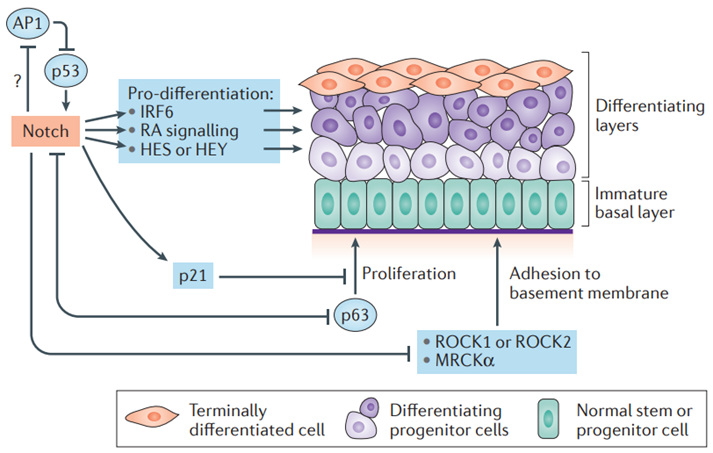
Notch信号通路介导的肿瘤抑制[10]
虽然tarlatamab只是围绕DLL3靶点进行药物研发活动的第一个收获,但是DLL3靶向药物的探索绝对不止于此。
Rova-T是最早进入临床的DLL3靶向药物,也是第一个进入III期阶段的DLL3 ADC。Rova-T由人源化DLL3单抗、可裂解linker和吡咯并苯二氮卓类衍生物(PBD)毒素组成,DAR值为2。
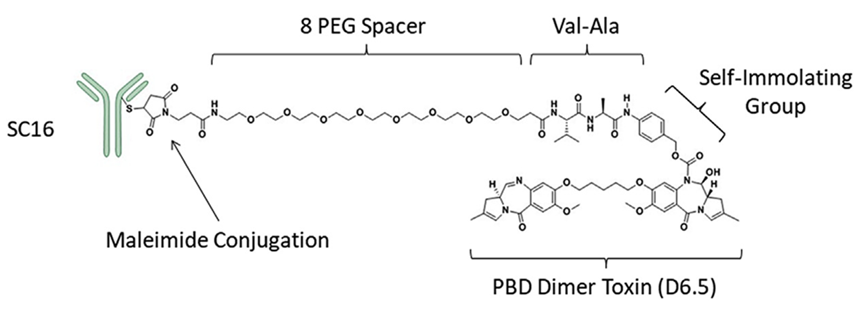
Rova-T的结构设计[11]
可惜的是,两项III期研究(MERU[12]和TAHOE[13])均以失败告终。并且,Rova-T的安全性令人担忧,一线治疗的治疗相关不良事件(TRAE)发生率高达79%。此后很长一段时间,DLL3 ADC赛道陷入了沉寂。
ORR表现突出,ZL-1310有望革新治疗
自2017年Rova-T宣告退场至今,全球仅有3款DLL3 ADC进入临床阶段,开发难度可想而知。此次露面的ZL-1310是目前全球进度最快的DLL3 ADC,其数据成色如何也备受关注。

来源:再鼎医药ENA 2024大会PPT
ZL-1310的安全性得分从设计上来看已经有所保障。经TMALIN技术平台优化的ADC分子具备极高的全身循环稳定性和更高的肿瘤富集特性,并且ZL-1310的毒素为拓扑异构酶I抑制剂,其毒性相比PBD更为可控。
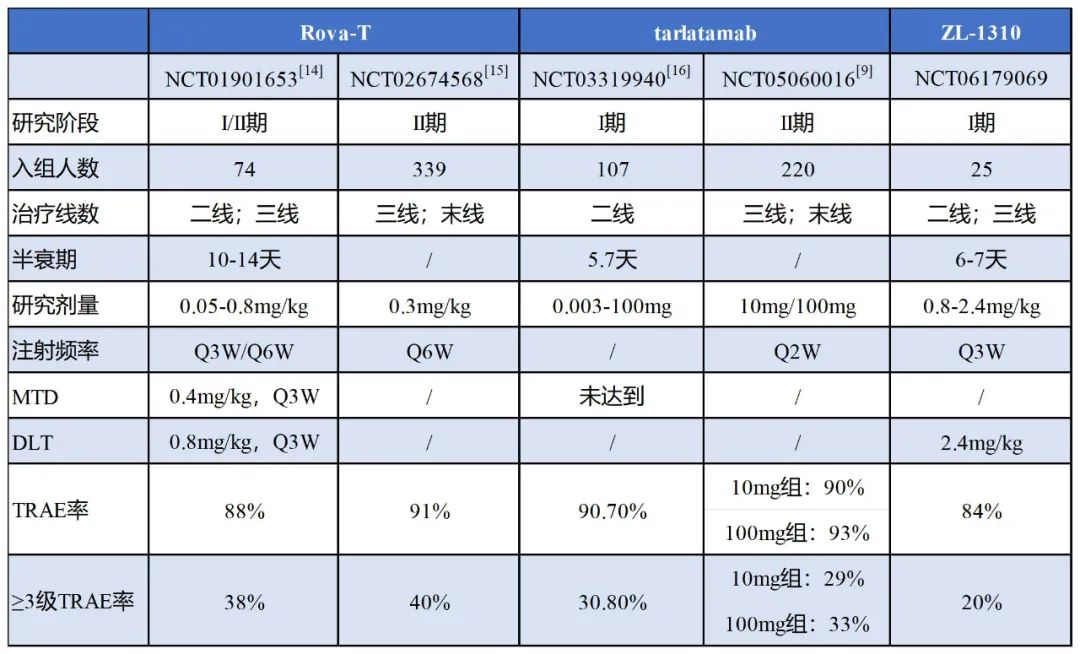
本次公布的安全性数据呼应了这一设计。ZL-1310在所有剂量水平(0.8-2.4mg/kg)下均具有良好的耐受性。25例患者接受治疗后,最常见的不良事件(AE)为中性粒细胞减少症(12%,3/25)。此外,3级及3级以上TRAE发生率为20%(5/25),严重TRAE发生率为8%(2/25),没有患者因治疗期间不良事件(TEAE)而终止治疗。
尤为值得注意的是,研究中未见报道ZL-1310导致的细胞因子释放综合征(CRS),而这是tarlatamab被诟病的地方。在II期研究中,高达55%的患者在接受tarlatamab治疗后出现了CRS,其中一半为严重CRS[9]。CRS是一种严重的全身性炎症反应,有可能危及患者生命,因此在临床治疗中需注意此类副作用的发生。
参考Rova-T和tarlatamab的安全性数据,ZL-1310在Ia期研究中表现出的安全性还是比较可靠的,可以在后续研究中继续收集安全性数据。
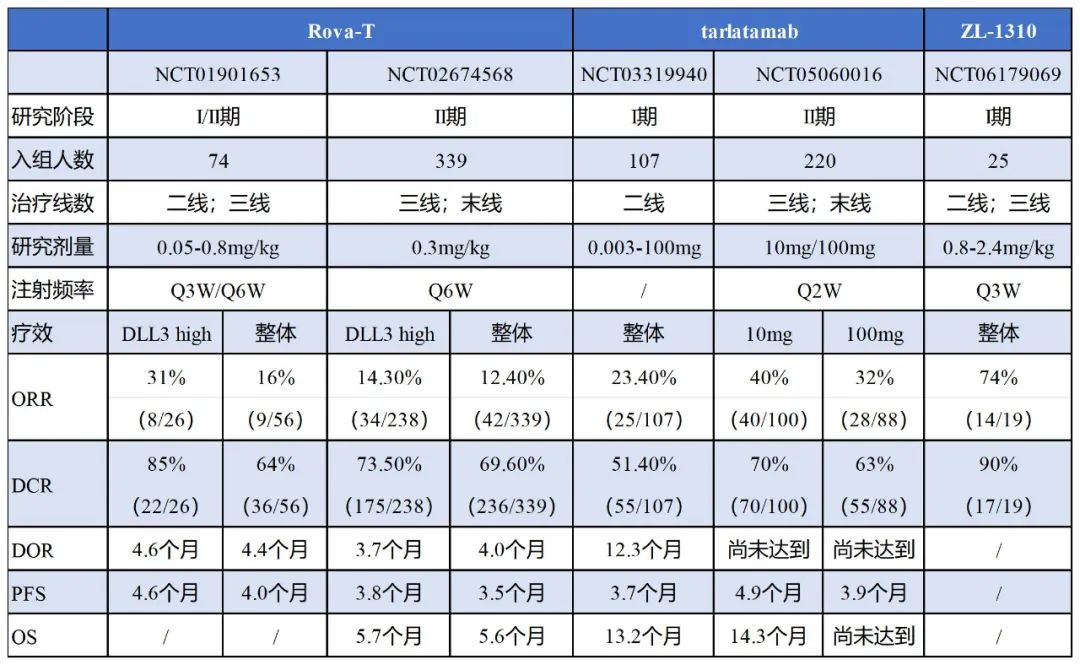
Rova-T、tarlatamab和ZL-1310早中期安全性数据概览
基于TMALIN技术平台设计的ADC分子还具有另一优势——无论是否被细胞内吞均可发挥抗肿瘤作用,并且兼顾高DAR值(8)和均一性。这一特点赋予了ZL-1310实现高效肿瘤杀伤效果的可能性空间。
从本次公布的数据来看,ZL-1310也已显露出可观的初步疗效。在19例可评估肿瘤结果的患者中,ORR达到了74%(14/19),并且ZL-1310在所有剂量水平上均表现出抗肿瘤活性。
Rova-T、tarlatamab和ZL-1310早中期疗效数据概览
值得注意的是,DLL3 H-Score评分大于5(范围:5-260)的患者均实现了缓解,换言之,DLL3过表达的患者,ORR达到了100%。
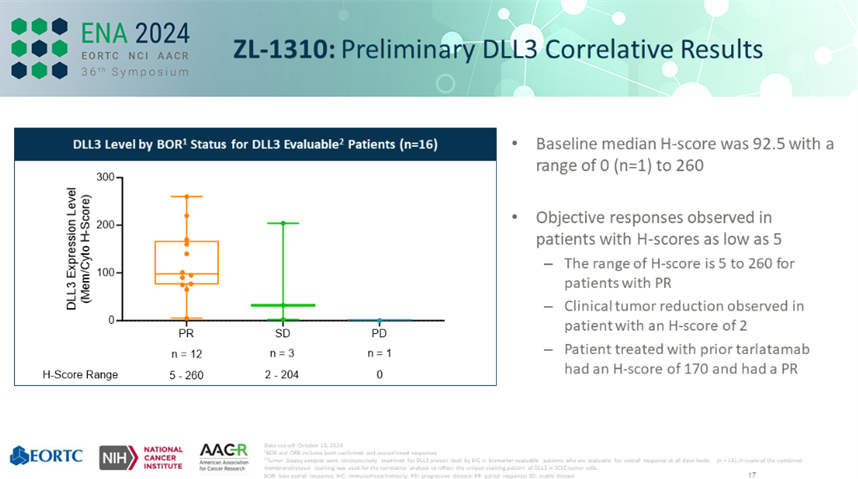
来源:再鼎医药ENA 2024大会PPT
参考Rova-T和tarlatamab的疗效数据,ZL-1310目前展现出的SCLC治疗效果非常突出。若其疗效能在后续研究中保持,ZL-1310有望为SCLC领域带来突破性的治疗革新。
此外,本项研究在美国和中国同步开展,这一点可以保障中美同步研发的进度,为ZL-1310后续在美国的监管注册减少阻碍。这也从侧面说明了再鼎医药对ZL-1310的全球开发有着清晰的规划。在昨晚的临床数据解读电话会议中,再鼎医药总裁兼全球研发负责人Rafael G. Amado博士也提到,未来将视ZL-1310的表现(比如6个月时的ORR)与FDA沟通加速批准事宜。
此前上市的tarlatamab为二线治疗,不过安进已开展多项临床进一步分别评估tarlatamab作为LS-SCLC的放化疗后巩固治疗、ES-SCLC的一线后维持治疗和二线治疗的潜力。鉴于ZL-1310在Ia期研究中有着非常不错的疗效,并且可控的安全性也提供了探索联合治疗的空间,未来ZL-1310也有希望在前线治疗中验证更广泛的适用性。再鼎医药已计划在2025年开展ZL-1310联合阿替利珠单抗和化疗一线治疗SCLC的剂量递增研究。
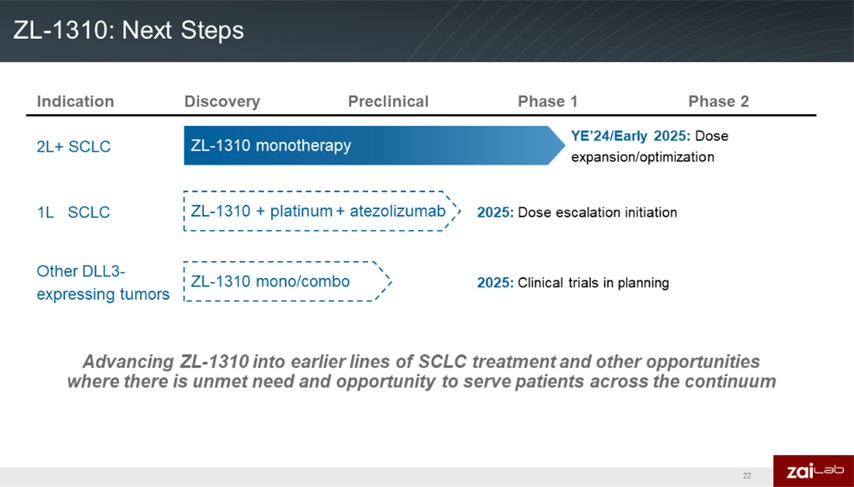
来源:再鼎医药ENA 2024大会PPT
这次的数据还有一点意外收获,1例接受tarlatamab治疗后疾病进展的患者,接受ZL-1310治疗后,在第一次肿瘤评估时实现了部分缓解(PR)。另外,基线有脑转移且可评估的6例SCLC患者均实现了PR。这些案例预示,ZL-1310有可能覆盖更多的SCLC患者,包括脑转移患者,这类患者在ES-SCLC中占比达到50%。
总结
DLL3是小细胞肺癌(SCLC)极具潜力的治疗靶点,赛道进展一直备受瞩目,只是其药物研发颇为不顺,沉寂多年。随着越来越多的DLL3产品显露治疗实力,这个赛道也将聚集更多的实力玩家,而SCLC领域也将有望诞生更多丰富的治疗选择。值得注意的是,在ES-SCLC不断取得突破的同时,局限期SCLC(LS-SCLC)也在今年迎来了激动人心的进展——度伐利尤单抗治疗LS-SCLC的III期ADRIATIC研究取得积极结果,这类患者终于有望迎来放化疗之外的治疗选择。
ZL-1310的积极数据再次验证了再鼎医药选择品种的眼光。公司运营十年以来,再鼎医药管线中已经汇聚了多款实力产品,如肿瘤电场治疗、艾加莫德、瑞普替尼等产品,涉及肿瘤、自免、感染疾病等领域。随着在研管线项目的持续推进,再鼎医药在肿瘤领域和自免疾病中的布局实力不断显露,期待再鼎医药为患者带来下一个突破性药物。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


