Cell子刊:武汉大学闫卫团队揭开癌症放疗引起肌无力的新机制
来源:生物世界 2025-06-24 09:15
该研究表明,放疗通过激活花生四烯酸代谢通路诱导肿瘤细胞分泌富含亚精胺合酶的小细胞外囊泡(sEV),被骨骼肌吸收后引起多胺代谢通路的变化,进而促进骨骼肌肌力减退。
放疗(Radiotherapy)可降低癌症复发和死亡的风险,但其伴随的包括肌肉纤维化和无力在内的多种副作用,严重影响了患者的生活质量。然而,其潜在机制尚不明确。

在这项最新研究中,研究团队发现,癌细胞通过小细胞外囊泡(sEV)分泌更多的亚精胺合酶(SRM),从而在放疗后引发骨骼肌无力。
从机制上来说,放疗应激可诱导肿瘤细胞膜上的磷脂被磷脂酶代谢生成较多游离的花生四烯酸(ArA),ArA 的积累会提高亚精胺合酶(SRM)的类泛素化修饰(ISGylation),从而促进 SRM 从原发肿瘤中被封装到肿瘤细胞产生的小细胞外囊泡(sEV)中,进而特异性诱导亚精胺在骨骼肌中合成并积累。亚精胺作为修饰底物,通过羟腐胺赖氨酸化真核翻译起始因子5A(eIF5A),进一步促进了 I 型胶原纤维的积累。而 I 型胶原纤维过度积累(纤维化)改变了骨骼肌的力学特性,干扰了肌原纤维的收缩效率,从而影响肌力传输导致肌力减退。
此外,研究团队进一步发现,SRM 蛋白的内体分选以及通过 sEV 分泌依赖类泛素化修饰(ISGylation),而放疗应激和 ArA 积累恰恰促进了 SRM 蛋白的 ISGylation 修饰,使其经细胞外囊泡分泌导致下游骨骼肌的功能障碍。
在这些发现的基础上,研究团队提出,一种临床上用于降血压的药物氯沙坦(Losartan)处理肿瘤原发灶,与放疗联合应用,能够有效抑制 SRM 的 ISGylation 修饰,通过阻断 SRM 分泌,显著改善放疗后骨骼肌的病理变化,为开发新型放射防护剂、缓解放疗引发的毒副作用提供了重要的理论依据和潜在干预靶点。
该研究的核心发现:
- 辐射通过诱导肿瘤分泌亚精胺合酶,引发肌肉无力;
- 循环的亚精胺合酶诱导骨骼肌中胶原纤维沉积;
- 放疗引起的花生四烯酸积累诱导亚精胺合酶分泌;
- 氯沙坦通过阻断亚精胺合酶的类泛素化修饰(ISGylation)来缓解肌肉无力。
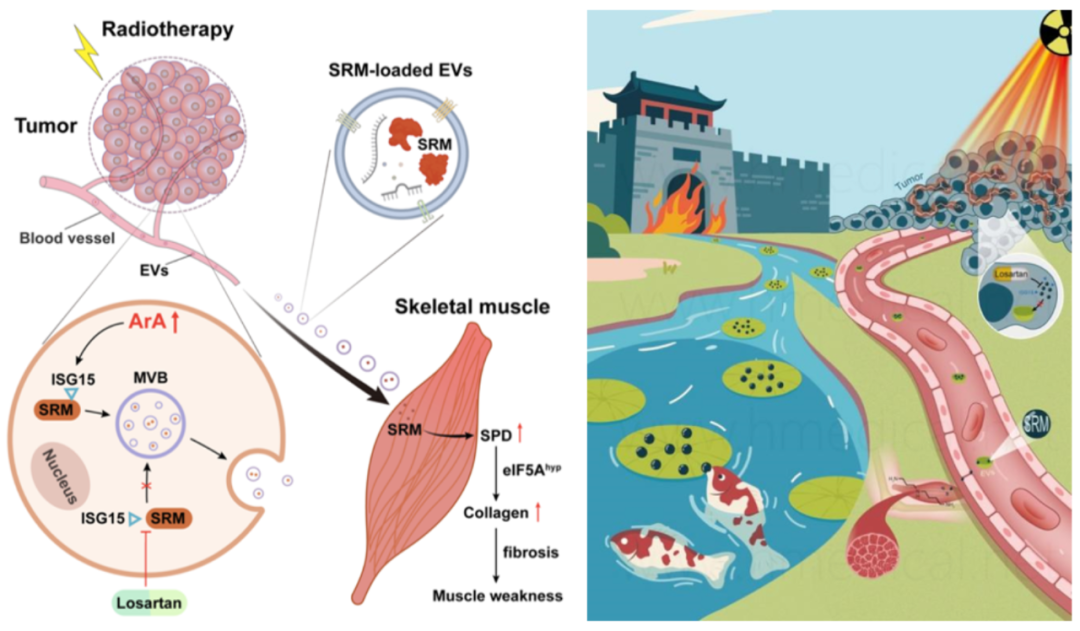
放疗刺激肿瘤分泌胞外囊泡,诱使骨骼肌无力(城门失火,殃及池鱼)
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


