慢性疼痛难题有望破解!Nature:科学家发现SLC45A4 基因有望成为慢性疼痛患者的新希望
来源:生物谷原创 2025-08-26 11:52
来自牛津大学等机构的科学家们通过研究发现了一种名为SLC45A4的基因,其能编码一种神经元多胺转运蛋白且与慢性疼痛密切相关,这一发现不仅为理解疼痛的分子机制提供了新的视角。
在当今快节奏的生活中,慢性疼痛似乎已经成了许多人难以摆脱的 “影子”,无论是长时间伏案工作后的腰酸背痛,还是因疾病引发的持续性不适,慢性疼痛不仅影响着我们的生活质量,还给社会带来了沉重的经济负担。有数据显示,全球约有五分之一的成年人受到慢性疼痛的困扰,而慢性疼痛更是全球致残的首要原因。现有的治疗手段往往因疗效有限、耐受性差等问题难以满足需求。
那么,有没有一种更有效、更安全的治疗方法呢?
近日,一篇发表在国际杂志Nature上题为 “SLC45A4 is a pain gene encoding a neuronal polyamine transporter” 的研究报告中,来自牛津大学等机构的科学家们通过研究发现了一种名为SLC45A4的基因,其能编码一种神经元多胺转运蛋白且与慢性疼痛密切相关。这一发现不仅为理解疼痛的分子机制提供了新的视角,还可能为开发新型镇痛药物开辟道路。

慢性疼痛的成因复杂,其中一个重要因素是伤害性感受器(即能感知伤害性刺激的感觉神经元)及其投射的中枢伤害性回路兴奋性增强,这种过度活跃会导致疼痛信号持续传递至大脑,进而引发慢性疼痛。然而,目前对于调节这些神经元兴奋性的分子机制仍不完全清楚。这项研究中,研究人员就旨在探索SLC45A4基因在疼痛感知中的作用,并揭示其编码的多胺转运蛋白如何影响神经元的兴奋性,为开发新的镇痛策略提供理论依据。
研究人员首先通过全基因组关联研究(GWAS)分析了来自英国生物银行(UKB)中 132,552 名欧洲血统参与者的慢性疼痛数据,发现SLC45A4基因中的某些单核苷酸变异(SNVs)与疼痛强度显著相关,其中位于该基因内含子的 rs10625280 和错义变异 rs3739238(p.Asn718Asp)关联性尤为显著。随后,这些变异在百万退伍军人计划(MVP)的欧洲血统人群(约 60 万参与者)和芬兰基因组计划(FinnGen)中均得到验证,且效应方向一致,证实了SLC45A4与疼痛感知的遗传关联。
为探究该基因的体内功能,研究人员利用 CRISPR-Cas9 基因编辑技术培育出Slc45a4基因敲除(KO)小鼠模型。这些小鼠出生时无明显缺陷,但存在早期胚胎致死的潜在可能,且在约 20 天时会出现“盐和胡椒”样的白色毛发表型(70 天时消失),这与多胺(如亚精胺)调节黑色素生成的功能一致。
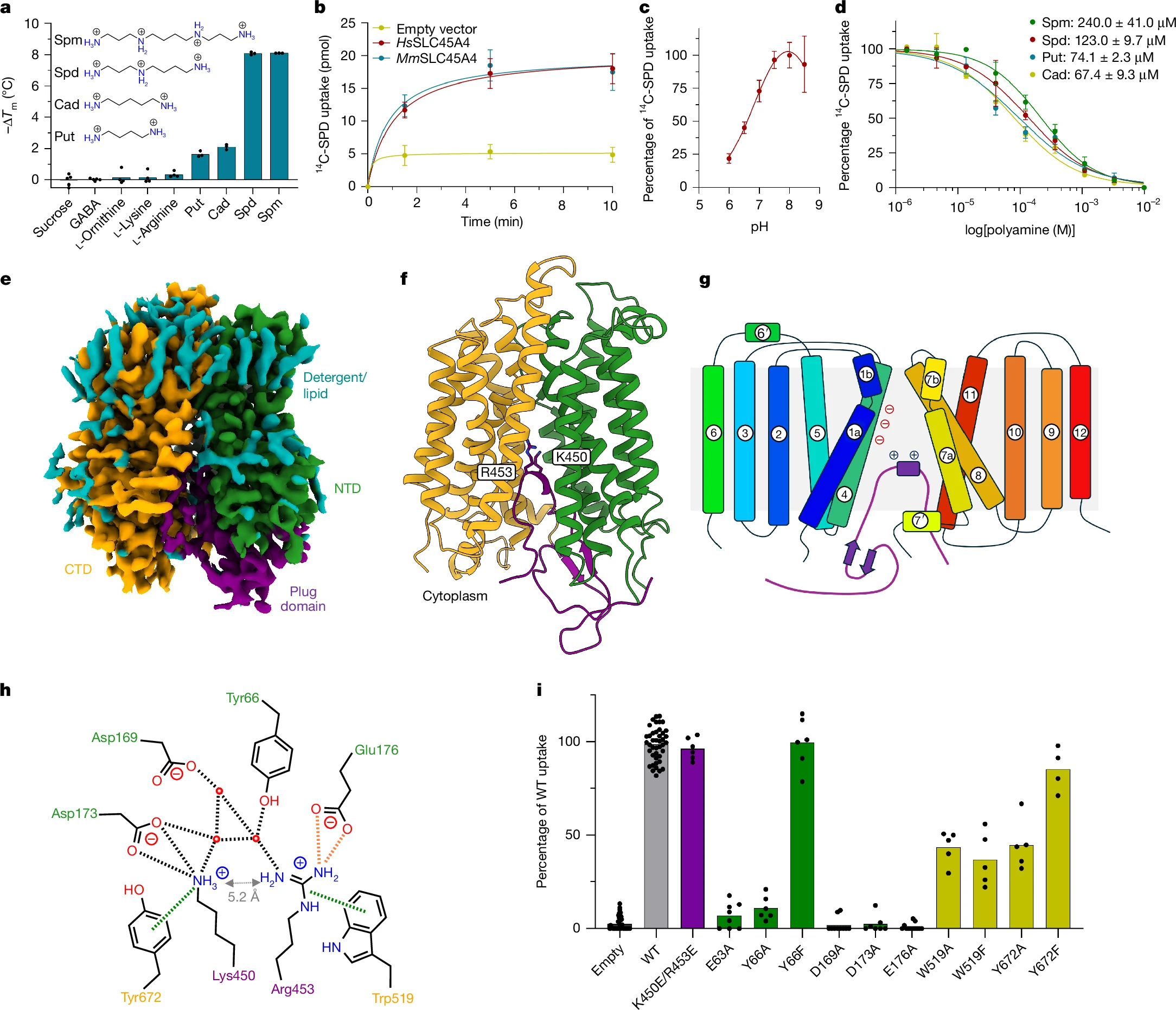
SLC45A4是一种具有插头结构域的多胺转运蛋白
进一步研究揭示,SLC45A4编码的蛋白是一种具有独特结构的血浆膜多胺转运蛋白。此前研究曾推测其为蔗糖转运蛋白,但本研究通过代谢组学关联分析和细胞实验证实,该蛋白能非选择性转运多胺(包括腐胺(Put)、亚精胺(Spd)、精胺(Spm)和尸胺(Cad)),且对不同多胺的亲和力存在差异:Put 和 Cad 的亲和力最高(IC₅₀分别为 74 μM 和 67 μM),其次是 Spd(123 μM)和 Spm(240 μM)。其转运活性在 pH 7.5-8.5 时最佳,且不受赖氨酸、鸟氨酸等阳离子氨基酸的抑制。
冷冻电镜(cryo-EM)结构分析显示,SLC45A4由 12 个跨膜 α 螺旋组成,属于主要易化超家族(MFS)折叠,呈向内开放构象。其独特之处在于跨膜螺旋 6(TM6)和 TM7 之间插入了一个 25.5 kDa 的细胞质插头结构域,该结构域通过赖氨酸(Lys450)和精氨酸(Arg453)与转运蛋白的酸性梯段(如 Asp169、Asp173、Glu176)相互作用,处于自抑制状态,可能通过类似溶酶体多胺转运蛋白 ATP13A2 的膜 destabilization 机制调节多胺释放。
表达分析显示,Slc45a4在小鼠神经系统中广泛表达,尤其在背根神经节(DRG)的所有感觉神经元亚型中富集,包括肽能伤害性感受器(CGRP⁺)、非肽能伤害性感受器(IB4 结合)、C - 低阈值机械感受器(酪氨酸羟化酶⁺)以及有髓机械感受器和本体感受器(NF200⁺),且在大直径 NF200⁺传入神经元中表达量更高。在人类感觉神经元中也检测到SLC45A4的表达,且电转实验证实其定位于细胞膜,符合膜转运蛋白的功能特征。
Slc45a4敲除小鼠的多胺稳态发生显著改变:脊髓中 Spd 水平降低,DRG 中 Put 水平升高,血浆中 Spd 水平升高,表明该转运蛋白在多胺跨细胞转运中起关键作用。行为学实验显示,敲除小鼠的机械敏感性(如 von Frey 毛刺激、针刺)和冷敏感性(干冰刺激)无显著变化,但对伤害性热刺激(48°C 和 50°C 热板)的敏感性降低,热梯度实验中更偏好温暖区域,且福尔马林诱导的第一相疼痛行为(0-15 分钟,与 TRPA1 介导的伤害性感受器直接激活相关)显著减少。
电生理研究进一步揭示,敲除小鼠 DRG 中 IB4⁻伤害性神经元(主要为肽能)的超阈值兴奋性降低,而 IB4⁺神经元无明显变化。在离体皮肤 - 神经制备实验中,C - 机械 - 热伤害性感受器(C-MHs,即 C - 多模态伤害性感受器)对超阈值机械刺激和热刺激(32-50°C)的反应显著减弱,其第一和第二 Spike 阈值升高、放电频率降低。这些结果表明,SLC45A4通过调节 C-MHs 的兴奋性影响热痛和伤害性刺激诱导的强直性疼痛感知。
这项研究首次揭示了SLC45A4作为神经元多胺转运蛋白与慢性疼痛的直接关联,阐明了其通过调节多胺稳态影响 C - 多模态伤害性神经元兴奋性的分子机制。这一发现不仅丰富了对慢性疼痛分子机制的认识,还为开发新型镇痛药物提供了潜在靶点。
目前,临床上常用的镇痛药物多存在疗效有限、副作用大等问题,而针对SLC45A4或其编码蛋白的药物有望通过特异性调节多胺转运来靶向疼痛信号,克服现有疗法的不足。
然而,从基础研究到临床应用仍需更多探索:未来需明确SLC45A4在不同类型慢性疼痛(如炎性痛、神经病理性痛)中的具体作用,解析其与 TRPV1 等多胺敏感离子通道的相互作用,并通过临床前和临床试验验证基于该靶点的镇痛疗法的安全性和有效性。(生物谷Bioon.com)
参考文献:
Middleton, S.J., Markússon, S., Åkerlund, M. et al. SLC45A4 is a pain gene encoding a neuronal polyamine transporter. Nature (2025). doi:10.1038/s41586-025-09326-y
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


