Lab Chip:从“肠”计议!3D生物打印肠芯片,引领药物测试新革命
来源:生物谷原创 2025-01-20 11:00
研究利用同轴生物打印技术成功构建3D肠芯片,筛选出合适生物墨水,打印的管状结构多种细胞共培养良好,在绒毛形成、黏液分泌、屏障功能及药物代谢等方面表现出色,性能优于传统模型。

在医药研发的征程中,寻找更贴合人体生理环境的实验模型一直是科研人员的攻坚方向。近期,Lab Chip的一项创新研究Rapid automated production of tubular 3D intestine-on-a-chip with diverse cell types using coaxial bioprinting通过同轴生物打印技术,成功开发出三维管状肠芯片(IOC),为小肠研究与药物测试领域带来了新的希望之光。

以往,药物研发对动物实验过度依赖,但动物和人类在生理构造与机能上存在较大差异,这使得动物实验结果在预测人体药物反应时准确性欠佳,同时还引发了诸多伦理争议。而口服药物在医疗实践中广泛应用,小肠作为药物吸收的核心器官,构建精确的体外小肠模型对于优化药物递送流程、提升研发成效至关重要。然而,传统的二维transwell模型以及现有肠芯片,在模拟小肠复杂三维结构与功能方面存在明显短板。
为此,科研人员开启了构建新型肠芯片的探索之旅。他们培养Caco-2、EA.hy926和人小肠平滑肌细胞(HSISMC),明确了细致的培养条件与细胞收集方法。同时,制备了多种生物墨水,如3%明胶、1%胶原蛋白、4%海藻酸盐等,并运用流变仪对其性能进行严格检测,以筛选出适配生物打印的材料。借助三层同轴喷嘴与3D生物打印机,打印出模拟小肠形态的管状结构,并将其稳固固定在芯片平台上,还设立二维transwell模型作为对照组。此外,利用细胞标记技术,从多个维度对模型功能展开全方位检测。
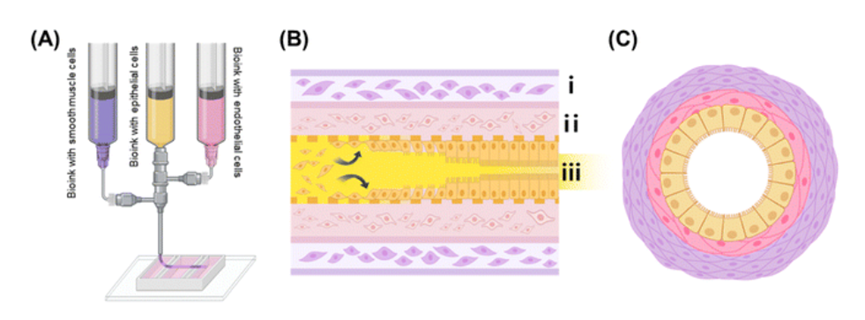
图1. IOC的制造过程
实验发现,3%明胶生物墨水在包裹细胞时效果出色,能均匀分布细胞,且在后续处理中不会对Caco-2细胞的活性产生负面影响。预交联的胶原蛋白生物墨水,经过特定温度处理后,打印性能稳定可靠,无需额外支撑材料辅助。海藻酸盐-胶原蛋白混合生物墨水,不仅具备快速凝胶的特性,而且由于胶原蛋白的添加,显著提升了细胞活力,为细胞营造了适宜长期生长的环境。
打印完成的管状结构内,多种细胞成功实现粘附与共培养。经过7天的培养,细胞活力检测结果显示细胞存活状态良好。三维共聚焦图像清晰呈现出上皮细胞、血管内皮细胞和小肠平滑肌细胞形成了层次分明的结构,成功构建出具有生理功能的三维可灌注体系,与小肠的实际生理结构高度相似。
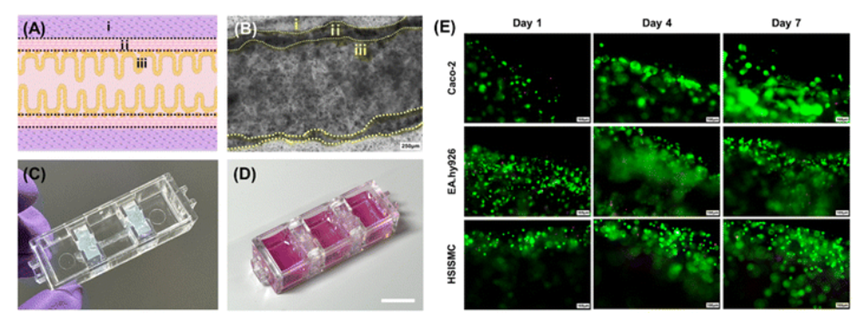
图2. 小肠样管状结构的形成
在动态培养的IOC模型中,成功诱导出高度超100 μm的绒毛。免疫染色和qRT-PCR检测结果表明,与绒毛和隐窝功能紧密相关的LYZ和VIL1基因,在动态IOC模型中的表达水平显著高于二维transwell模型。这充分证明该模型在模拟小肠的吸收和保护功能方面优势显著。
在黏液分泌方面,动态IOC模型的MUC2表达量更高,意味着其黏液分泌功能更强。在屏障功能测试中,IOC模型对荧光染料的阻挡能力远超二维transwell模型,展现出良好的屏障完整性。在药物代谢测试中,IOC模型对乙酰氨基酚的代谢反应符合预期,进一步验证了其在药物测试中的可靠性与有效性。

图3. 体外模型的肠道功能评估
总体而言,这项研究开发的IOC模型,在结构和功能上极大程度地模拟了人体小肠,有效弥补了传统模型的不足。它为小肠研究和药物测试提供了更精准、高效的工具,有望加快药物研发进程,提高研发成功率。随着研究的持续深入,相信这一创新的肠芯片技术将在医药领域发挥更为重要的作用,为人类健康事业开辟新的篇章。(生物谷Bioon.com)
参考文献:
Song H, Hong Y, Lee H. Rapid automated production of tubular 3D intestine-on-a-chip with diverse cell types using coaxial bioprinting. Lab Chip. 2024;25(1):90-101. Published 2024 Dec 17. doi:10.1039/d4lc00731j
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


