中国科学家用自主研发的抗癌药,对抗更难缠、更要命的“男性杀手”
来源:奇点糕 2022-05-24 09:52
“只要一个男人活得足够久,他就很难逃过前列腺癌。”
“只要一个男人活得足够久,他就很难逃过前列腺癌。”
这句广为流传的话凸显了前列腺癌的凶猛。事实上,在80岁以上的男性中,70%的人身体中存在一定数量的前列腺癌细胞。在美国,6位男性中,就有1位在一生中会遭遇前列腺癌[1]。
好消息是,中国男性前列腺癌的发病率远远低于西方。美国前列腺癌发病率为75.7/10万,位居男性癌症发病率首位;而中国仅为6.47/10万,位居第六,相差可谓巨大[2]。
但坏消息是,中国前列腺癌的死亡率远高于美国。造成这种差距的主要原因之一是确诊时的分期。美国前列腺癌初诊患者中仅有7%为转移性疾病[3],而我国这一数据则为50%左右[4]。
图片来源:VEER
AR拮抗剂:一代更比一代强
1942年,离化疗问世还有7年。
这一年,加拿大籍美国外科医生Huggins和他的学生Hodges,在著名期刊 Cancer Research上发表了一篇划时代的论文[5]。
他们的研究显示,用手术切除睾丸或者用雌激素拮抗雄激素,可以延缓转移性前列腺癌的进展,同时表明,雄激素在前列腺癌的发展中起着至关重要的作用。Huggins也因此于1966年获得了诺贝尔生理学或医学奖。
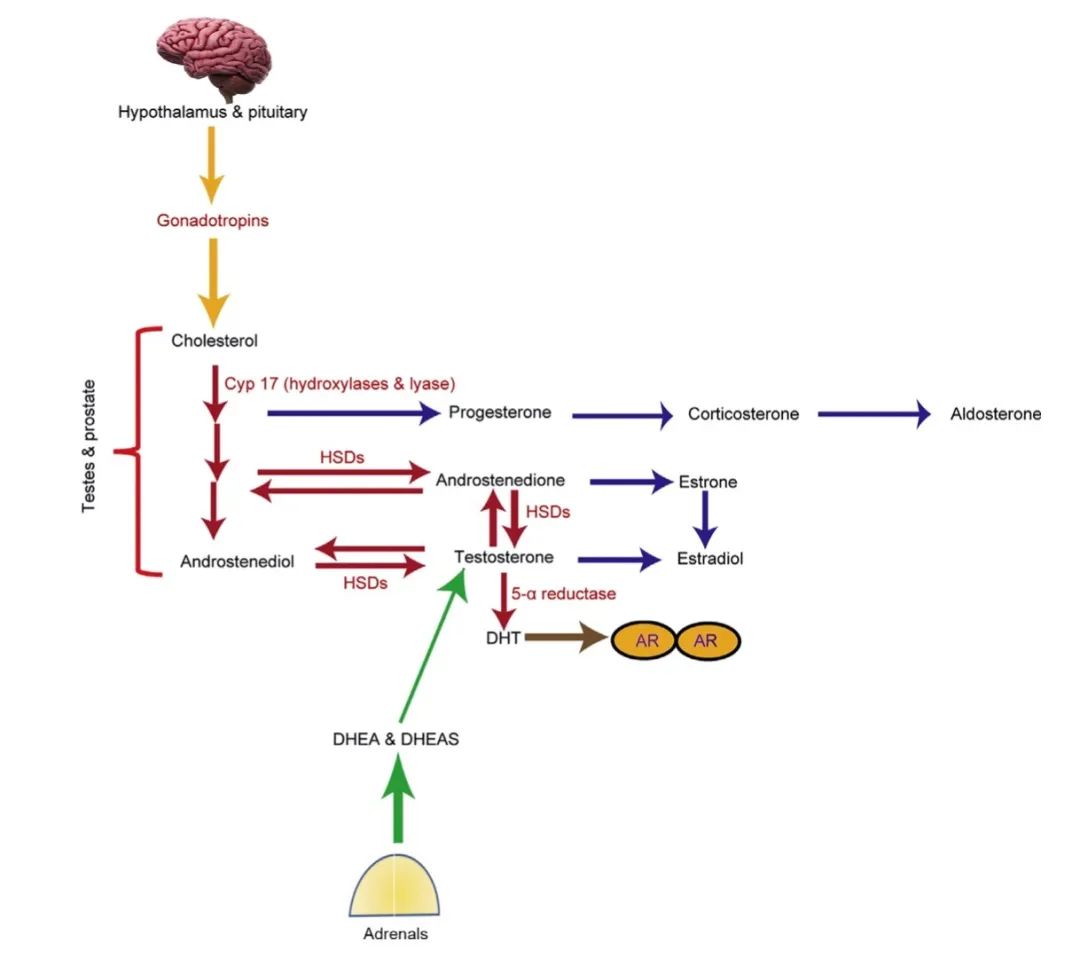
以雄激素及其受体为靶点的药物开发思路
Huggins的伟大研究让前列腺癌的治疗进入了与雄激素对抗的新纪元,并随之产生了三个技术路线。第一是雄激素剥夺治疗(ADT),直接抑制睾丸合成雄激素;第二是CYP17酶抑制剂,抑制雄激素合成过程中的必需酶;第三是雄激素受体(AR)拮抗剂,与雄激素竞争性地结合AR,阻止癌细胞的增殖。
这其中,研究最为火热的当属AR拮抗剂。
在前列腺癌的治疗中,AR的确是一个绝佳的靶点。在Huggins之后,几十项前瞻性分析都证明,雄激素与AR结合是前列腺癌发展的重要驱动力,并且几乎所有的前列腺癌病例AR均为阳性[6]。
烈火烹油的研究很快转化为临床成果。1985年左右,全球首个第一代AR拮抗剂氟他胺上市。十年后,第二款一代AR拮抗剂比卡鲁胺上市[7]。
比卡鲁胺衍生自氟他胺,这两款药物可谓是同胞兄弟,但比卡鲁胺对AR的亲和力要比氟他胺高4~5倍,药效更强,成为第一代AR拮抗剂的主流。但不幸的是,持续暴露于比卡鲁胺会导致AR配体结合域W741发生突变,将比卡鲁胺转化为激动剂,发挥和雄激素类似的功能,最终造成治疗失败[8]。
图片来源:VEER
为第二代AR拮抗剂开山的是两位大牛科学家:纪念斯隆凯特琳癌症中心的Charles Sawyers,和加州大学洛杉矶分校的Michael Jung,他们通力合作研发出了全球首个第二代AR拮抗剂恩扎卢胺。值得一提的是,Sawyers还曾因参与格列卫的开发,而获得了拉斯克奖。
数据显示,恩扎卢胺对AR的亲和力是比卡鲁胺的8~10倍[9],并且可以抑制AR核转位。更重要的是,恩扎卢胺在一系列测试中均未发现激动剂现象。
2012年,恩扎卢胺被FDA批准上市,用于治疗转移性去势抵抗性前列腺癌(mCRPC)[10]。2018年,第二款二代AR拮抗剂阿帕他胺也获批上市,用于治疗非转移性去势抵抗性前列腺癌(nmCRPC)[11]。2019年,第三款二代AR拮抗剂达罗他胺获批上市,适应症为nmCRPC[12]。
第二代AR拮抗剂无疑将治疗标准推到了一个新的高度,但并非完美无缺。
在恩扎卢胺的1/2期研究中,3 名患者发生癫痫[13]。在3期AFFIRM研究中,恩扎卢胺组有5名患者(0.6%)发生癫痫,而安慰剂组未发生癫痫[14]。同样在3期ENZAMET研究中,恩扎卢胺组有7名患者(1%)发生癫痫,安慰剂组未发生癫痫,同时,恩扎卢胺组临床显著性疲劳也更常见(25% vs 14%)[15]。后续的研究发现,恩扎卢胺的中枢神经毒性可能与GABAa的拮抗活性以及血脑屏障穿透性相关[16]。
图片来源:VEER
阿帕他胺虽然在中枢神经毒性方面有所改善,但并未完全杜绝癫痫。在3期SPARTAN研究中,仍然有2名患者(0.2% )发生了癫痫,而安慰剂组无癫痫发生。同时,阿帕他胺组的疲劳发生率相较安慰剂组也更高(30.4% vs 21.1%)。除此之外,阿帕他胺组的皮疹发生率也远高于安慰剂组(23.8% vs 5.5%)[17]。
寻找更完美的AR拮抗剂
世界上有没有完美的小分子药物呢?或许有,但绝不可能一击命中。
2009年,Charles Sawyers和Michael Jung带领的团队,在顶级期刊《科学》上发表文章,解密了恩扎卢胺的发现过程。
他们首先筛选了一种先导化合物——非甾体激动剂 RU59063。随后对 RU59063的结构做了调整,将激动剂转变为拮抗剂。此后,他们又测试了近两百个结构优化方案,最后选定了MDV3100和RD162两款候选化合物。鉴于MDV3100具有更好的成药性,研究团队选定MDV3100进行临床试验[9],成为最终的恩扎卢胺。
仍然是Sawyers和Jung团队,他们在不久之后,又基于前述的候选化合物,经过结构优化,获得了一种新的小分子ARN-509,也就是阿帕他胺[18]。
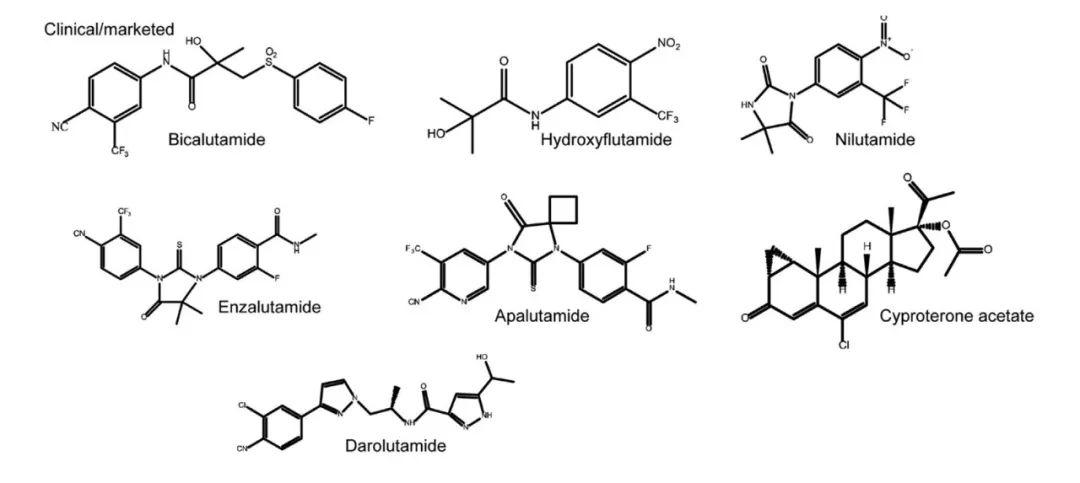
几款AR拮抗剂的分子结构
就在恩扎卢胺上市后的第二年,中国恒瑞医药的科学家看到了进一步寻找完美小分子的机遇。
“恒瑞在瑞维鲁胺立项的时候,主要有两个愿景,第一,我们希望开发出中枢神经安全性更高的药物;第二,我们希望提高前列腺癌创新药在中国的可及性和可负担性。”恒瑞全球研发总裁张连山告诉奇点网。
恒瑞的科学家以MDV3100为先导化合物,制定了几项重要的结构优化目标:最大程度降低药物的血脑屏障通透性,尽可能避免中枢神经毒性;进一步优化药物的药代动力学(PK)特征;尽可能提升小分子的成药性。
在设计之初,研究团队发现,恩扎卢胺在动物体内的主要代谢途径是氧化、脱甲基及水解反应,而其代谢物和原型药物活性相当。进一步发现,MDV3100脱甲基和水解代谢反应的位点主要在分子末端的N-甲基酰胺基团上。这意味着,这个尾链片段允许有较大的改动,在不影响药物活性的情况下,还可以减少临床上的活性代谢物,简化后续的研究。
同时,为了达到进一步降低中枢神经系统副作用的目的,增强分子的极性,降低药物的血脑屏障通透性,也是立项初始的重要目标。
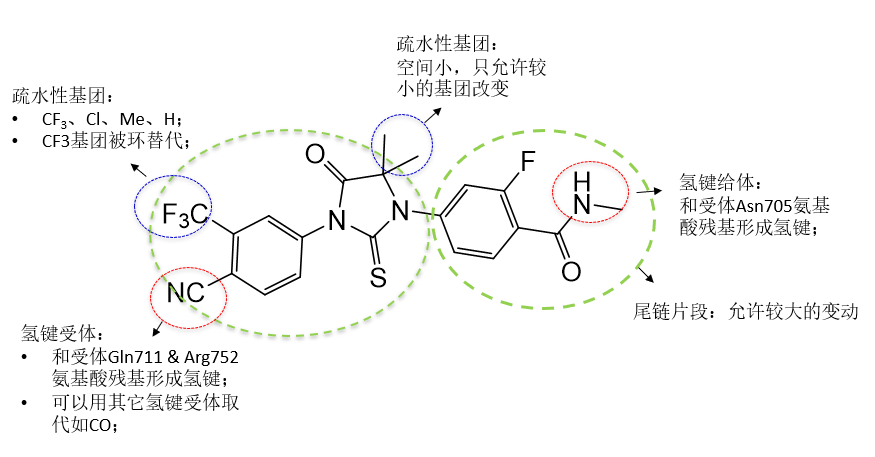
先导化合物结构分析(恒瑞供图)
在此基础上,研究团队先后对先导分子的左侧疏水性基团、中心母核片段和右侧尾链片段分别进行优化,重点放在对右侧的N-甲基苯甲酰胺基团的修饰和优化上。
首先,去掉尾链的N-甲基酰胺基团,引入代谢稳定的杂环氧基,得到第1个候选化合物。这款化合物体外活性与恩扎卢胺接近,但其疏水性常数(clogP)较高,hERG抑制作用较强,且大鼠口服吸收差,因此没有继续评价。
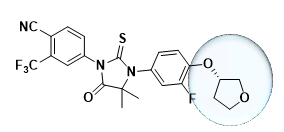
候选化合物1(恒瑞供图)
需要说明的是,clogP高意味着化合物的亲脂性高,往往导致低水相溶解度和口服吸收利用度差。而hERG抑制性是早期发现阶段评价药物心脏毒性最重要的指标。
接下来进入第二轮优化。在第1个候选化合物的杂环氧基上引入羟基取代基,得到了第2个候选化合物。这款化合物体外活性略优于恩扎卢胺。与候选化合物1相比,分子极性增加,ClogP降低,hERG抑制作用也大大降低,同时大鼠口服吸收利用度也有了大幅提升。
美中不足的是,这款化合物结构较为复杂,分子中含有两个手性中心,合成难度高,在药物的可开发性上不是很优异。
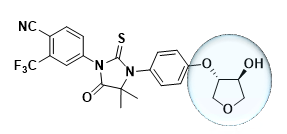
候选化合物2(恒瑞供图)
接着进一步优化。这次研究人员将第2个候选化合物的杂环基开环,得到了最终的化合物瑞维鲁胺(SHR3680)。瑞维鲁胺体外拮抗活性略优于恩扎卢胺,也没有AR激动活性,hERG抑制也进一步下降。
更重要的是,瑞维鲁胺在小鼠脑组织中药物浓度与血药浓度比值远低于恩扎卢胺(MDV 3100:0.607-0.773,SHR3680:0.159-0.198 )[19],且对GABAa的拮抗作用弱,因此诱导癫痫发作的可能性更小。
最后,瑞维鲁胺仅有一个手性中心,其手性原料简单易得,药物可开发性更强。
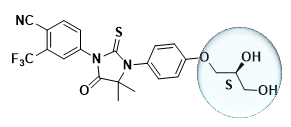
瑞维鲁胺分子结构(恒瑞供图)
回顾整个分子结构的优化过程,就会发现,双羟基的引入,非常巧妙地达成了设计之初的几个目标。
首先,双羟基的引入,各主要作用基团相互作用基本保留,叔醇羟基和靶点Leu-880形成额外的氢键作用,体外活性略优;从安全角度出发,引入双羟基的基团,会增大分子极性,提高水溶性,降低血脑屏障的通透能力,从而降低癫痫及其他中枢神经系统副作用的风险;同时,增大极性有利于改善hERG抑制性,降低心血管风险。
其次,从药物代谢位点出发,改变代谢位点,减少其代谢清除,提高了同剂量条件下原型药物的暴露水平;同时,水溶性的增加,也提高了药物暴露水平,更适合开发普通制剂;原料易得,合成简单。
瑞维鲁胺优异的理化和生化特性,也体现在了最终的药代动力学数据上。
恩扎卢胺、阿帕他胺以及达罗他胺三款药物的批准剂量分别为160 mg qd,240 mg qd和600 mg bid,瑞维鲁胺的临床推荐剂量为240 mg qd。
在稳态下,瑞维鲁胺的药物体内总暴露量曲线下面积(AUC)为 649 μg*h/mL[19],恩扎卢胺为321.5 μg*h/mL[20],阿帕他胺为100 μg*h/mL[21]。而每次600mg,一天给药两次的达罗他胺稳态AUC为105.6 μg*h/mL[22]。可见,在临床剂量下,瑞维鲁胺具有很高的药物暴露水平。
瑞维鲁胺的药物消除半衰期为4天,恩扎卢胺、阿帕他胺和达罗他胺的药物消除半衰期分别为5.8天、3 天、以及20小时。可以看出达罗他胺半衰期相对较短,再加上其空腹口服生物利用度仅为30%(和食物同服能提高2-2.5倍),因此需要较高的剂量和更频繁的给药次数。
那么,经过这一系列的优化,瑞维鲁胺的中枢神经安全性如何呢?
瑞维鲁胺1/2期研究显示,接受治疗的197 名患者均未报告任何级别的癫痫发作,精妙的药物优化设计转化成了可见的临床获益[19]。
2018年6月,瑞维鲁胺启动首个3期研究,适应症为转移性激素敏感性前列腺癌(mHSPC)。相较于阿帕他胺的同类关键研究,瑞维鲁胺的研究设计有三点不同,第一是研究人群仅限高肿瘤负荷患者,因为这个群体的预后更差,对新治疗的需求也更大;第二,研究的对照组是比卡鲁胺,而非安慰剂,这是因为,在研究启动时,比卡鲁胺为国内临床上广泛可及的标准治疗药物选择;第三,研究纳入了大量中国患者,为中国临床使用提供更坚实的证据。
基于这项3期研究的初步结果,2021年10月,瑞维鲁胺向国家药监局递交了首个上市申请,并被纳入优先审评审批程序,该研究的完整结果将在今年ASCO年会上以口头汇报的形式进行首次公布。2021年,瑞维鲁胺又启动了第二个关键3期研究用于高危局限性前列腺癌患者的围手术期治疗,这是全球第二个新型AR拮抗剂围手术期治疗前列腺癌的国际多中心关键研究。
我们也期待在不久的将来,国产创新药瑞维鲁胺能够为中国前列腺癌患者带来更多获益。
参考文献:
【1】Pollock PA, Ludgate A, Wassersug RJ. In 2124, half of all men can count on developing prostate cancer. Curr Oncol. 2015 Feb;22(1):10-2.
【2】李星,曾晓勇. 中国前列腺癌流行病学研究进展[J]. 肿瘤防治研究,2021,48(1):98-102.
【3】Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer statistics, 2022. CA Cancer J Clin. 2022 Jan;72(1):7-33.
【4】中国抗癌协会泌尿男生殖系肿瘤专业委员会. 2018版转移性前列腺癌诊治中国专家共识. 中华外科杂志,2018,56(9):646-652.
【5】Huggins, Chakles M.D. EFFECT OF ORCHIECTOMY AND IRRADIATION ON CANCER OF THE PROSTATE, Annals of Surgery: June 1942 - Volume 115 - Issue 6 - p 1192-1200.
【6】Narayanan R. Therapeutic targeting of the androgen receptor (AR) and AR variants in prostate cancer. Asian J Urol. 2020 Jul;7(3):271-283.
【7】Narayanan R. Therapeutic targeting of the androgen receptor (AR) and AR variants in prostate cancer. Asian J Urol. 2020 Jul;7(3):271-283.
【8】Bohl CE, Gao W, Miller DD, Bell CE, Dalton JT. Structural basis for antagonism and resistance of bicalutamide in prostate cancer. Proc Natl Acad Sci U S A. 2005 Apr 26;102(17):6201-6.
【9】Tran C, Ouk S, Clegg NJ, Chen Y, Watson PA, Arora V, Wongvipat J, Smith-Jones PM, Yoo D, Kwon A, Wasielewska T, Welsbie D, Chen CD, Higano CS, Beer TM, Hung DT, Scher HI, Jung ME, Sawyers CL. Development of a second-generation antiandrogen for treatment of advanced prostate cancer. Science. 2009 May 8;324(5928):787-90.
【10】https://www.drugs.com/history/xtandi.html
【11】https://www.drugs.com/history/erleada.html
【12】https://www.drugs.com/history/nubeqa.html
【13】Scher HI, Beer TM, Higano CS, Anand A, Taplin ME, Efstathiou E, et al. Antitumour activity of MDV3100 in castration-resistant prostate cancer: a phase 1-2 study. Lancet. 2010;375(9724):1437–46.
【14】Scher HI, Fizazi K, Saad F, Taplin ME, Sternberg CN, Miller K, et al. Increased survival with enzalutamide in prostate cancer after chemotherapy. N Engl J Med. 2012;367(13):1187–97.
【15】Davis ID, Martin AJ, et,al. ENZAMET Trial Investigators and the Australian and New Zealand Urogenital and Prostate Cancer Trials Group. Enzalutamide with Standard First-Line Therapy in Metastatic Prostate Cancer. N Engl J Med. 2019 Jul 11;381(2):121-131.
【16】Foster WR, Car BD, Shi H, Levesque PC, Obermeier MT, Gan J, et al.Drug safety is a barrier to the discovery and development of newandrogen receptor antagonists. Prostate 2010;71:480–8.
【17】Smith MR, Saad F, Chowdhury S, Oudard S, Hadaschik BA, Graff JN, Olmos D, Mainwaring PN, Lee JY, Uemura H, Lopez-Gitlitz A, Trudel GC, Espina BM, Shu Y, Park YC, Rackoff WR, Yu MK, Small EJ; SPARTAN Investigators. Apalutamide Treatment and Metastasis-free Survival in Prostate Cancer. N Engl J Med. 2018 Apr 12;378(15):1408-1418.
【18】Clegg NJ, Wongvipat J, Joseph JD, Tran C, Ouk S, Dilhas A, Chen Y, Grillot K, Bischoff ED, Cai L, Aparicio A, Dorow S, Arora V, Shao G, Qian J, Zhao H, Yang G, Cao C, Sensintaffar J, Wasielewska T, Herbert MR, Bonnefous C, Darimont B, Scher HI, Smith-Jones P, Klang M, Smith ND, De Stanchina E, Wu N, Ouerfelli O, Rix PJ, Heyman RA, Jung ME, Sawyers CL, Hager JH. ARN-509: a novel antiandrogen for prostate cancer treatment. Cancer Res. 2012 Mar 15;72(6):1494-503.
【19】Qin X, Ji D, Gu W, Han W, Luo H, Du C, Zou Q, Sun Z, He C, Zhu S, Chong T, Yao X, Wan B, Yang X, Bai A, Jin C, Zou J, Ye D. Activity and safety of SHR3680, a novel antiandrogen, in patients with metastatic castration-resistant prostate cancer: a phase I/II trial. BMC Med. 2022 Mar 4;20(1):84.
【20】NDA Multi-disciplinary Review and Evaluation :Xtandi (enzalutamide)
【21】NDA/BLA Multi-Disciplinary Review and Evaluation NDA 210951 :Erleada (apalutamide)
【22】NDA212099 Multi-disciplinaryReviewandEvaluation :Darolutamide/NUBEQA
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


