Adv Sci | 中山大学聂燕/黄迪/杨林槟/宋尔卫等合作发现基底样乳腺癌的潜在治疗新靶点
来源:生物探索 2024-03-21 09:43
该研究旨在研究BLBC特异性TFs在调节肿瘤进展中的作用,以探索针对BLBC的新治疗策略。
中山大学聂燕、黄迪、杨林槟及宋尔卫等合作在Advanced Science在线发表题为“Activation of Bivalent Gene POU4F1 Promotes and Maintains Basal-like Breast Cancer”的研究论文,在生物信息学分析确定的BLBC高活性候选TFs中,POU4F1在BLBC中唯一上调,并与不良预后相关。POU4F1通过直接结合CDK2和CCND1启动子调节G1/S转变,是BLBC肿瘤生长和恶性表型所必需的。
更重要的是,POU4F1通过CDK2介导的EZH2磷酸化和随后的ESR1启动子中的H3K27me3修饰来抑制ERα表达,从而维持BLBC的身份。敲除BLBC细胞中的POU4F1重新激活功能性ERα表达,使BLBC对他莫昔芬治疗敏感。深入的表观遗传学分析表明,POU4F1启动子中二价染色质的亚型特异性重新配置和激活有助于其在BLBC中的独特表达,并由DNA去甲基化酶TET1维持。这些结果揭示了亚型特异性表观遗传激活的TF在促进和维持BLBC中起关键作用,表明POU4F1是BLBC的潜在治疗靶点。

乳腺癌是世界上最常见的癌症,在2020年首次超过肺癌。基底样乳腺癌(Basal-like breast cancer, BLBC),约占乳腺癌的15%-20%,是根据乳腺癌的转录程序进行分类的,具有增殖活性高、细胞周期检查点失调的特点。约75%的BLBC为三阴性乳腺癌(TNBCs),不表达雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2 (HER2)。因此,内分泌治疗和HER2靶向治疗是无效的,手术和化疗仍然是主要的治疗方法。
BLBC本身具有侵袭性的临床行为,再加上缺乏有效的分子靶点,导致BLBC预后不良。尽管有大量关于BLBC的遗传信息,但没有明确的BLBC遗传致癌驱动因素。因此,探索BLBC的发生和发展机制对于发现新的BLBC治疗靶点至关重要。
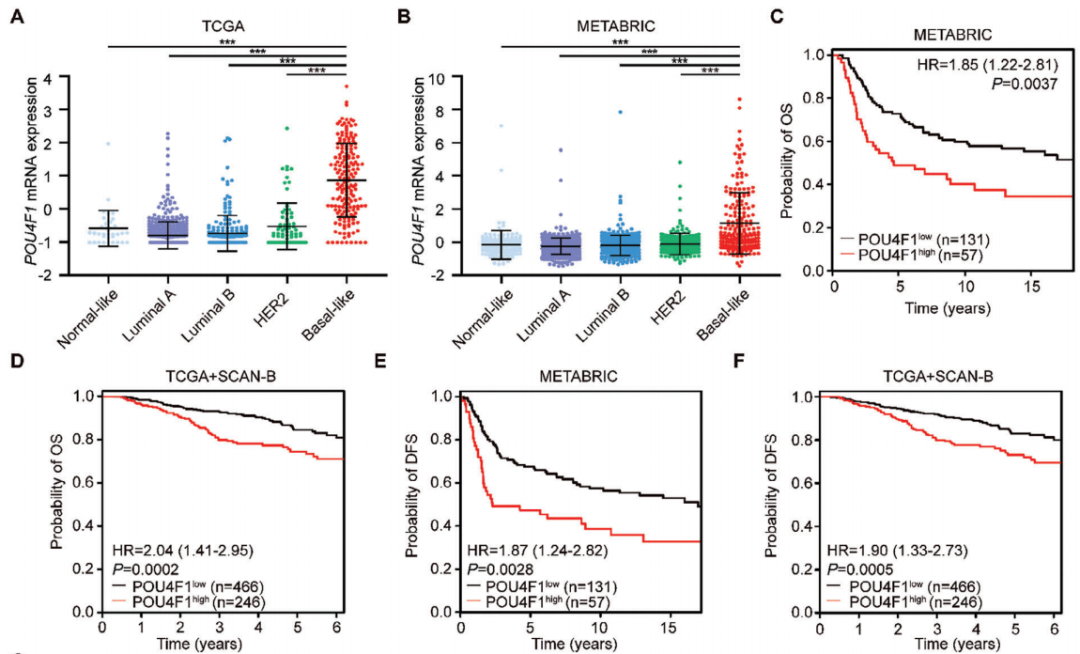
POU4F1在BLBC中表达上调,与预后不良相关(Credit: Advanced Science)
转录失调是癌症的一个标志,可能是癌症发生和发展的重要驱动因素。越来越多的研究证实,转录程序失调可由转录因子(transcription factors, TFs)主导,它是参与基因转录调控的关键蛋白。有限的TFs在特定癌症类型中过度活跃,代表了一类独特的药物靶点。例如,ERα是调节乳腺癌腔内表型的主要TFs之一,也是内分泌治疗的关键靶点。然而,BLBC的主要TFs和潜在的调控机制仍不清楚。
TFs特异性结合基因组启动子和增强子的DNA序列。越来越多的研究表明,TF结合增强子区域在DNA甲基化谱中发生了显著改变,并与细胞类型特异性基因表达密切相关。在乳腺癌中,增强子区域的异常DNA甲基化已被证明与不同的分子亚型相关。因此,癌症特异性TF可以从含有假定的TF结合位点的增强子区域的DNA甲基化谱中推断出来。该研究旨在研究BLBC特异性TFs在调节肿瘤进展中的作用,以探索针对BLBC的新治疗策略。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


