Mol Cell:张永有团队揭示硫化氢介导的代谢重塑促进肺癌细胞铁死亡
来源:生物探索 2024-10-01 11:37
本研究不仅揭示了H2S促进铁死亡的分子机制,还指出SAHH作为潜在的肿瘤治疗靶点的价值,同时也为基于气体信号分子和铁死亡调控的肿瘤治疗交叉领域提供新的思路。
厦门大学张永有教授团队在Molecular Cell上发表了文章 Hydrogen sulfide-mediated persulfidation regulates homocysteine metabolism and enhances ferroptosis in non-small-cell lung cancer 。该研究深入解析了H2S介导的过硫化修饰,抑制SAHHH活性,重塑同源半胱氨酸代谢,增强非小细胞肺癌(NSCLC)细胞对铁死亡敏感性的分子机制,为潜在的肺癌治疗开辟了新方向。
在机制探究中,研究团队利用代谢组学发现H2S导致NSCLC细胞含硫氨基酸代谢异常,并增加胱氨酸耗竭诱导的铁死亡条件下脂质过氧化和ROS的生成;进一步蛋白组学分析发现H2S特异性地过硫化修饰S-腺苷同型半胱氨酸水解酶(S-adenosyl homocysteine hydrolase, SAHH)的第195位半胱氨酸残基,抑制SAHH的酶活性,进而减少下游同型半胱氨酸的生成。在胱氨酸受限的环境下,这一效应加剧半胱氨酸及谷胱甘肽的耗竭,最终促进NSCLC细胞的铁死亡。尤为关键的是,同型半胱氨酸能够逆转H2S促进的铁死亡,也验证了H2S通过调控同型半胱氨酸代谢影响铁死亡进程的分子机制。
此外,SAHH作为这一过程中的关键调控因子,其表达水平与酶活性直接影响铁死亡进程;敲低SAHH表达增强NSCLC细胞对铁死亡的敏感性,进一步证实了SAHH在铁死亡调控中的重要作用。临床样本和数据库的分析结果也表明SAHH的高表达与肺腺癌患者预后不良呈现正相关。因此,调控SAHH活性或干扰其过硫化修饰过程,为肺癌治疗提供潜在的新策略。
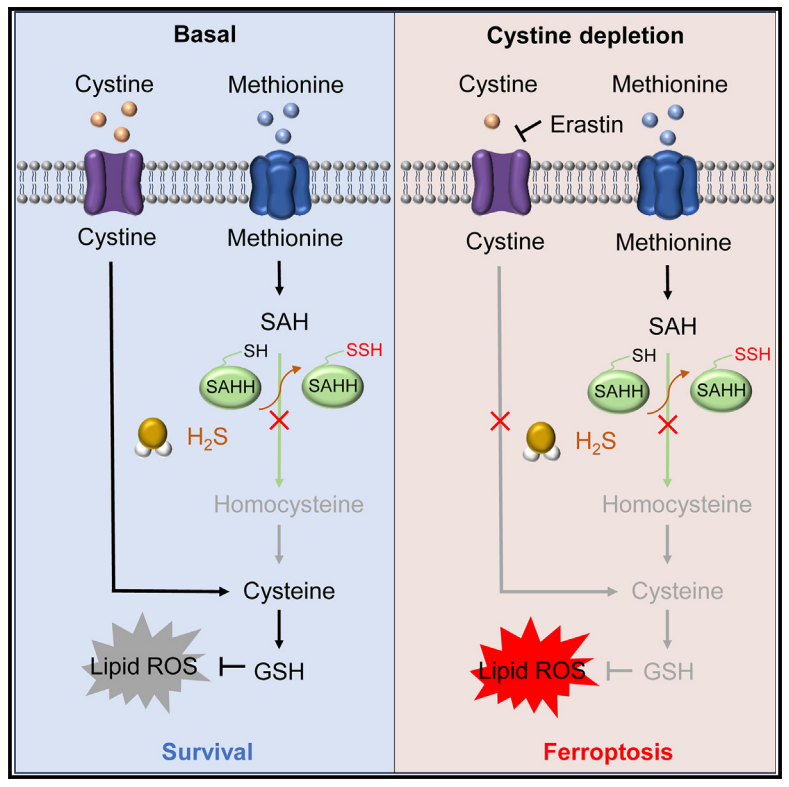
模式图(Credit: Molecular Cell)
这一发现不仅揭示了H2S促进铁死亡的分子机制,还指出SAHH作为潜在的肿瘤治疗靶点的价值,同时也为基于气体信号分子和铁死亡调控的肿瘤治疗交叉领域提供新的思路。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


