Cell Research: 科学家揭示了一种代谢酶参与细胞的代谢过程并抑制结直肠肿瘤的发生
来源:生物谷原创 2023-02-09 11:42
磷酸化在细胞周期、生长、凋亡和信号转导等多个细胞过程中起着重要的调节作用。蛋白质的可逆磷酸化是通过相互对立的激酶和磷酸酶的活性来完成的。
磷酸化在细胞周期、生长、凋亡和信号转导等多个细胞过程中起着重要的调节作用。蛋白质的可逆磷酸化是通过相互对立的激酶和磷酸酶的活性来完成的。磷酸化可溶性代谢产物的代谢酶,如丙酮酸激酶亚型M2、磷酸甘油酸激酶1、己糖激酶和核苷二磷酸激酶1和2,也可以作为蛋白激酶并磷酸化各种蛋白质底物来调节Warburg效应、基因表达、细胞周期进展和增殖、细胞凋亡、自噬、外体分泌、T细胞激活、铁运输、离子通道开放和许多其他基本的细胞功能。
然而,代谢酶是否具有蛋白质磷酸酶的功能,如果是的话,它参与了哪个细胞过程,还没有被探索。

图片来源: https://doi.org/10.1038/s41422-022-00773-0
近日,来自中国科学院大学的研究者们在Cell Research杂志上发表了题为“Fructose-1,6-bisphosphatase 1 dephosphorylates IκBα and suppresses colorectal tumorigenesis”的文章,本研究发现揭示了FBP1作为一种蛋白磷酸酶之前未被认识到的作用,并确立了FBP1介导的IκBα去磷酸化在结直肠肿瘤发生中的关键作用。
越来越多的证据表明,一些可磷酸化可溶性代谢物的代谢酶也可以磷酸化多种蛋白质底物,如蛋白激酶,以调节细胞周期、细胞凋亡和许多其他基本的细胞过程。然而,代谢酶是否作为一种蛋白磷酸酶使蛋白质去磷酸化仍是未知的。
在本研究中,研究者揭示了葡萄糖异生酶1,6-二磷酸果糖酶(FBP1),它催化1,6-二磷酸果糖(F-1,6-BP)的水解成6-磷酸果糖(F-6-P)作为一种蛋白质磷酸酶,通过分子对接和分子动力学(MD)模拟高通量筛选代谢性磷酸酶。
此外,研究者通过磷酸蛋白质组学分析确定IκBα是Fbp1介导的去磷酸化的底物。在机制上,Fbp1直接与I-κBα的丝氨酸(S)32/36在肿瘤坏死因子α刺激下相互作用并去磷酸化,从而抑制核因子-κB的激活。
分子动力学模拟表明,Fbp1介导的IκBα去磷酸化的催化机理与F-1,6-BP去磷酸化类似,只是IκBα去磷酸化的势垒较高。在功能上,依赖于Fbp1的NF-κB失活通过使肿瘤细胞对炎症应激敏感并阻止髓系来源的抑制细胞的动员来抑制结直肠肿瘤的发生。
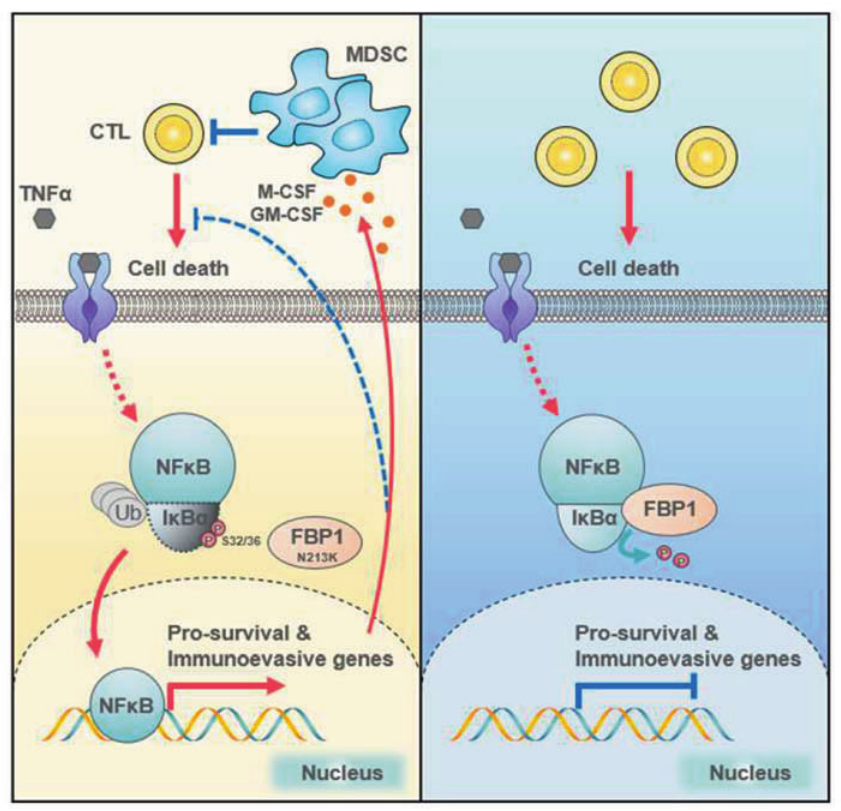
结直肠癌组织中Fbp1的表达与NF-κB的活化、细胞存活和多药耐药干细胞的侵袭呈负相关
图片来源: https://doi.org/10.1038/s41422-022-00773-0
在本研究中,研究者通过使肿瘤细胞对炎性应激诱导的细胞死亡敏感,建立了FBP1在结直肠癌初始肿瘤生长中的肿瘤抑制作用。在机制上,Fbp1与IκBα相互作用,并在肿瘤坏死因子α刺激下使其去磷酸化,从而阻止IκBα的降解,并减弱随后的NF-κB激活。
在启动的恶性细胞中失活的NF-κB通过下调细胞生存基因而降低其在炎性微环境中的存活率。同时,在NF-κB失活细胞中,TgFb1、Csf1、Csf3和Kit1的表达水平也下降,从而通过阻止MDSCs的动员来促进CTL的侵袭和抗肿瘤免疫。这两种机制都参与了FBP1的抑瘤活性。(生物谷 Bioon.com)
参考文献
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


