Science重磅:AI设计蛋白新突破,David Baker团队设计出响应刺激的双态铰链蛋白!
来源:brainology 2023-08-22 10:45
总的来说,这项新研究开发出了同时具有两种明确状态的铰链蛋白,可以应用于“蛋白质开关”的设计。这种双态开关的研究能使蛋白质设计超越静态结构,转向更复杂的多态组装和生物传感器设计,为蛋白设计提供了更广阔的
蛋白质设计领域先驱、华盛顿大学 David Baker 教授在 Sicence 期刊发表了题为:Design of stimulus-responsive two-state hinge proteins 的研究论文。
该研究通过人工智能(AI)辅助设计,开发出一种铰链样蛋白质,这种铰链蛋白同时具有两种明确的构象,在与目标蛋白结合时显示出稳定的构象变化,因此可以根据这种特异性定制出“蛋白质开关”。这项工作为产生响应生物刺激的蛋白质开关提供了研究基础,为蛋白设计领域带来全新变革!
在自然界中,许多天然蛋白质可以在两种构象之间转换以响应环境刺激,例如目标分子的结合、翻译后修饰或 pH 的变化。这个过程在结构上类似于晶体管控制计算设备中的电子信息流,只不过蛋白质传递的是生化信息。
然而,天然蛋白质都是经过漫长的进化才衍化得来,人工设计的蛋白往往很难做到在两种折叠状态之间进行这样的构象转换。因为人工蛋白质设计通常旨在优化一个单一的、非常稳定的构象,使其拥有折叠能量景观的全局最小值。
因此,如何设计出同时具有两种不同构象且结构完整的人工蛋白质是蛋白质设计领域的一个重大挑战。其中,最关键的一个要求是,所设计的蛋白质需要同时具有两个不同最小值的能量景观,就像一座山峰之中同时有两个山坳,一片沙漠之中同时有两个绿洲。
在这项最新研究中,David Baker 团队描述了一种铰链蛋白的设计概念,这种蛋白具有两个明确定义和结构的构象状态:在没有配体的情况下表现为X设计状态,而在配体存在的情况下通过构象变化转换为 Y 设计状态。
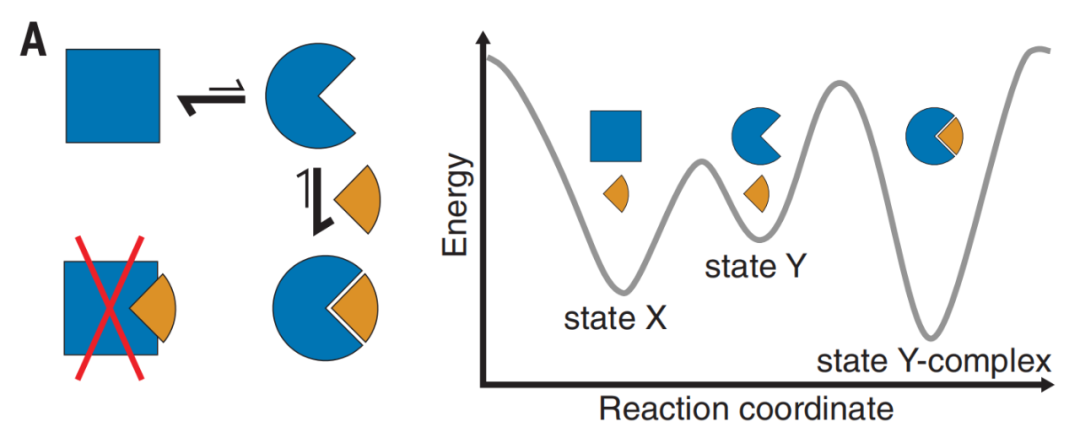
研究小组通过 X 射线晶体学、电子显微镜、双电子-电子共振光谱等技术对设计的铰链蛋白的蛋白质结构、结合动力学和构象平衡进行了全面表征。研究结果表明,尽管存在显著的结构差异,但这两种构象状态的设计具有原子水平的精度,并且构象平衡和结合平衡是紧密耦合的。
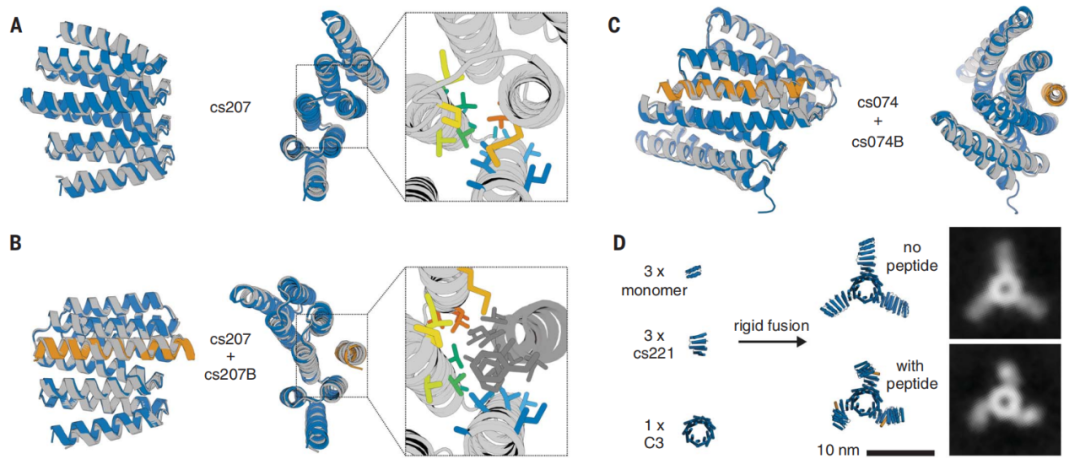
因此,这种铰链蛋白可以广泛适用于蛋白质开关的设计,就像是电子电路中的晶体管一样,研究人员可以将蛋白质开关与外部输出和输入耦合,其状态转换通过与天然蛋白(例如胰高血糖素、神经肽、分泌素)结合而不是人工设计肽。
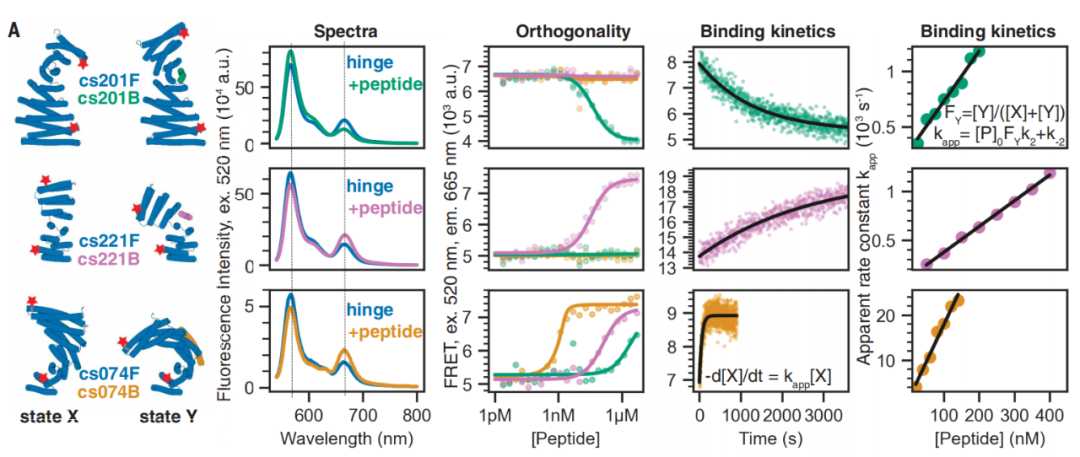
基于这种设计的铰链蛋白可以用于创建生物传感设备,并将它们合并到更大的蛋白质系统中,以解决各种突出的设计挑战:铰链蛋白可以作为一种模块,在其内部安装特定的酶活位点,从而实现两种明确构象的切换——当底物结合时有利于一种状态,当产物释放时有利于另一种状态。
这对于之前的 LOCKR 开关而言是不可能的,因为 LOCKR 开关只有一个明确的构象,另一个状态往往是无序的。缺乏定义的第二状态使得它不适合于构建蛋白质开关或基于离散状态的计算系统中的机械耦合。
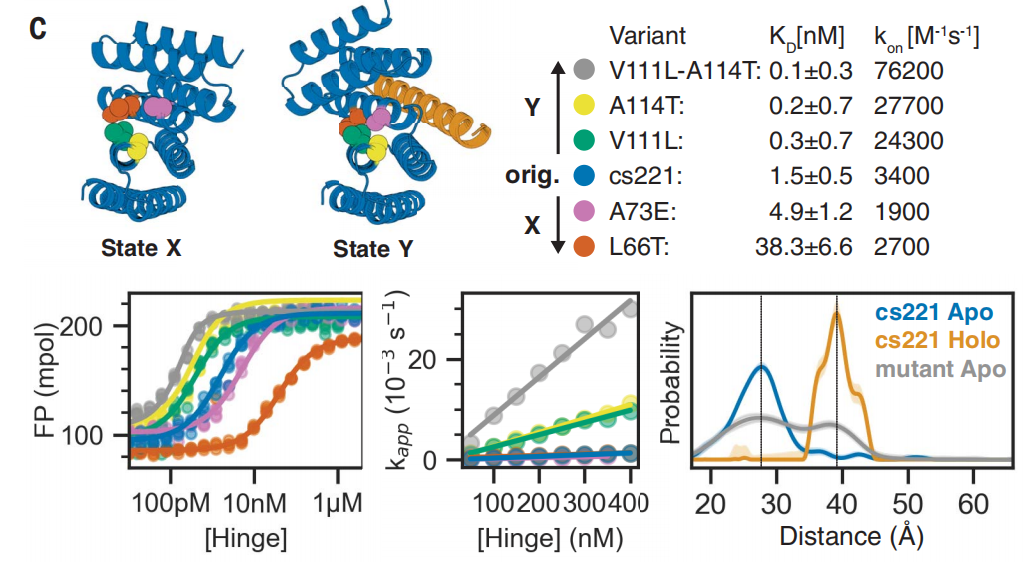
总的来说,这项新研究开发出了同时具有两种明确状态的铰链蛋白,可以应用于“蛋白质开关”的设计。这种双态开关的研究能使蛋白质设计超越静态结构,转向更复杂的多态组装和生物传感器设计,为蛋白设计提供了更广阔的可能性。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。



