生死大考!CD79b ADC将在今晚迎来ODAC灵魂拷问
来源:医药魔方 2023-03-09 11:38
同为基因泰克的产品,维泊妥珠单抗能否延续“前辈”利妥昔单抗的辉煌?要撼动R-CHOP的地位也并非易事。疗效、安全性、优势人群的选择、生物标志物的开发、以及药物经济学都是需要考虑的因素,相信这次ODAC
近些年,如果说哪类创新药最受关注,抗体偶联药物(ADC)一定不能缺席。无论是管线储备上,还是市场空间的想象上,ADC都可谓是当前最热门的赛道之一。目前,全球披露的ADC项目超过500个,已上市的ADC药物也有15款。
近日,阿斯利康以11.88亿美元引进康诺亚Claudin 18.2 ADC,石药集团以6.925亿美元将Nectin-4 ADC授权给Corbus,科伦博泰与默沙东就多款ADC达成近百亿美元交易等新闻的出现,无疑给本就火热的ADC赛道又添了一把火。
不过,再热的赛道也不乏冷静思考。
3月9日,罗氏的CD79b ADC维泊妥珠单抗(polatuzumab vedotin)将迎来肿瘤药物咨询委员会(ODAC)的灵魂拷问——基于III期POLARIX研究结果,评估维泊妥珠单抗在既往未经治疗的弥漫性大B细胞淋巴瘤(DLBCL)患者中的获益-风险情况,是否给与其一线治疗适应症。

DLBCL是最常见的淋巴瘤亚型,占非霍奇金淋巴瘤(NHL)的30%~40%。目前,R-CHOP方案(利妥昔单抗,环磷酰胺,多柔比星,长春新碱,泼尼松)是DLBCL的一线标准治疗,但仍有~40%的患者会出现初治耐药、难治或复发。复发或难治性(R/R)DLBCL的后续治疗也是临床上面临的难点。
▌维泊妥珠单抗的作用机制
在淋巴瘤领域,基于B细胞抗原方面的成功经验(例如:CD20),科学家们继续其他B细胞表面蛋白的探索。CD79b是B细胞受体(BCR)的一部分,在超过90%的B细胞-NHL中表达。CD79b与抗体结合后,可触发BCR和结合抗体的内化,这种特性提示可以将目标分子选择性递送给B细胞。内化后,BCR和结合抗体被降解,从而释放目标分子(细胞毒性药物)。
维泊妥珠单抗就是一种抗CD79b ADC,由三个部分组成:抗CD79b单克隆抗体,细胞毒性成分monomethyl auristatin(MMAE)(注:通过抑制微管蛋白,从而抑制有丝分裂),以及将两者共价结合的可切割连接物(linker)。
▌对DLBCL发起挑战:GO29365研究
临床上,约有50%的R/R DLBCL不适合强化挽救治疗和自体干细胞移植(SCT)的二线方案,这部分患者的预后较差。常见的治疗选择有R-GemOx方案(利妥昔单抗+吉西他滨+奥沙利铂)、BR方案(苯达莫司汀+利妥昔单抗)等,中位PFS在3.6~6.7个月。
维泊妥珠单抗对DLBCL发起的挑战始于GO29365研究,这是一项Ib/II期随机临床试验,纳入不适合接受造血干细胞移植的R/R DLBCL,随机分为维泊妥珠单抗+BR组(n=40)和BR组(n=40)。
结果显示,维泊妥珠单抗+BR组和BR组的完全缓解(CR)率分别为40%和18%。维泊妥珠单抗+BR组中获得CR或部分缓解(PR)的患者中,缓解持续时间(DOR)≥6个月的占64%,DOR≥1年的占48%,而BR组中这两个指标分别为30%和20%。
基于该数据,美国FDA于2019年6月10日加速批准(AA)维泊妥珠单抗+BR用于既往至少接受过2种治疗方案的R/R DLBCL。
2022年1月,《Blood Advances》发表了GO29365研究的OS结果。在随机化阶段之后,另有106名患者作为扩展队列接受了维泊妥珠单抗+BR治疗。最终共纳入192名R/R DLBCL患者,维泊妥珠单抗+BR组152名(安全性评估,n=6;随机化,n=40;扩展队列,n=106),BR组40名。

结果显示,维泊妥珠单抗+BR组和BR组的中位PFS分别为9.2个月和3.7个月(HR=0.39),中位OS分别为12.4个月和4.7个月(HR=0.42)。扩展队列中,独立审查委员会(IRC)评估的ORR为41.5%,CR率为38.7%,中位PFS和OS分别为6.6个月和12.5个月。在BR基础上联合维泊妥珠单抗可取得显著的生存获益。
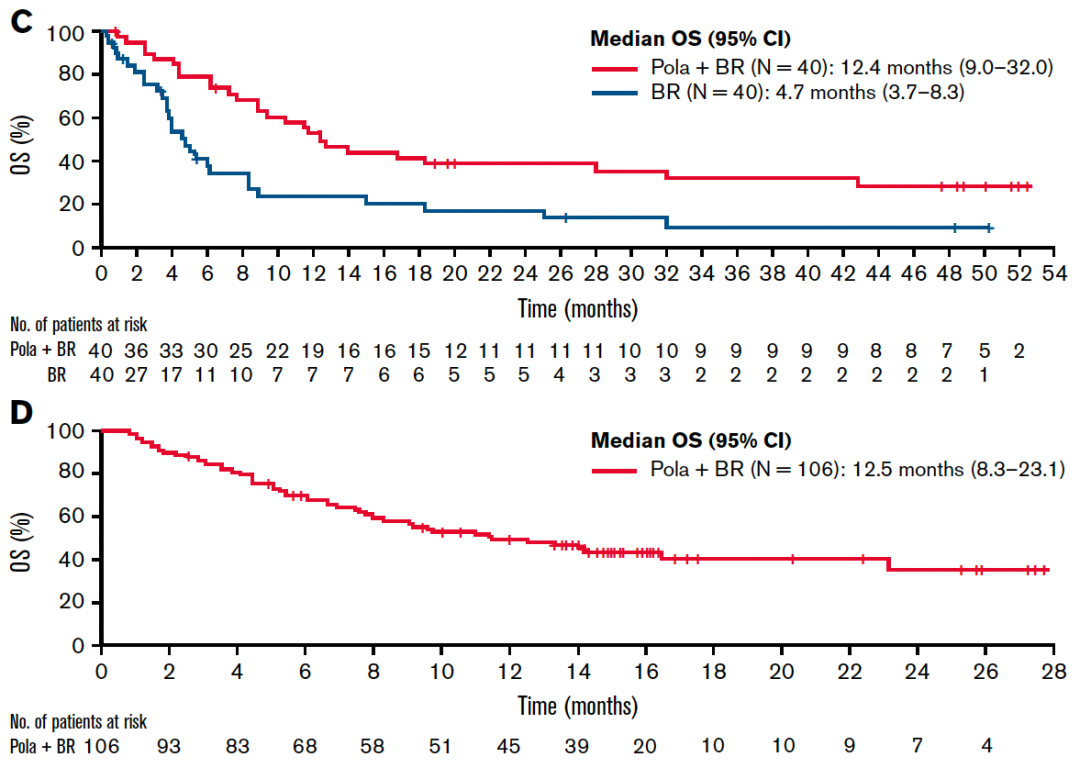
维泊妥珠单抗+BR组和BR组的OS.
GO29365研究里程碑. 图片来自DeepMed数据库
需要注意的是,FDA在2019年6月10日给与AA时,要求申办方在上市后完成两项验证性研究:
第一项:就是POLARIX研究(GO39942,NCT03274492),一项全球多中心、随机、双盲、安慰剂对照的III期临床研究,纳入既往未经治疗的DLBCL患者,按照1:1随机分为维泊妥珠单抗联合R-CHP组或R-CHOP组。主要终点为PFS,次要终点包括OS和安全性。
第二项:是POLARGO研究(MO40598,NCT04182204),一项III期、多中心、开放标签的随机化试验,旨在评估维泊妥珠单抗+利妥昔单抗、吉西他滨和奥沙利铂(R-GemOx)vs. R-GemOx用于R/R DLBCL的疗效与安全性。主要终点是OS,关键次要终点包括PFS、缓解率、安全性,重点关注周围神经病变(PN)的情况(注:2022年ASCO会议期间公布了安全性磨合阶段的初步结果,提示维泊妥珠单抗联合R-GemOx是安全且可耐受的)。
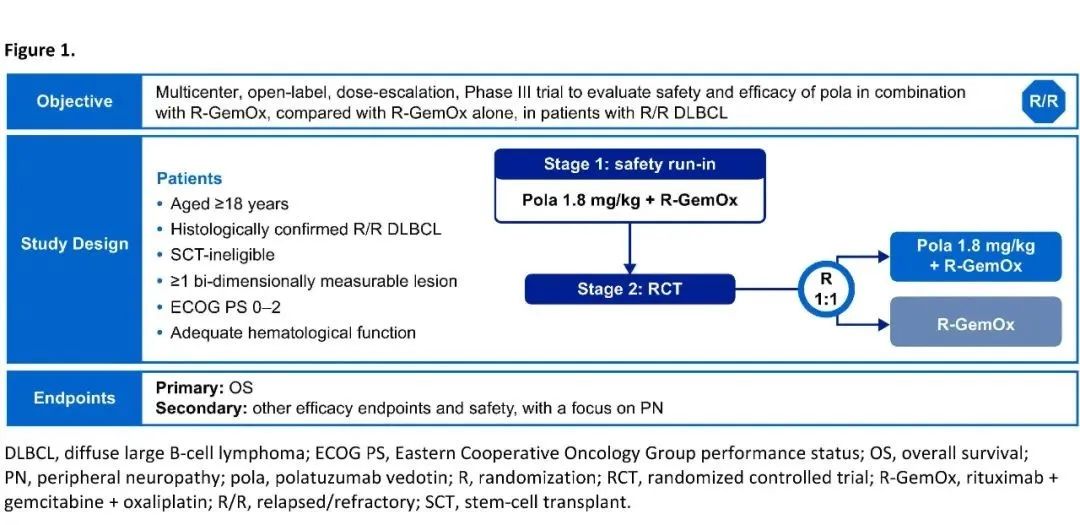
POLARGO研究设计
▌向DLBCL一线治疗推进:POLARIX研究
R-CHOP方案的一线治疗地位已有20多年,科学家们不断尝试和探索,希望能进一步提高疗效。然而,不论是强化治疗、巩固治疗、优化抗CD20单抗、还是联合新型靶向治疗药物等,均未有优效于R-CHOP方案的依据。使用医药魔方DeepMed数据库对比功能,下图展示了伊布替尼PHOENIX研究、来那度胺ROBUST研究、硼替佐米REMoDL-B研究以及维泊妥珠单抗POLARIX研究的主要信息。
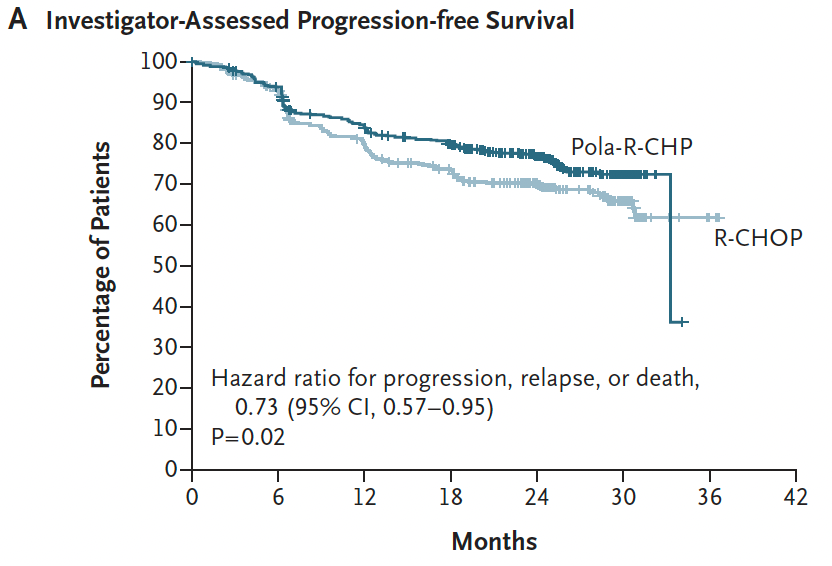
2021年美国血液学会(ASH)年会上,维泊妥珠单抗联合R-CHP(利妥昔单抗,环磷酰胺,多柔比星,泼尼松)对比R-CHOP(利妥昔单抗,环磷酰胺,多柔比星,长春新碱,泼尼松)一线治疗DLBCL的III期POLARIX研究公布详细数据,并同步发表在《新英格兰医学》上。
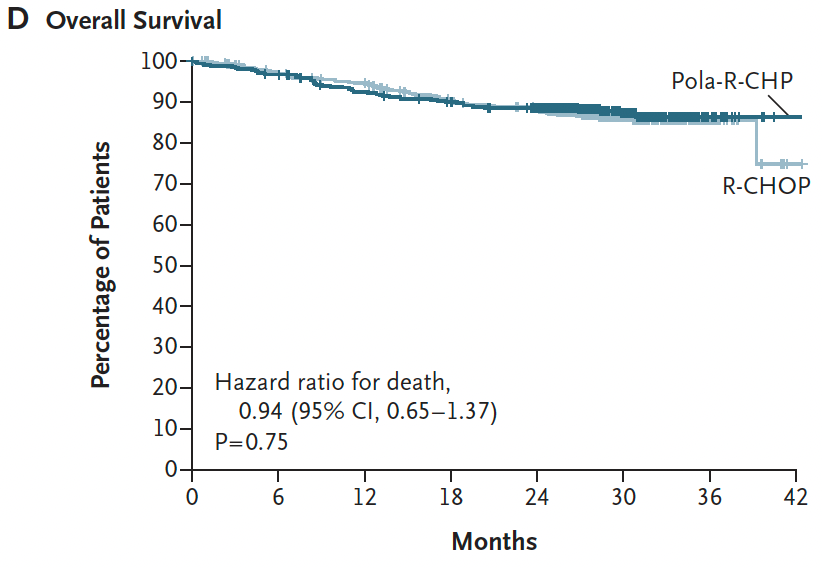
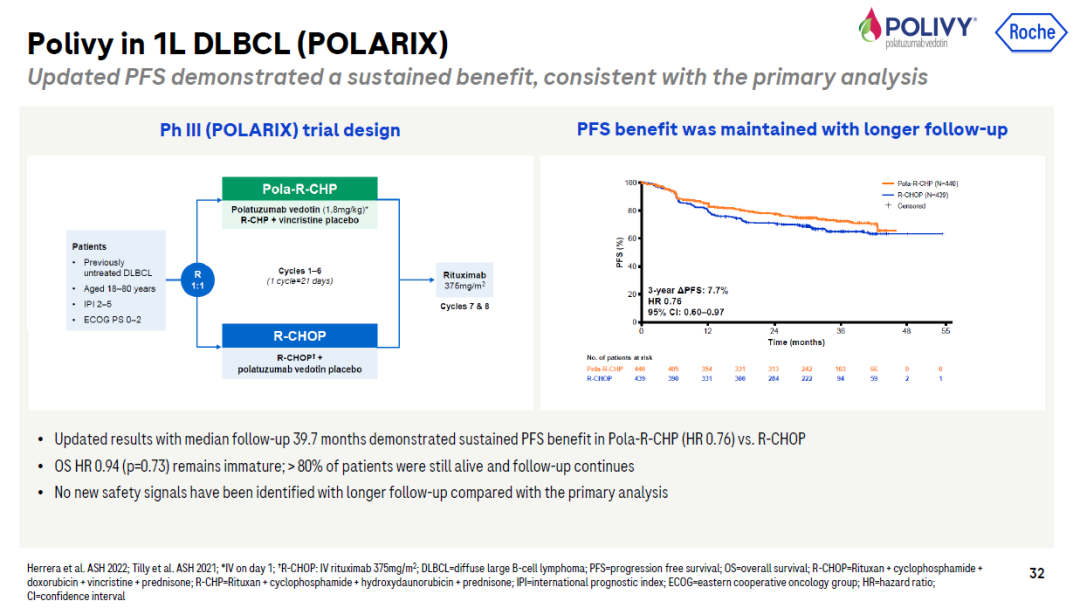
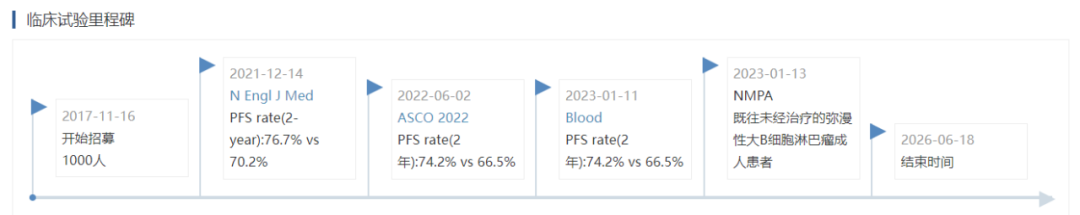
POLARIX研究里程碑. 图片来自DeepMed数据库
▌POLARIX研究亚洲人群数据
亚洲人群数据也是大家关心的问题。2023年1月,《Blood》发布了POLARIX研究亚洲人群数据分析结果。共纳入281例患者,全球研究意向性治疗(ITT)人群中来自亚洲的有160例,121例来自ITT中国扩展队列,旨在评估亚洲人群与全球人群PFS的一致性。其中141人被随机分配到维泊妥珠单抗联合R-CHP组,140人被分配到R-CHOP组。
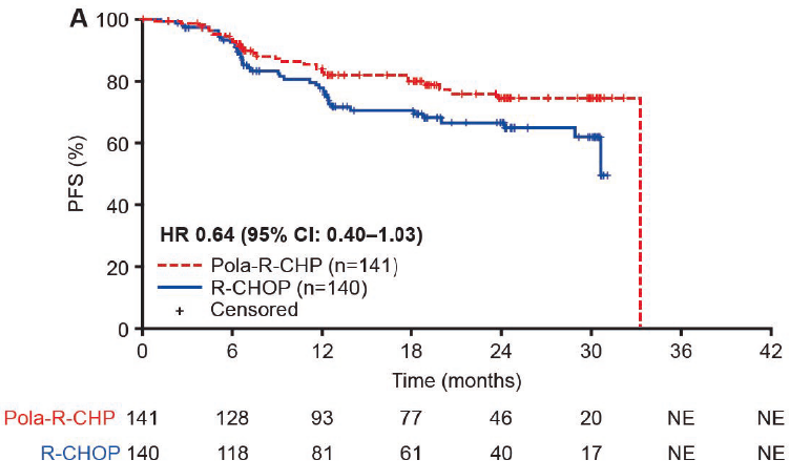
两组的安全性相当,包括3-4级不良事件发生率(72.9% vs. 66.2%)、严重AEs(32.9% vs 32.4%),5级AEs(1.4% vs 0.7%),造成治疗中断的AEs(5.0% vs 7.2%),以及任何级别的周围神经病变(44.3% vs 50.4%)。
OS数据在分析时尚未成熟[ 维泊妥珠单抗联合R-CHP组:10例死亡(7.1%),R-CHOP组:15例死亡(10.7%)],未分层HR=0.64(95%CI 0.29-1.42)(下图)。
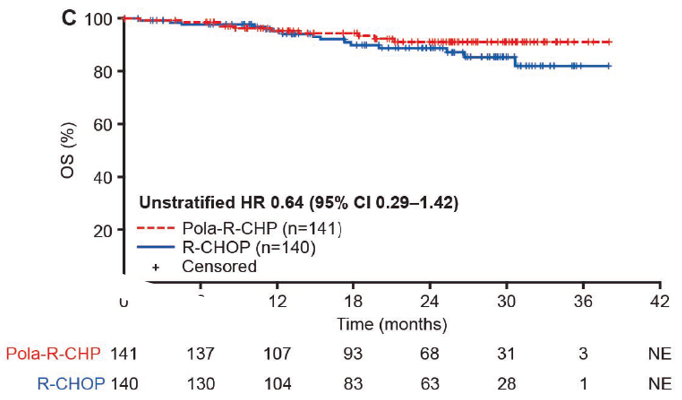
▌领域内的讨论
随着POLARIX研究结果的公布,引起领域内的广泛关注,维泊妥珠单抗联合R-CHP是否应被视为新的一线标准治疗方案成为讨论热点。虽然产生了PFS获益且几乎没有毒性增加,但由于不能提高CR率,以及目前尚未能显示出明确的OS获益,使得其循证依据显得并不那么完美。
为何PFS改善未能转换为OS获益,具体原因尚不清楚。一个可能的原因是,在接受维泊妥珠单抗联合R-CHP后,复杂的生物学特征使得后续治疗更加困难——获得更好肿瘤退缩的同时,残留与疾病复发相关的肿瘤细胞。其次,巩固性放疗可能会“平衡”两组间的OS。此外,还有更复杂的因素,包括淋巴瘤微环境和免疫系统中的靶点。有一个重要的提示来自亚组分析,亚组分析显示,年龄较大(>60岁)的高危男性患者似乎更能从维泊妥珠单抗治疗中获益,尤其是ABC亚型。因此,我们或需要更理想的分子标志物以明确亚组分析中得到的提示,寻找出最适合接受维泊妥珠单抗治疗的目标人群。从另一个角度来看,当一线使用维泊妥珠单抗联合R-CHP而不是R-CHOP时,可能就会在二线或后线治疗中失去了一种强有效的药物,特别是对于不适合强化挽救治疗或不符合自身移植条件,以及那些需要有效的桥接方案以接受CAR-T治疗的患者。
药物经济学也是临床医生在选择治疗方案时需要考虑的重要因素。2022年12月,《Blood》也发表了相关研究,用模型来评估维泊妥珠单抗联合R-CHP和R-CHOP的成本效益,通过POLARIX结果预估PFS和OS,结果以增量成本-效益比来描述。支付意愿(WTP)阈值为15万美元/质量调整生命年(QALY)。
分析显示,如果维泊妥珠单抗联合R-CHP的5年PFS为69.6%,R-CHOP为62.7%,则在WTP为15万美元/QALY的情况下,维泊妥珠单抗联合R-CHP具有成本-效益。如果5年PFS为66.1%或更低,则不再具有成本-效益。因此,维泊妥珠单抗联合R-CHP是否具有成本-效益,高度取决于PFS获益能否随着时间的推移而保持,此外还与CAR-T疗法等成本有关。制定合理的价格或明确最可能获益的目标人群可能有助于提高维泊妥珠单抗的成本-效益。
临床医生对维泊妥珠单抗又持怎样的态度呢?英国血液学会官方期刊《eJHAEM》曾在2022年做过一项问卷调查。174名受访医生中,大多数来自美国的医学中心(57%)。70%的受访者表示,考虑到PFS差异不够充分,缺乏OS获益,且经济成本较高,在是否会用维泊妥珠单抗联合R-CHP替代R-CHOP方案的问题上仍旧非常谨慎,在调查过程中也观察到医生观点的不一致。
同为基因泰克的产品,维泊妥珠单抗能否延续“前辈”利妥昔单抗的辉煌?要撼动R-CHOP的地位也并非易事。疗效、安全性、优势人群的选择、生物标志物的开发、以及药物经济学都是需要考虑的因素,相信这次ODAC会给DLBCL的治疗理念带来重要的参考价值。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


