Cell Res:清华大学俞立团队揭示基于迁移体的新型细胞分泌模式
来源:生物世界 2024-07-01 09:28
在这项最新研究中,研究团队发现分泌蛋白(包括信号蛋白)通过组成性分泌途径和调节性分泌途径被分泌载体运输到迁移体中。
2014年,清华大学俞立团队在 Cell Research 期刊发表论文【1】,发现了一种新的细胞器——迁移体(Migrasome)。
此后,俞立团队发表多篇论文,进一步揭示了迁移体的产生机制及其功能。例如,2021年5月,俞立团队在 Cell 期刊发表论文【2】,将新型细胞器迁移体与线粒体联系了起来,该研究发现在细胞外的迁移体中存在线粒体,并进一步揭示了迁移体的功能——轻度线粒体应激后,受损的线粒体会被转运到迁移体中,再被迁移体运送到细胞外。这一过程被命名为线粒体胞吐(Mitocytosis),是细胞对线粒体的一种质控过程,把受损的线粒体清理出去。
迁移体中富含信号分子(例如趋化因子、细胞因子和血管生成因子),其对这些信号分子的空间精确递送方面发挥着关键作用,影响着包括器官形态发生及血管生成在内的关键生理过程。然而,调控这些信号分子在迁移体中积累的机制一直不明确。
2024年6月25日,清华大学俞立教授团队在 Cell Research 期刊发表了题为:Localized, highly efficient secretion of signaling proteins by migrasomes 的研究论文【3】。
该研究提供了令人信服的证据,表明迁移体是迁移细胞的主要分泌途径,揭示了一种之前未知的特化的、高度局部化的分泌模式,其在概念上与在神经元系统中观察到的靶向神经递质释放(突触囊泡释放)相似。

迁移细胞中的迁移体(Migrasome)是新近发现的细胞器,是一种平均直径约2µm的囊泡结构。迁移体在将信号分子靶向递送至精确位置方面发挥着辅助作用,从而对需要整合空间和化学信息的生理过程产生重大影响。俞立团队在此前的研究中发现,迁移体中的趋化因子和生长因子对器官形态发生过程发挥重要作用;而在鸡胚胎中的迁移单核细胞沿着其迁移轨迹释放富含血管内皮生长因子A(VEGFA)的迁移体,从而协调毛细血管生长并在血管生成中发挥关键作用。
然而,迁移体在选择性转运和随后释放这些信号分子的精确机制仍有待完全阐明。
细胞分泌是一项基本的生物学过程,它始于信号肽引导分泌蛋白进入内质网(ER)。在信号肽被剪切后,这些蛋白质通过COPII包被的囊泡被运送到高尔基体复合体。在高尔基体内,它们会进一步进行翻译后修饰,然后通过组成性分泌途径或调节性分泌途径被定向释放。尤其是调节性途径,需要颗粒或细胞器中间体进行分泌,并由特定的细胞信号激活。在此背景下,循环内体,尤其是富含VAMP3的管状突起对于某些Rab GTP酶(例如Rab11)控制TNF等分泌性货物定向输送至细胞膜至关重要。相比之下,Rab8通常与组成性分泌途径相关。
马达蛋白(包括驱动蛋白、动力蛋白和肌球蛋白),在分泌囊泡的细胞内转运中发挥关键作用。这些蛋白穿过细胞骨架网络,驱动蛋白和动力蛋白促进微管的远距离运输,肌球蛋白协调囊泡沿肌动蛋白丝的短程运动。这对分泌的最后步骤至关重要,包括囊泡对接和与质膜的融合。分泌载体与质膜的最终融合是由Q-SNARE(例如SNAP23)和R-SNARE(例如VAMP2和VAMP3)介导,各种研究表明,SNARE蛋白水平是细胞因子分泌的限速步骤。分泌效率和分泌量受膜上SNARE蛋白水平的调节,因此,SNARE蛋白的膜密度决定了分泌的倾向性。
神经元中存在着高度局部分泌,在神经元中,含有神经递质的突触囊泡通过轴突运输被运送到轴突末端,由马达蛋白驱动。到达后,囊泡释放被激活,等待动作电位触发神经递质在轴突末端的释放——这是突触传递的关键步骤。但其他细胞类型是否也具有类似的特化的分泌机制,目前仍有待证明。除了轴突末端之外,在其他特化细胞结构中发生此类过程的情况尚未得到充分了解。
在这项最新研究中,研究团队发现分泌蛋白(包括信号蛋白)通过组成性分泌途径和调节性分泌途径被分泌载体运输到迁移体中。在细胞迁移过程中,在肌动蛋白依赖性马达蛋白Myosin-5a的驱动下,这些分泌载体的很大一部分被重定向到细胞后方并主动转运到迁移体中。一旦到达迁移体,这些分泌载体通过SNARE介导的机制与迁移体膜融合。
值得注意的是,该研究还发现,抑制迁移体形成会显著减少迁移细胞的分泌,这表明迁移体是迁移细胞的主要分泌途径。
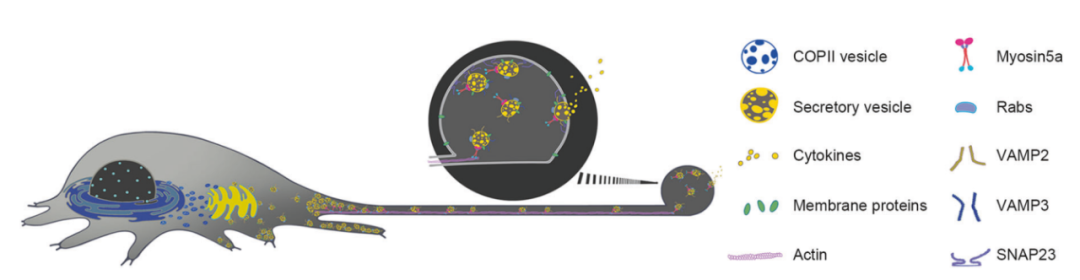
据于这些数据,研究团队提出了一种之前未知的特化的、高度局部化的分泌模式,在概念上与在神经元系统中观察到的靶向神经递质释放(突触囊泡释放)相似。
论文链接:
1. https://www.nature.com/articles/cr2014135
2. https://doi.org/10.1016/j.cell.2021.04.029
3. https://www.nature.com/articles/s41422-024-00992-7
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


